编者按:
心血管-肾脏-代谢(CKM)综合征作为近年来的学术热点,备受临床关注。在近期于南京召开的2026胰岛代谢学术会议(IMF)期间,首都医科大学附属北京朝阳医院内分泌科王广教授围绕“代谢标志物在CKM综合征中的预测价值”主题,从残余胆固醇调控、甲状腺激素敏感性的性别差异,到数据驱动的聚类分型进行了全面梳理,为CKM综合征的早期识别与精准干预提供了新的思路。

王广教授
博士、主任医师、二级教授、博士生导师
首都医科大学附属北京朝阳医院内分泌科主任;
首都医科大学内分泌代谢学系主任;
中华医学会内分泌学分会 常务委员;
北京医学会内分泌学分会 候任主任委员;
北京市战略科技人才、北京市领军人才、北京市登峰人才;
第七届“全国优秀科技工作者”;
主持国家科技部重点研发项目及国家自然科学基金6项;
以第一或通讯作者在Science、Nature Medicine、Metabolism、Cell Metabolism等发表论文90余篇。
一、要而论之:CKM综合征概述
2023年10月,美国心脏协会(AHA)首次提出心血管-肾脏-代谢(cardiovascular-kidney-metabolic,CKM)综合征的概念,将其定义为:一种由肥胖、糖尿病、慢性肾脏疾病(CKD)和心血管疾病(CVD,包括心力衰竭、心房颤动、冠心病、脑卒中和外周动脉疾病)之间病理生理相互作用导致的全身性疾病(图1)[1]。
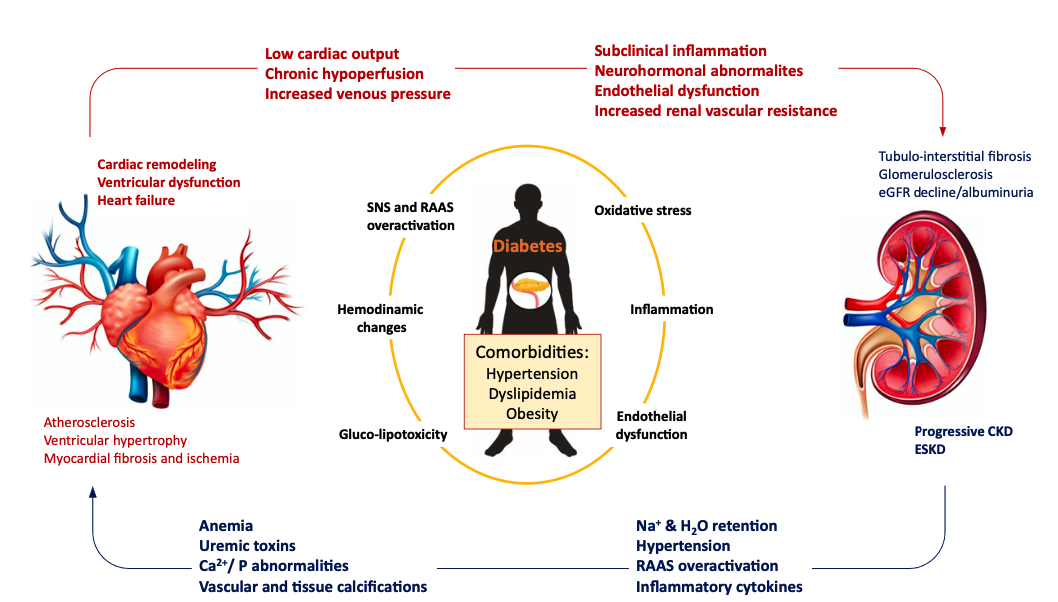
图1. 心血管-肾脏-代谢(CKM)综合征的定义
CKM综合征分为0~4期,阶段越高,心血管死亡风险越大[2]。美国NHANES 2011-2020年队列研究[3]显示,CKM 2期患病率最高,晚期CKM患病率已达14.6%。值得关注的是,CKM综合征在早期阶段具有明确的可干预临床轨迹[4,5]。CKM综合征的代谢损害源头,在于过度脂肪沉积和胰岛素抵抗。因此,早期识别能够反映代谢紊乱的生物标志物,对于阻断CKM进展具有重要意义,这也成为当前研究与临床实践的重点方向。
二、残余胆固醇对CKM综合征的调控
残余胆固醇(Remnant Cholesterol, RC)是指富含甘油三酯脂蛋白(如极低密度脂蛋白VLDL、中密度脂蛋白IDL和乳糜微粒残余)中的胆固醇成分。与低密度脂蛋白胆固醇(LDL-C)不同,RC颗粒更小、致动脉粥样硬化作用更强,能够直接诱导巨噬细胞泡沫细胞形成,加速动脉粥样斑块进展。
王广教授课题组的前期研究为RC的临床意义提供了重要证据。首先,研究发现RC升高是中国糖尿病人群中高血压发生的独立预测因素[6]:与RC最低五分位组相比,最高五分位组高血压风险显著升高(HR=1.69,95%CI:1.31~2.18,P<0.0001),其预测能力优于甘油三酯(图2,左)。
其次,研究还发现甲状腺激素敏感性降低与高RC水平显著有关[7]:无论男女,在调整年龄和体重指数(BMI)后,TFQI、TSHI、TT4RI水平越高,RC水平越高;FT3/FT4比值越高,RC水平越低(所有趋势检验P值均<0.001)(图2,右)。这些发现为RC在CKM综合征中的作用提供了重要线索。

图2. 残余胆固醇的临床关联(左:RC与高血压风险;右:RC与甲状腺激素敏感性)
在此基础上,课题组基于中国健康与养老追踪调查(CHARLS)数据库开展了深入研究,进一步揭示了RC与CKM的密切关联[8]。该研究纳入CHARLS 2011-2020年数据(共17708名参与者),中位随访时间达9.0年。结果显示:随着RC水平升高,中晚期CKM的比例明显上升;无论是基线水平还是在随访过程中,RC水平升高均与CKM进展相关,且在各亚组(包括不同年龄、性别、婚姻状况、居住地、吸烟和饮酒)中二者关系稳健。
综上,RC水平与晚期CKM独立相关;RC升高增加了CKM 0~3期患者发生CVD的风险;RC是被忽视的CKM风险信号,具备低成本、可重复、潜在可干预的优势,值得在临床筛查中推广应用。
三、甲状腺激素敏感性与CKM综合征的性别差异关联
甲状腺激素调控着心血管、肝脏、肾脏、糖脂代谢等多个系统。传统的激素研究多聚焦于“水平是否正常”,但王广教授团队的研究进一步提示:真正影响代谢风险的,是激素作用效应的“灵敏度”。甲状腺激素敏感性能否作为“代谢健康状态”的量化指标?这是团队研究的核心切入点。
课题组前期已从多个代谢维度证实了甲状腺激素敏感性的广泛影响。研究发现,甲状腺激素敏感性降低与高同型半胱氨酸(Hcy)升高[9]、内脏脂肪指数(VAI)升高[10]、残余胆固醇升高[7]、非酒精性脂肪性肝病(NAFLD)患病率增加[11]及妊娠期糖尿病(GDM)风险增加[12]均显著相关。这些发现表明,甲状腺激素敏感性可能是反映全身代谢状态的一个整合性指标。
基于上述扎实的研究基础,研究团队纳入8391名甲状腺功能正常的成年人,采用Logistic回归与限制性立方样条分析(RCS),系统评估甲状腺激素敏感性与CKM综合征(stage 2)的关联[13]。结果显示:甲状腺激素敏感性下降显著增加CKM风险,且男性比女性更易受影响,限制性立方样条分析进一步证实了这一性别差异(图3)。

图3. 男性比女性更易受甲状腺激素敏感性影响
年龄分层分析进一步揭示:在>50岁男性中,甲状腺激素敏感性与CKM综合征的关联最为显著;而在35~50岁女性中,甲状腺激素敏感性同样影响CKM综合征的发生风险。
以上发现提示,甲状腺激素敏感性下降是CKM综合征的重要危险因素,尤其在老年男性中。因此,甲状腺激素敏感性指标可作为评估CKM风险的潜在生物标志物,用于实现精准筛查策略。在个性化干预方面,男性(尤其是50岁以上)可能需要更严格的甲状腺功能监测和代谢管理,以早期识别高危人群,切实降低CKM综合征的发生风险。
四、数据驱动的聚类分析识别CKM综合征的不同亚型
在临床实践中,早期CKM患者(仅表现为代谢危险因素)具有高度异质性,其未来发展为心、肾等特定器官并发症的风险差异显著。现有的分期系统难以对此风险进行精准区分,导致预防策略缺乏针对性。为此,王广教授课题组引入无监督机器学习聚类方法,旨在基于临床数据,从早期CKM患者中识别出具有不同并发症风险的独特表型。
研究数据来源于UK Biobank数据库,纳入CKM 1~3期患者(训练集34487人,验证集9713人),中位随访15.88年。通过11个基线代谢指标进行聚类分析,识别出五个临床亚型(图4)[14]:
LR(低风险组):各项代谢指标相对正常,并发症风险均最低;
LHR(代谢性肝病高危组):以肝功能和脂代谢指标异常为主,慢性肝病风险最高;
CBHR(脑血管高危组):以血压和UACR升高为主,脑血管事件风险最高;
ADHR(年龄相关风险组):以高龄为特点,脑血管事件与CKD风险较高;
CRHR(代谢炎症-心肾高危组):多种代谢紊乱伴炎症因子升高,CVD与CKD风险最高。

图4. 五个临床亚型的基线聚类特征和累积疾病发生结局
在累积疾病发生结局方面,各亚型呈现出明显的差异。多基因风险评分分析显示:高血压与卒中的遗传风险主要富集于脑血管高危组(CBHR),而BMI、CVD和2型糖尿病的遗传风险则主要富集于代谢炎症-心肾高危组(CRHR)。
在遗传变异层面,三个高危位点呈现亚型特异性富集:APOE ε4(rs429358 T>C)主要富集于脑血管高危组(CBHR),FTO rs9939609 T>A主要富集于代谢炎症-心肾高危组(CRHR),而TM6SF2 rs58542926 C>T则主要富集于代谢性肝病高危组(LHR)。
蛋白质组学分析进一步揭示了各亚型的生物学特征(图5):
LHR(代谢性肝病高危组)显著富集于代谢过程,尤其是小分子分解代谢、氨基酸代谢及细胞色素P450介导的外源物代谢;
CBHR(脑血管高危组)主要涉及代谢调控、血管重塑、神经活性配体-受体相互作用及松弛素信号通路;
ADHR(年龄相关风险组)以体液免疫、趋化因子信号及激素信号通路的富集为特征;
CRHR(代谢炎症-心肾高危组)富集于趋化作用、体液免疫应答及炎症通路。

图5. 不同亚组血浆蛋白质组学特征
综上所述,基于UK Biobank数据,利用临床生物标志物对CKM综合征进行分型,所识别的5个亚型(LR、LHR、CBHR、ADHR、CRHR)具备独特的血浆蛋白质组学特征与遗传风险模式,为识别高危CKM患者并开展靶向干预提供科学依据。此外,非肥胖且NCCR水平较高的个体CMM风险最低,提示在评估CMM风险时需要同时关注肌肉量和脂肪量。
五、结语
CKM综合征整合心血管、肾脏与代谢三大系统,为临床实践提供了更广阔的视野。王广教授团队从残余胆固醇、甲状腺激素敏感性到聚类分型,层层深入,为CKM早期识别与精准干预提供了重要依据。残余胆固醇是低成本、可干预的风险信号;甲状腺激素敏感性揭示了性别与年龄差异;聚类分型实现了从“分期”到“分型”的跨越。未来,随着多组学与人工智能的融入,CKM精准管理将更加可及,需多学科共同努力,为患者带来更长远的健康获益。
参考文献
[1] Ndumele CE, Neeland IJ, Tuttle KR et al. A Synopsis of the Evidence for the Science and Clinical Management of Cardiovascular-Kidney-Metabolic (CKM) Syndrome: A Scientific Statement From the American Heart Association. Circulation 2023; 148 (20): 1636-1664.
[2] Siddiqi TJ, Cherney D, Siddiqui HF et al. Effects of Sodium-Glucose Cotransporter-2 Inhibitors on Kidney Outcomes across Baseline Cardiovascular-Kidney-Metabolic Conditions: A Systematic Review and Meta-Analyses. J Am Soc Nephrol 2025; 36 (2): 242-255.
[3] Minhas AMK, Mathew RO, Sperling LS et al. Prevalence of the Cardiovascular-Kidney-Metabolic Syndrome in the United States. J Am Coll Cardiol 2024; 83 (18): 1824-1826.
[4] Kittelson KS, Junior AG, Fillmore N et al. Cardiovascular-kidney-metabolic syndrome - An integrative review. Prog Cardiovasc Dis 2024; 87: 26-36.
[5] Claudel SE, Verma A. Cardiovascular-kidney-metabolic syndrome: A step toward multidisciplinary and inclusive care. Cell Metab 2023; 35 (12): 2104-2106.
[6] Wang J, Sun Q, An Y et al. The association of remnant cholesterol (RC) and interaction between RC and diabetes on the subsequent risk of hypertension. Frontiers in Endocrinology 2022; Volume 13 - 2022.
[7] Sun H, Zhu W, Liu J et al. Reduced Sensitivity to Thyroid Hormones Is Associated With High Remnant Cholesterol Levels in Chinese Euthyroid Adults. The Journal of Clinical Endocrinology & Metabolism 2023; 108 (1): 166-174.
[8] Ding X, Tian J, Chang X et al. Association between remnant cholesterol and the risk of cardiovascular-kidney-metabolic syndrome progression: insights from the China health and retirement longitudinal study. European Journal of Preventive Cardiology 2025; 32 (13): 1157-1165.
[9] Ding X, Wang Y, Liu J et al. Impaired Sensitivity to Thyroid Hormones Is Associated With Elevated Homocysteine Levels in the Euthyroid Population. The Journal of Clinical Endocrinology & Metabolism 2022; 107 (9): e3731-e3737.
[10] Wei Y, Yang M, Liu J et al. Associations Between Sensitivity to Thyroid Hormones and Visceral Adiposity in Euthyroid Adults. J Clin Endocrinol Metab 2025; 110 (8): e2744-e2753.
[11] Zhou L, Jiang L, An Y et al. Association of Sensitivity to Thyroid Hormones and Non-Alcoholic Fatty Liver Disease and the Severity of Liver Fibrosis in Euthyroid Adults: A Retrospective Study. Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy 2025; 18 (null): 479-490.
[12] Sun H, Zhou Y, Liu J et al. Maternal pre-pregnancy obesity modifies the association between first-trimester thyroid hormone sensitivity and gestational Diabetes Mellitus: a retrospective study from Northern China. Diabetol Metab Syndr 2023; 15 (1): 212.
[13] Jiang L, Zhou L, Liu J et al. Sex Differences in the Association Between Thyroid Hormone Sensitivity and Cardiovascular-Kidney-Metabolic Syndrome. J Clin Endocrinol Metab 2025; 110 (10): e3303-e3312.
[14] Yang M, Su C, Chang X et al. Data-driven cluster analysis identifies distinct types of cardiovascular-kidney-metabolic syndrome. European Journal of Preventive Cardiology 2025. 2 comments
心血管-肾脏-代谢(CKM)综合征作为近年来的学术热点,备受临床关注。在近期于南京召开的2026胰岛代谢学术会议(IMF)期间,首都医科大学附属北京朝阳医院内分泌科王广教授围绕“代谢标志物在CKM综合征中的预测价值”主题,从残余胆固醇调控、甲状腺激素敏感性的性别差异,到数据驱动的聚类分型进行了全面梳理,为CKM综合征的早期识别与精准干预提供了新的思路。

王广教授
博士、主任医师、二级教授、博士生导师
首都医科大学附属北京朝阳医院内分泌科主任;
首都医科大学内分泌代谢学系主任;
中华医学会内分泌学分会 常务委员;
北京医学会内分泌学分会 候任主任委员;
北京市战略科技人才、北京市领军人才、北京市登峰人才;
第七届“全国优秀科技工作者”;
主持国家科技部重点研发项目及国家自然科学基金6项;
以第一或通讯作者在Science、Nature Medicine、Metabolism、Cell Metabolism等发表论文90余篇。
一、要而论之:CKM综合征概述
2023年10月,美国心脏协会(AHA)首次提出心血管-肾脏-代谢(cardiovascular-kidney-metabolic,CKM)综合征的概念,将其定义为:一种由肥胖、糖尿病、慢性肾脏疾病(CKD)和心血管疾病(CVD,包括心力衰竭、心房颤动、冠心病、脑卒中和外周动脉疾病)之间病理生理相互作用导致的全身性疾病(图1)[1]。

图1. 心血管-肾脏-代谢(CKM)综合征的定义
CKM综合征分为0~4期,阶段越高,心血管死亡风险越大[2]。美国NHANES 2011-2020年队列研究[3]显示,CKM 2期患病率最高,晚期CKM患病率已达14.6%。值得关注的是,CKM综合征在早期阶段具有明确的可干预临床轨迹[4,5]。CKM综合征的代谢损害源头,在于过度脂肪沉积和胰岛素抵抗。因此,早期识别能够反映代谢紊乱的生物标志物,对于阻断CKM进展具有重要意义,这也成为当前研究与临床实践的重点方向。
二、残余胆固醇对CKM综合征的调控
残余胆固醇(Remnant Cholesterol, RC)是指富含甘油三酯脂蛋白(如极低密度脂蛋白VLDL、中密度脂蛋白IDL和乳糜微粒残余)中的胆固醇成分。与低密度脂蛋白胆固醇(LDL-C)不同,RC颗粒更小、致动脉粥样硬化作用更强,能够直接诱导巨噬细胞泡沫细胞形成,加速动脉粥样斑块进展。
王广教授课题组的前期研究为RC的临床意义提供了重要证据。首先,研究发现RC升高是中国糖尿病人群中高血压发生的独立预测因素[6]:与RC最低五分位组相比,最高五分位组高血压风险显著升高(HR=1.69,95%CI:1.31~2.18,P<0.0001),其预测能力优于甘油三酯(图2,左)。
其次,研究还发现甲状腺激素敏感性降低与高RC水平显著有关[7]:无论男女,在调整年龄和体重指数(BMI)后,TFQI、TSHI、TT4RI水平越高,RC水平越高;FT3/FT4比值越高,RC水平越低(所有趋势检验P值均<0.001)(图2,右)。这些发现为RC在CKM综合征中的作用提供了重要线索。

图2. 残余胆固醇的临床关联(左:RC与高血压风险;右:RC与甲状腺激素敏感性)
在此基础上,课题组基于中国健康与养老追踪调查(CHARLS)数据库开展了深入研究,进一步揭示了RC与CKM的密切关联[8]。该研究纳入CHARLS 2011-2020年数据(共17708名参与者),中位随访时间达9.0年。结果显示:随着RC水平升高,中晚期CKM的比例明显上升;无论是基线水平还是在随访过程中,RC水平升高均与CKM进展相关,且在各亚组(包括不同年龄、性别、婚姻状况、居住地、吸烟和饮酒)中二者关系稳健。
综上,RC水平与晚期CKM独立相关;RC升高增加了CKM 0~3期患者发生CVD的风险;RC是被忽视的CKM风险信号,具备低成本、可重复、潜在可干预的优势,值得在临床筛查中推广应用。
三、甲状腺激素敏感性与CKM综合征的性别差异关联
甲状腺激素调控着心血管、肝脏、肾脏、糖脂代谢等多个系统。传统的激素研究多聚焦于“水平是否正常”,但王广教授团队的研究进一步提示:真正影响代谢风险的,是激素作用效应的“灵敏度”。甲状腺激素敏感性能否作为“代谢健康状态”的量化指标?这是团队研究的核心切入点。
课题组前期已从多个代谢维度证实了甲状腺激素敏感性的广泛影响。研究发现,甲状腺激素敏感性降低与高同型半胱氨酸(Hcy)升高[9]、内脏脂肪指数(VAI)升高[10]、残余胆固醇升高[7]、非酒精性脂肪性肝病(NAFLD)患病率增加[11]及妊娠期糖尿病(GDM)风险增加[12]均显著相关。这些发现表明,甲状腺激素敏感性可能是反映全身代谢状态的一个整合性指标。
基于上述扎实的研究基础,研究团队纳入8391名甲状腺功能正常的成年人,采用Logistic回归与限制性立方样条分析(RCS),系统评估甲状腺激素敏感性与CKM综合征(stage 2)的关联[13]。结果显示:甲状腺激素敏感性下降显著增加CKM风险,且男性比女性更易受影响,限制性立方样条分析进一步证实了这一性别差异(图3)。

图3. 男性比女性更易受甲状腺激素敏感性影响
年龄分层分析进一步揭示:在>50岁男性中,甲状腺激素敏感性与CKM综合征的关联最为显著;而在35~50岁女性中,甲状腺激素敏感性同样影响CKM综合征的发生风险。
以上发现提示,甲状腺激素敏感性下降是CKM综合征的重要危险因素,尤其在老年男性中。因此,甲状腺激素敏感性指标可作为评估CKM风险的潜在生物标志物,用于实现精准筛查策略。在个性化干预方面,男性(尤其是50岁以上)可能需要更严格的甲状腺功能监测和代谢管理,以早期识别高危人群,切实降低CKM综合征的发生风险。
四、数据驱动的聚类分析识别CKM综合征的不同亚型
在临床实践中,早期CKM患者(仅表现为代谢危险因素)具有高度异质性,其未来发展为心、肾等特定器官并发症的风险差异显著。现有的分期系统难以对此风险进行精准区分,导致预防策略缺乏针对性。为此,王广教授课题组引入无监督机器学习聚类方法,旨在基于临床数据,从早期CKM患者中识别出具有不同并发症风险的独特表型。
研究数据来源于UK Biobank数据库,纳入CKM 1~3期患者(训练集34487人,验证集9713人),中位随访15.88年。通过11个基线代谢指标进行聚类分析,识别出五个临床亚型(图4)[14]:
LR(低风险组):各项代谢指标相对正常,并发症风险均最低;
LHR(代谢性肝病高危组):以肝功能和脂代谢指标异常为主,慢性肝病风险最高;
CBHR(脑血管高危组):以血压和UACR升高为主,脑血管事件风险最高;
ADHR(年龄相关风险组):以高龄为特点,脑血管事件与CKD风险较高;
CRHR(代谢炎症-心肾高危组):多种代谢紊乱伴炎症因子升高,CVD与CKD风险最高。

图4. 五个临床亚型的基线聚类特征和累积疾病发生结局
在累积疾病发生结局方面,各亚型呈现出明显的差异。多基因风险评分分析显示:高血压与卒中的遗传风险主要富集于脑血管高危组(CBHR),而BMI、CVD和2型糖尿病的遗传风险则主要富集于代谢炎症-心肾高危组(CRHR)。
在遗传变异层面,三个高危位点呈现亚型特异性富集:APOE ε4(rs429358 T>C)主要富集于脑血管高危组(CBHR),FTO rs9939609 T>A主要富集于代谢炎症-心肾高危组(CRHR),而TM6SF2 rs58542926 C>T则主要富集于代谢性肝病高危组(LHR)。
蛋白质组学分析进一步揭示了各亚型的生物学特征(图5):
LHR(代谢性肝病高危组)显著富集于代谢过程,尤其是小分子分解代谢、氨基酸代谢及细胞色素P450介导的外源物代谢;
CBHR(脑血管高危组)主要涉及代谢调控、血管重塑、神经活性配体-受体相互作用及松弛素信号通路;
ADHR(年龄相关风险组)以体液免疫、趋化因子信号及激素信号通路的富集为特征;
CRHR(代谢炎症-心肾高危组)富集于趋化作用、体液免疫应答及炎症通路。

图5. 不同亚组血浆蛋白质组学特征
综上所述,基于UK Biobank数据,利用临床生物标志物对CKM综合征进行分型,所识别的5个亚型(LR、LHR、CBHR、ADHR、CRHR)具备独特的血浆蛋白质组学特征与遗传风险模式,为识别高危CKM患者并开展靶向干预提供科学依据。此外,非肥胖且NCCR水平较高的个体CMM风险最低,提示在评估CMM风险时需要同时关注肌肉量和脂肪量。
五、结语
CKM综合征整合心血管、肾脏与代谢三大系统,为临床实践提供了更广阔的视野。王广教授团队从残余胆固醇、甲状腺激素敏感性到聚类分型,层层深入,为CKM早期识别与精准干预提供了重要依据。残余胆固醇是低成本、可干预的风险信号;甲状腺激素敏感性揭示了性别与年龄差异;聚类分型实现了从“分期”到“分型”的跨越。未来,随着多组学与人工智能的融入,CKM精准管理将更加可及,需多学科共同努力,为患者带来更长远的健康获益。
参考文献
[1] Ndumele CE, Neeland IJ, Tuttle KR et al. A Synopsis of the Evidence for the Science and Clinical Management of Cardiovascular-Kidney-Metabolic (CKM) Syndrome: A Scientific Statement From the American Heart Association. Circulation 2023; 148 (20): 1636-1664.
[2] Siddiqi TJ, Cherney D, Siddiqui HF et al. Effects of Sodium-Glucose Cotransporter-2 Inhibitors on Kidney Outcomes across Baseline Cardiovascular-Kidney-Metabolic Conditions: A Systematic Review and Meta-Analyses. J Am Soc Nephrol 2025; 36 (2): 242-255.
[3] Minhas AMK, Mathew RO, Sperling LS et al. Prevalence of the Cardiovascular-Kidney-Metabolic Syndrome in the United States. J Am Coll Cardiol 2024; 83 (18): 1824-1826.
[4] Kittelson KS, Junior AG, Fillmore N et al. Cardiovascular-kidney-metabolic syndrome - An integrative review. Prog Cardiovasc Dis 2024; 87: 26-36.
[5] Claudel SE, Verma A. Cardiovascular-kidney-metabolic syndrome: A step toward multidisciplinary and inclusive care. Cell Metab 2023; 35 (12): 2104-2106.
[6] Wang J, Sun Q, An Y et al. The association of remnant cholesterol (RC) and interaction between RC and diabetes on the subsequent risk of hypertension. Frontiers in Endocrinology 2022; Volume 13 - 2022.
[7] Sun H, Zhu W, Liu J et al. Reduced Sensitivity to Thyroid Hormones Is Associated With High Remnant Cholesterol Levels in Chinese Euthyroid Adults. The Journal of Clinical Endocrinology & Metabolism 2023; 108 (1): 166-174.
[8] Ding X, Tian J, Chang X et al. Association between remnant cholesterol and the risk of cardiovascular-kidney-metabolic syndrome progression: insights from the China health and retirement longitudinal study. European Journal of Preventive Cardiology 2025; 32 (13): 1157-1165.
[9] Ding X, Wang Y, Liu J et al. Impaired Sensitivity to Thyroid Hormones Is Associated With Elevated Homocysteine Levels in the Euthyroid Population. The Journal of Clinical Endocrinology & Metabolism 2022; 107 (9): e3731-e3737.
[10] Wei Y, Yang M, Liu J et al. Associations Between Sensitivity to Thyroid Hormones and Visceral Adiposity in Euthyroid Adults. J Clin Endocrinol Metab 2025; 110 (8): e2744-e2753.
[11] Zhou L, Jiang L, An Y et al. Association of Sensitivity to Thyroid Hormones and Non-Alcoholic Fatty Liver Disease and the Severity of Liver Fibrosis in Euthyroid Adults: A Retrospective Study. Diabetes, Metabolic Syndrome and Obesity: Targets and Therapy 2025; 18 (null): 479-490.
[12] Sun H, Zhou Y, Liu J et al. Maternal pre-pregnancy obesity modifies the association between first-trimester thyroid hormone sensitivity and gestational Diabetes Mellitus: a retrospective study from Northern China. Diabetol Metab Syndr 2023; 15 (1): 212.
[13] Jiang L, Zhou L, Liu J et al. Sex Differences in the Association Between Thyroid Hormone Sensitivity and Cardiovascular-Kidney-Metabolic Syndrome. J Clin Endocrinol Metab 2025; 110 (10): e3303-e3312.
[14] Yang M, Su C, Chang X et al. Data-driven cluster analysis identifies distinct types of cardiovascular-kidney-metabolic syndrome. European Journal of Preventive Cardiology 2025. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言