导语
时光回溯,五年回望。2021年4月27日,原研*司美格鲁肽注射液(诺和泰®)在中国正式获批用于2型糖尿病(T2DM)治疗。上市仅1年后,司美格鲁肽便荣获中国创新十大新药大奖。彼时,或许尚未有人充分预见,这一事件将对中国糖尿病管理产生何等深远的影响。
作为领域内的领先药物,司美格鲁肽在不断拓展新的治疗方向——从降糖到心血管保护,再到肾脏保护,接连取得一个又一个令人瞩目的新突破,成为截至目前#唯一同时拥有糖心肾三大适应症的胰高糖素样肽-1受体激动剂(GLP-1RA)。回顾其发展历程,司美格鲁肽的价值不仅在于提供了一种新型治疗手段,更在于它对传统糖尿病治疗理念的挑战与革新,以及其所体现的勇于探索、不断超越的科学精神。值此原研司美格鲁肽中国获批上市5周年之际,让我们一同梳理这些年来它所走过的值得铭记的足迹。
*本文涉及司美格鲁肽剂量为0.5 mg/1.0 mg
#截至2026年4月
铸就传奇:司美格鲁肽一路高歌,斩获糖心肾三大适应症
司美格鲁肽的故事始于降糖,却不止于降糖。美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)共同见证了这一过程。从2017年12月到2025年1月,FDA陆续批准了司美格鲁肽的糖心肾三大适应症。
鉴于充分的循证证据和明确的临床需求,NMPA加快了对司美格鲁肽的审批进程,仅用4年时间便在中国实现了糖心肾三大适应症的全面覆盖:
2021年4月,司美格鲁肽的降糖及心血管双适应症在中国获批,用于成人T2DM患者的血糖控制,以及降低伴有心血管疾病(CVD)的T2DM成人患者的主要心血管不良事件(MACE,心血管死亡、非致死性心肌梗死或非致死性卒中)风险。
2025年7月,NMPA新增批准其慢性肾脏病(CKD)适应症,用于降低伴有CKD的T2DM成人患者估算肾小球滤过率(eGFR)持续下降、终末期肾病和心血管死亡风险。
至此,司美格鲁肽成为中国首个同时具有降糖、心血管和肾脏三大适应症的GLP-1RA,实现了该类药物在适应症覆盖上的重要突破。
循证获益持续积累:司美格鲁肽重磅研究相继发布,构建完整证据体系
自2007年以来,司美格鲁肽先后开展了15项Ⅰ期临床试验和4项Ⅱ期临床试验。在明确其药代动力学/药效学(PK/PD)特征并确定用于T2DM患者的剂量方案后,2013年底启动了SUSTAIN系列Ⅲ期临床试验,覆盖广泛T2DM人群,夯实了司美格鲁肽的全面获益证据。与此同时,多项靶器官结局研究陆续开展,确证了司美格鲁肽的心肾获益;真实世界研究也进一步验证了其在临床实践中的综合价值,由此构建起完整的证据体系。
SUSTAIN系列研究:明确降糖疗效及综合代谢调控作用
SUSTAIN系列研究证实,司美格鲁肽可有效降低糖化血糖蛋白(HbA1c)水平,降幅最高达1.8%,显著优于多种对照药物。同时,该药可有效减轻体重、降低血压、全面改善血脂谱,展现出全面的综合代谢调控价值[1-11]。其中,SUSTAIN China研究证实,在中国T2DM人群中,二甲双胍基础上联合司美格鲁肽1.0 mg治疗30周,HbA1c显著降低达1.8%,HbA1c<7%的达标率高达86.1%,体重显著减轻4.2 kg,腰围显著缩小4.2 cm[10]。
心血管获益
SUSTAIN 6研究:确证心血管保护作用
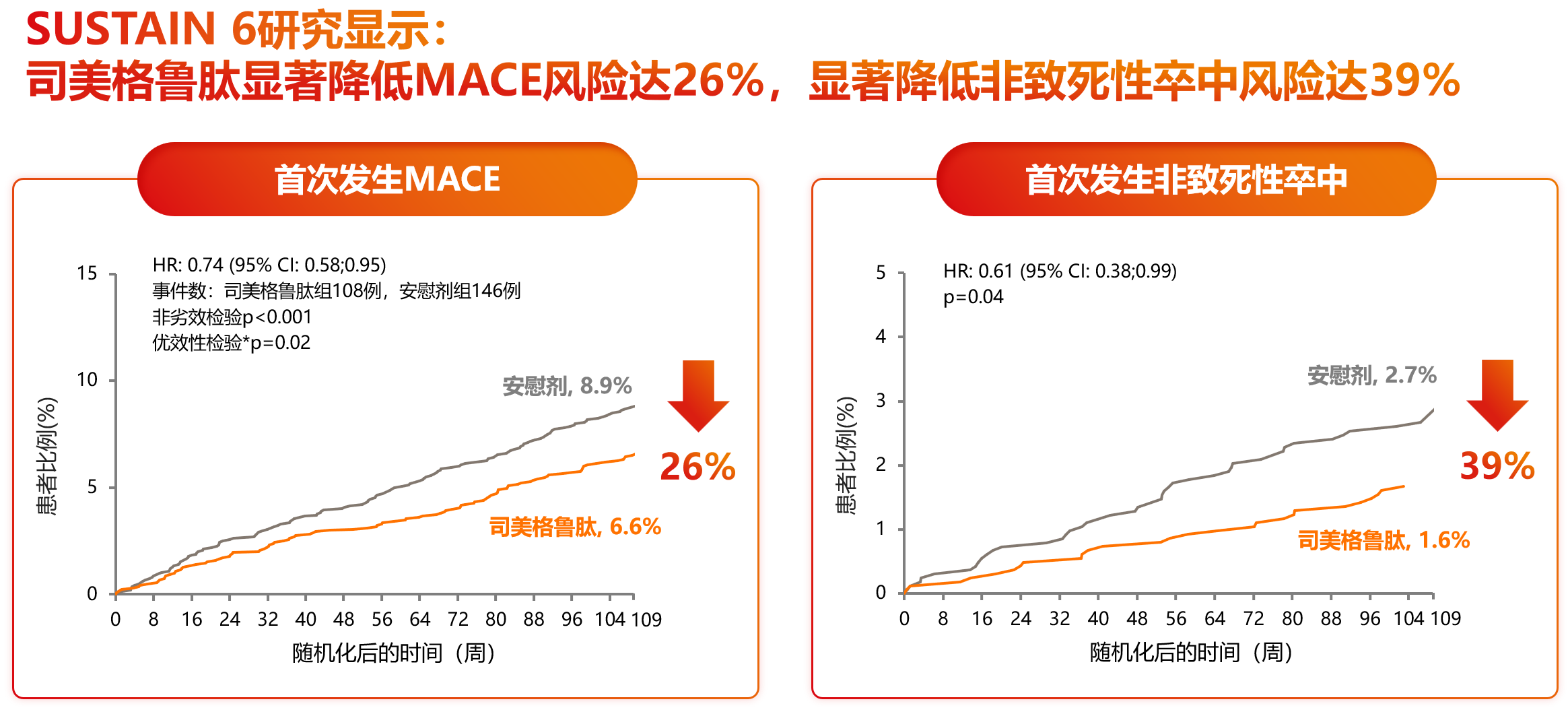
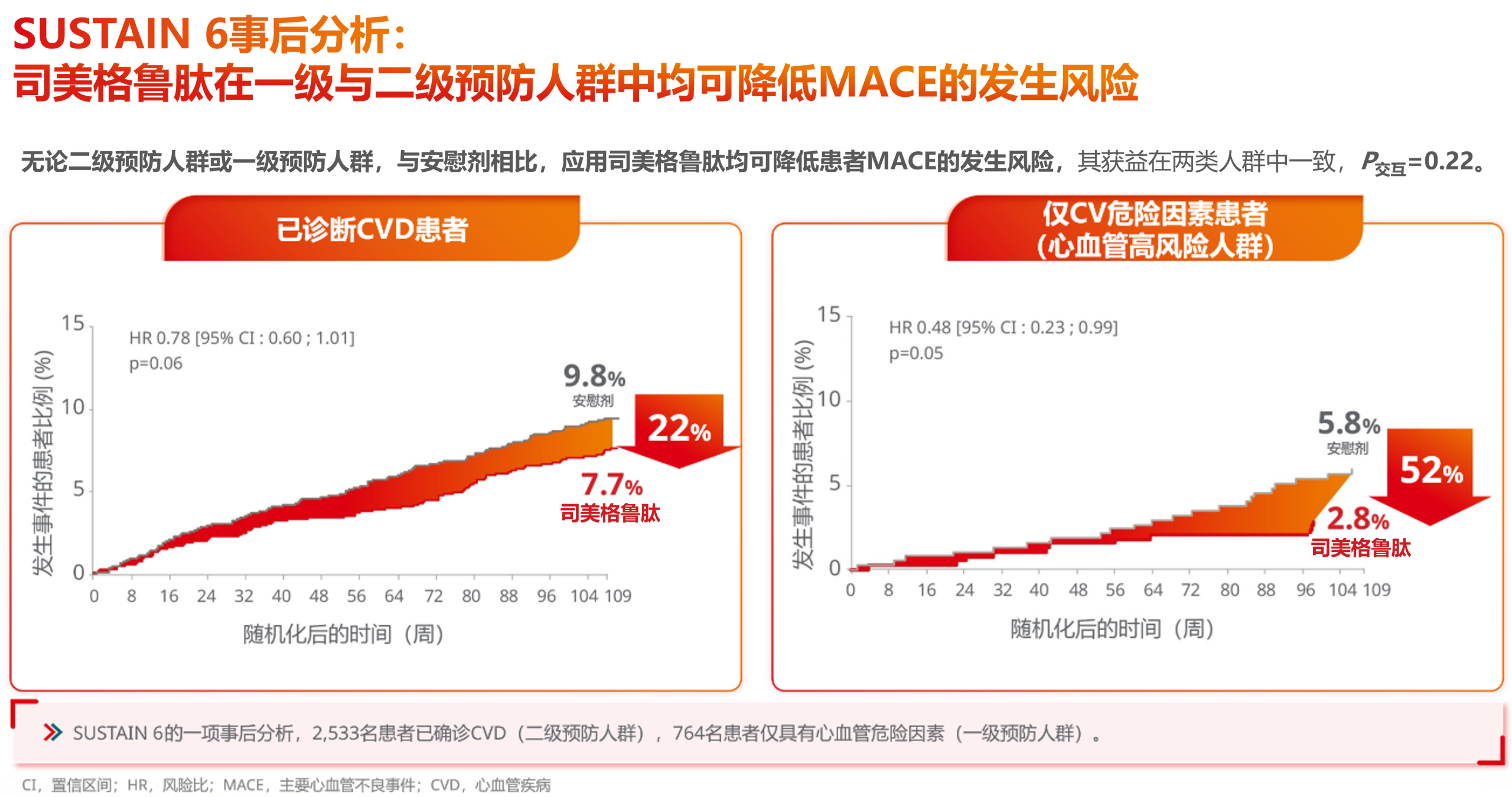
2016年,大型心血管结局试验(CVOT)SUSTAIN 6研究结果公布,为司美格鲁肽心血管适应症的获批提供了核心依据。结果证实,对于T2DM合并CVD或心血管高风险患者,司美格鲁肽可显著降低MACE风险达26%,显著降低非致死性卒中风险达39%[12]。而且,无论是已诊断CVD的二级预防人群,还是心血管高风险(仅合并高血压、高血脂等危险因素但尚未发病)的一级预防人群,司美格鲁肽均可显著降低MACE发生风险,其获益在两类人群中一致(P交互=0.22)[13]。而在替尔泊肽的CVOT研究SURPASS-CVOT中,纳入的受试者均为合并CVD的T2DM患者,在MACE风险降低方面达到非劣效[14]。
值得注意的是,司美格鲁肽的心血管获益独立于其降糖作用,也不受基线体重指数(BMI)和体重变化的影响[15]。这不仅支持其心血管获益具有普适性,也强烈提示其心血管保护主要源自药物本身的直接效应。
肾脏获益
FLOW研究:实现里程碑突破,首次证实GLP-1RA的肾脏硬终点获益
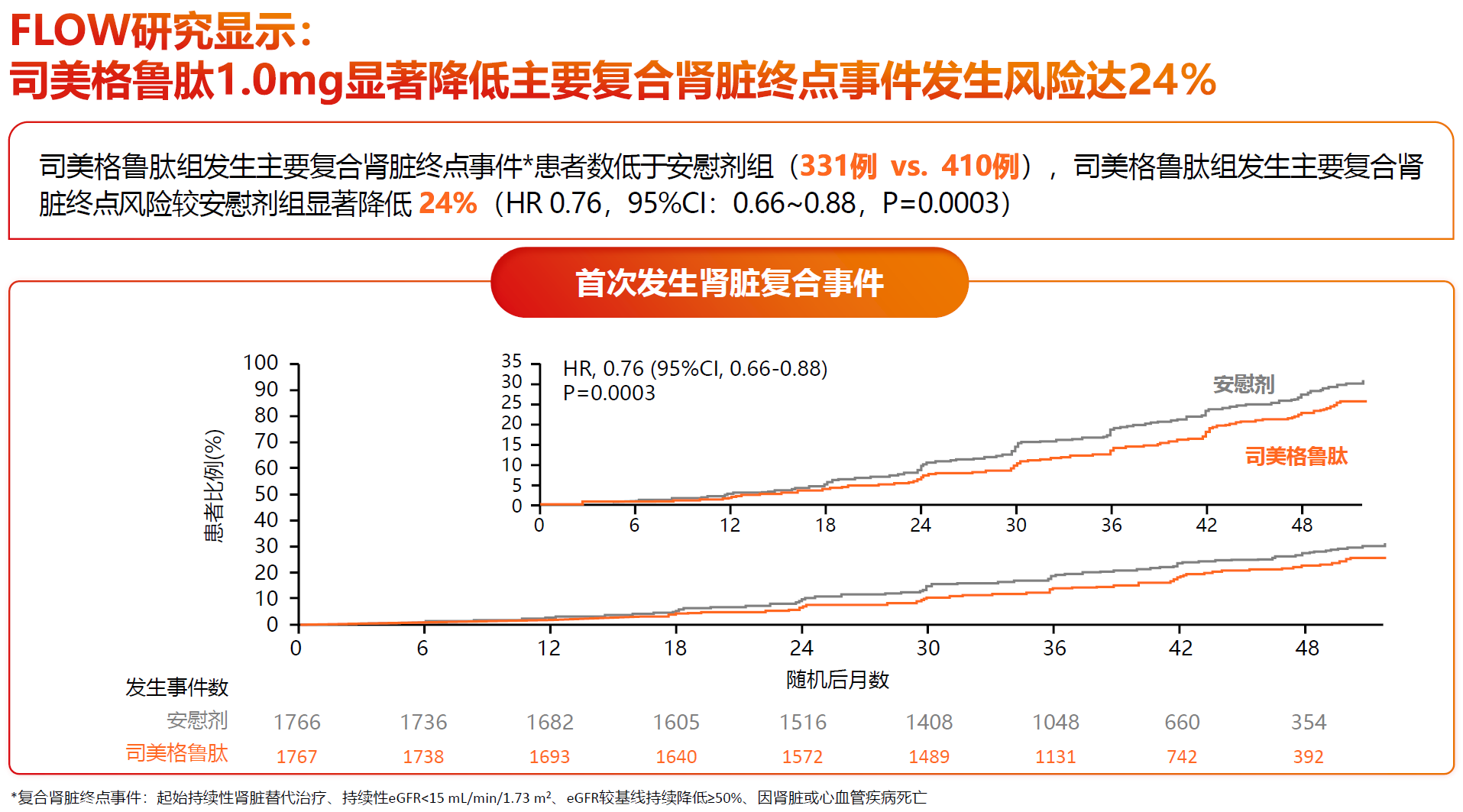
2024年,司美格鲁肽的大型肾脏结局试验(KOT)——FLOW研究结果重磅公布,这是肠促胰素类药物的目前*唯一一项KOT,取得了里程碑式突破。结果证实,在T2DM合并CKD患者中,司美格鲁肽1.0 mg显著降低肾脏复合事件风险达24%,显著降低尿白蛋白肌酐比值(UACR)达40%,并明显延缓肾功能下降;同时,显著降低MACE风险18%,并降低全因死亡风险20%[16]。FLOW研究是司美格鲁肽新增CKD适应症的核心驱动力,随着司美格鲁肽的加入,T2DM合并CKD治疗形成了四大支柱的新格局。司美格鲁肽也因此成为中国首个同时具有降糖、心血管保护及肾脏保护三大适应症的肠促胰素类药物。
*截至2026年4月
外周动脉疾病获益
STRIDE研究:拓展心血管获益新边界
2025年,首项评估降糖药物对T2DM合并症状性外周动脉疾病(PAD)患者功能结局影响的随机对照研究——STRIDE研究结果公布,揭示了司美格鲁肽1.0 mg改善这类人群功能结局的明确证据,使其成为目前首个能显著改善PAD患者运动功能的降糖药物[17]。结果证实,司美格鲁肽1.0 mg显著改善最大步行距离达13%,平均增加40米,达到主要终点。其他次要终点也有显著改善,包括无痛步行距离、血管生活质量(VascuQoL-6)评分、踝肱指数(ABI)等。STRIDE研究意义重大,进一步拓宽了司美格鲁肽从“中心”到“外周”的血管保护证据链。

指南认证一线地位:以心肾结局为导向,司美格鲁肽是优选降糖药
近年来,T2DM管理理念发生重大变更,从单纯追求血糖达标,转向以心肾结局为导向,强调根据药物的心肾保护获益及患者合并症特征来选择降糖药物,而非仅基于降糖效果。随着循证医学证据的不断积累,以司美格鲁肽为代表的GLP-1RA因具有明确的心肾获益,受到最新国内外权威指南的一致认可与推荐,被提升至一线治疗地位[20,21]。根据2024版中国糖尿病防治指南和2026版ADA指南,司美格鲁肽在T2DM管理中的一线治疗适用人群包括:合并ASCVD或其高风险、合并CKD,或合并超重/肥胖的T2DM患者[20,21]。
除了作为上述人群的起始治疗优先选择外,司美格鲁肽的临床应用还贯穿于T2DM的核心治疗路径,包括在口服降糖药疗效不佳时作为注射治疗的优选方案之一,以及作为胰岛素起始治疗前应优先考虑的关键选择,从而满足处于不同疾病阶段的患者治疗需求。
结语:循证引领时代,持续铸牢T2DM全方位管理防线
回首来时路,郁郁满芳华。原研司美格鲁肽在全球上市9年、中国上市5年以来,积累了丰富而坚实的循证医学证据,获得了T2DM、CVD及CKD三大适应症。目前*在肠促胰素类药物(包括GIP/GLP-1双受体激动剂)中,司美格鲁肽的糖心肾全面获益证据无出其右,树立领域标杆。此外,相较于仿制药,原研司美格鲁肽具备多重优势,不仅在生物药的发酵工艺、纯化技术、佐剂配方、杂质谱控制能力等方面具有明显技术优势,而且拥有高度领先的递送系统(预填充注射笔),给患者带来更佳的注射感受。
展望未来,原研司美格鲁肽将持续助力糖心肾全方位健康管理防线的构建,为改善中国T2DM患者的长期预后、守护患者健康贡献更多力量。
*截至2026年4月
参考文献
1. Sorli C, et al. Lancet Diabetes Endocrinol. 2017; 5(4): 251-260.
2. Ahrén B, et al. Lancet Diabetes Endocrinol. 2017; 5(5): 341-354.
3. Ahmann AJ, et al. Diabetes Care. 2018; 41(2): 258-266.
4. Aroda VR, et al. Lancet Diabetes Endocrinol. 2017; 5(5): 355-366.
5. Rodbard HW, et al. J Clin Endocrinol Metab. 2018; 103(6): 2291-2301.
6. Pratley RE, et al. Lancet Diabetes Endocrinol. 2018; 6(4): 275-286.
7. Lingvay I, et al. Lancet Diabetes Endocrinol. 2019; 7(11): 834-844.
8. Capehorn MS, et al. Diabetes Metab. 2020; 46(2): 100-109.
9. Zinman B, et al. Lancet Diabetes Endocrinol. 2019; 7(5): 356-367.
10. Ji L, et al. Diabetes Obes Metab. 2021; 23(2): 404-414.
11. Kellerer M, et al. Diabetes Obes Metab. 2022; 24(9): 1788-1799.
12. Marso SP, et al. N Engl J Med. 2016; 375(19): 1834-1844.
13. Leiter LA, et al. Cardiovasc Diabetol. 2019; 18(1): 73.
14. Nicholls SJ, et al. N Engl J Med. 2025; 393(24): 2409-2420.
15. Zhou J, et al. Diabetes Obes Metab. 2025; 27(10): 5706-5715.
16. Perkovic V, et al. N Engl J Med. 2024; 391(2): 109-121.
17. Bonaca MP, et al. Lancet. 2025; 405(10489): 1580-1593.
18. Holmes P, et al. Diabetes Ther. 2021; 12(11): 2891-2905.
19. Tan X, et al. Comparative effectiveness of once-weekly semaglutide vs dulaglutide on cardiovascular outcomes in US Medicare beneficiaries with type 2 diabetes and atherosclerotic cardiovascular disease. Presented at EASD2025 meeting. LBA 19.
20. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
21. American Diabetes Association. Diabetes Care. 2026; 49(Suppl. 1): S1-S371. 2 comments
时光回溯,五年回望。2021年4月27日,原研*司美格鲁肽注射液(诺和泰®)在中国正式获批用于2型糖尿病(T2DM)治疗。上市仅1年后,司美格鲁肽便荣获中国创新十大新药大奖。彼时,或许尚未有人充分预见,这一事件将对中国糖尿病管理产生何等深远的影响。
作为领域内的领先药物,司美格鲁肽在不断拓展新的治疗方向——从降糖到心血管保护,再到肾脏保护,接连取得一个又一个令人瞩目的新突破,成为截至目前#唯一同时拥有糖心肾三大适应症的胰高糖素样肽-1受体激动剂(GLP-1RA)。回顾其发展历程,司美格鲁肽的价值不仅在于提供了一种新型治疗手段,更在于它对传统糖尿病治疗理念的挑战与革新,以及其所体现的勇于探索、不断超越的科学精神。值此原研司美格鲁肽中国获批上市5周年之际,让我们一同梳理这些年来它所走过的值得铭记的足迹。
*本文涉及司美格鲁肽剂量为0.5 mg/1.0 mg
#截至2026年4月
铸就传奇:司美格鲁肽一路高歌,斩获糖心肾三大适应症
司美格鲁肽的故事始于降糖,却不止于降糖。美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)共同见证了这一过程。从2017年12月到2025年1月,FDA陆续批准了司美格鲁肽的糖心肾三大适应症。
鉴于充分的循证证据和明确的临床需求,NMPA加快了对司美格鲁肽的审批进程,仅用4年时间便在中国实现了糖心肾三大适应症的全面覆盖:
2021年4月,司美格鲁肽的降糖及心血管双适应症在中国获批,用于成人T2DM患者的血糖控制,以及降低伴有心血管疾病(CVD)的T2DM成人患者的主要心血管不良事件(MACE,心血管死亡、非致死性心肌梗死或非致死性卒中)风险。
2025年7月,NMPA新增批准其慢性肾脏病(CKD)适应症,用于降低伴有CKD的T2DM成人患者估算肾小球滤过率(eGFR)持续下降、终末期肾病和心血管死亡风险。
至此,司美格鲁肽成为中国首个同时具有降糖、心血管和肾脏三大适应症的GLP-1RA,实现了该类药物在适应症覆盖上的重要突破。
循证获益持续积累:司美格鲁肽重磅研究相继发布,构建完整证据体系
自2007年以来,司美格鲁肽先后开展了15项Ⅰ期临床试验和4项Ⅱ期临床试验。在明确其药代动力学/药效学(PK/PD)特征并确定用于T2DM患者的剂量方案后,2013年底启动了SUSTAIN系列Ⅲ期临床试验,覆盖广泛T2DM人群,夯实了司美格鲁肽的全面获益证据。与此同时,多项靶器官结局研究陆续开展,确证了司美格鲁肽的心肾获益;真实世界研究也进一步验证了其在临床实践中的综合价值,由此构建起完整的证据体系。

SUSTAIN系列研究:明确降糖疗效及综合代谢调控作用
SUSTAIN系列研究证实,司美格鲁肽可有效降低糖化血糖蛋白(HbA1c)水平,降幅最高达1.8%,显著优于多种对照药物。同时,该药可有效减轻体重、降低血压、全面改善血脂谱,展现出全面的综合代谢调控价值[1-11]。其中,SUSTAIN China研究证实,在中国T2DM人群中,二甲双胍基础上联合司美格鲁肽1.0 mg治疗30周,HbA1c显著降低达1.8%,HbA1c<7%的达标率高达86.1%,体重显著减轻4.2 kg,腰围显著缩小4.2 cm[10]。
心血管获益
SUSTAIN 6研究:确证心血管保护作用
2016年,大型心血管结局试验(CVOT)SUSTAIN 6研究结果公布,为司美格鲁肽心血管适应症的获批提供了核心依据。结果证实,对于T2DM合并CVD或心血管高风险患者,司美格鲁肽可显著降低MACE风险达26%,显著降低非致死性卒中风险达39%[12]。而且,无论是已诊断CVD的二级预防人群,还是心血管高风险(仅合并高血压、高血脂等危险因素但尚未发病)的一级预防人群,司美格鲁肽均可显著降低MACE发生风险,其获益在两类人群中一致(P交互=0.22)[13]。而在替尔泊肽的CVOT研究SURPASS-CVOT中,纳入的受试者均为合并CVD的T2DM患者,在MACE风险降低方面达到非劣效[14]。
值得注意的是,司美格鲁肽的心血管获益独立于其降糖作用,也不受基线体重指数(BMI)和体重变化的影响[15]。这不仅支持其心血管获益具有普适性,也强烈提示其心血管保护主要源自药物本身的直接效应。
肾脏获益
FLOW研究:实现里程碑突破,首次证实GLP-1RA的肾脏硬终点获益
2024年,司美格鲁肽的大型肾脏结局试验(KOT)——FLOW研究结果重磅公布,这是肠促胰素类药物的目前*唯一一项KOT,取得了里程碑式突破。结果证实,在T2DM合并CKD患者中,司美格鲁肽1.0 mg显著降低肾脏复合事件风险达24%,显著降低尿白蛋白肌酐比值(UACR)达40%,并明显延缓肾功能下降;同时,显著降低MACE风险18%,并降低全因死亡风险20%[16]。FLOW研究是司美格鲁肽新增CKD适应症的核心驱动力,随着司美格鲁肽的加入,T2DM合并CKD治疗形成了四大支柱的新格局。司美格鲁肽也因此成为中国首个同时具有降糖、心血管保护及肾脏保护三大适应症的肠促胰素类药物。
*截至2026年4月

外周动脉疾病获益
STRIDE研究:拓展心血管获益新边界
2025年,首项评估降糖药物对T2DM合并症状性外周动脉疾病(PAD)患者功能结局影响的随机对照研究——STRIDE研究结果公布,揭示了司美格鲁肽1.0 mg改善这类人群功能结局的明确证据,使其成为目前首个能显著改善PAD患者运动功能的降糖药物[17]。结果证实,司美格鲁肽1.0 mg显著改善最大步行距离达13%,平均增加40米,达到主要终点。其他次要终点也有显著改善,包括无痛步行距离、血管生活质量(VascuQoL-6)评分、踝肱指数(ABI)等。STRIDE研究意义重大,进一步拓宽了司美格鲁肽从“中心”到“外周”的血管保护证据链。

真实世界证据持续验证多重获益
指南认证一线地位:以心肾结局为导向,司美格鲁肽是优选降糖药
近年来,T2DM管理理念发生重大变更,从单纯追求血糖达标,转向以心肾结局为导向,强调根据药物的心肾保护获益及患者合并症特征来选择降糖药物,而非仅基于降糖效果。随着循证医学证据的不断积累,以司美格鲁肽为代表的GLP-1RA因具有明确的心肾获益,受到最新国内外权威指南的一致认可与推荐,被提升至一线治疗地位[20,21]。根据2024版中国糖尿病防治指南和2026版ADA指南,司美格鲁肽在T2DM管理中的一线治疗适用人群包括:合并ASCVD或其高风险、合并CKD,或合并超重/肥胖的T2DM患者[20,21]。
除了作为上述人群的起始治疗优先选择外,司美格鲁肽的临床应用还贯穿于T2DM的核心治疗路径,包括在口服降糖药疗效不佳时作为注射治疗的优选方案之一,以及作为胰岛素起始治疗前应优先考虑的关键选择,从而满足处于不同疾病阶段的患者治疗需求。
结语:循证引领时代,持续铸牢T2DM全方位管理防线
回首来时路,郁郁满芳华。原研司美格鲁肽在全球上市9年、中国上市5年以来,积累了丰富而坚实的循证医学证据,获得了T2DM、CVD及CKD三大适应症。目前*在肠促胰素类药物(包括GIP/GLP-1双受体激动剂)中,司美格鲁肽的糖心肾全面获益证据无出其右,树立领域标杆。此外,相较于仿制药,原研司美格鲁肽具备多重优势,不仅在生物药的发酵工艺、纯化技术、佐剂配方、杂质谱控制能力等方面具有明显技术优势,而且拥有高度领先的递送系统(预填充注射笔),给患者带来更佳的注射感受。
展望未来,原研司美格鲁肽将持续助力糖心肾全方位健康管理防线的构建,为改善中国T2DM患者的长期预后、守护患者健康贡献更多力量。
*截至2026年4月
参考文献
1. Sorli C, et al. Lancet Diabetes Endocrinol. 2017; 5(4): 251-260.
2. Ahrén B, et al. Lancet Diabetes Endocrinol. 2017; 5(5): 341-354.
3. Ahmann AJ, et al. Diabetes Care. 2018; 41(2): 258-266.
4. Aroda VR, et al. Lancet Diabetes Endocrinol. 2017; 5(5): 355-366.
5. Rodbard HW, et al. J Clin Endocrinol Metab. 2018; 103(6): 2291-2301.
6. Pratley RE, et al. Lancet Diabetes Endocrinol. 2018; 6(4): 275-286.
7. Lingvay I, et al. Lancet Diabetes Endocrinol. 2019; 7(11): 834-844.
8. Capehorn MS, et al. Diabetes Metab. 2020; 46(2): 100-109.
9. Zinman B, et al. Lancet Diabetes Endocrinol. 2019; 7(5): 356-367.
10. Ji L, et al. Diabetes Obes Metab. 2021; 23(2): 404-414.
11. Kellerer M, et al. Diabetes Obes Metab. 2022; 24(9): 1788-1799.
12. Marso SP, et al. N Engl J Med. 2016; 375(19): 1834-1844.
13. Leiter LA, et al. Cardiovasc Diabetol. 2019; 18(1): 73.
14. Nicholls SJ, et al. N Engl J Med. 2025; 393(24): 2409-2420.
15. Zhou J, et al. Diabetes Obes Metab. 2025; 27(10): 5706-5715.
16. Perkovic V, et al. N Engl J Med. 2024; 391(2): 109-121.
17. Bonaca MP, et al. Lancet. 2025; 405(10489): 1580-1593.
18. Holmes P, et al. Diabetes Ther. 2021; 12(11): 2891-2905.
19. Tan X, et al. Comparative effectiveness of once-weekly semaglutide vs dulaglutide on cardiovascular outcomes in US Medicare beneficiaries with type 2 diabetes and atherosclerotic cardiovascular disease. Presented at EASD2025 meeting. LBA 19.
20. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
21. American Diabetes Association. Diabetes Care. 2026; 49(Suppl. 1): S1-S371. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言