编者按
在澳大利亚,慢性肾脏病(CKD)的患病情况呈现出严峻的种族差异与高死亡率特征。数据显示,每8名土著居民中就有1人受此病困扰,其死亡率更是高达非原住民的3倍。放眼全球,心血管疾病已取代其他并发症,成为晚期肾病患者死亡的首要原因,占比高达40%~50%。面对这一复杂的公共卫生挑战,传统的单一学科诊疗模式已显得力不从心。近日,一场由肾脏科、心内科、内分泌科及全科医学领域8位顶尖专家共同参与的学术行动,为CKD管理带来了全新的“澳大利亚方案”。这份划时代的专家共识,旨在打破学科壁垒,重塑治疗路径。今天,我们将深度解读这份重磅指南,剖析其如何通过多学科协作,重新定义慢性肾病的治疗标准。
肾脏不是孤岛!
慢性肾病如何引爆全身“多米诺骨牌”
CKD不仅是肾功能逐渐恶化的局部疾病,更是一场波及全身的系统性危机。肾脏、心血管与代谢系统间的病理生理相互作用,导致多种合并症共存,使得晚期患者的心血管死亡率高达40%-50%(远超正常人群的26%)。因此,整合多学科资源、统筹管理合并症已成为改善预后的关键。
在澳大利亚,CKD已成为严峻的公共卫生负担。截至2021年,超200万人患病,造成约5.6万残疾调整生命年损失,占当年全国死亡总数的11%,并带来每年99亿美元的经济损失。尤为痛心的是健康不平等现象:土著和托雷斯海峡岛民群体的CKD患病率是非原住民的8倍,住院率和致死率更是分别高出8倍和3倍。
尽管过去十年间,针对糖尿病肾病(DKD)及特定肾病的新型药物(如内皮素受体拮抗剂等)取得了显著突破,但现有的管理指南仍存局限:国际指南(如KDIGO)缺乏本土适应性;旧版《CARI指南》已滞后;而初级保健手册则难以覆盖各级医疗服务的协同需求。
为填补这一空白,澳大利亚召集了涵盖肾脏科、心内科、内分泌科及全科医学的多学科专家团队。旨在制定一套简单、切实可行、基于证据且完全契合澳大利亚国情的共识建议,以优化医疗资源配置,缩小健康差距,并最终改善患者的治疗效果。
共识推荐:
从筛查监测到综合管理的临床实践路径
为确保指南的科学性与临床实用性,我们汇聚了来自澳大利亚各地的8位顶尖专家,组建了涵盖肾脏科、心内科、内分泌科及全科医学的多学科团队,以全面应对慢性肾病(CKD)复杂的合并症管理需求。研究采用改良版虚拟名义组技术:专家们首先依据GRADE标准独立提交建议,经去重整理后,在Microsoft Teams虚拟会议中进行深度阐述与辩论,并通过1-5分制进行匿名评分。最终,严格遵循国际共识程序,仅将支持率超过75%(平均分≥3.5)的建议纳入指南,确保每一条推荐都经得起推敲,真正服务于澳大利亚的临床实践。作者组初拟21条建议,经整合去重形成9项独立推荐。其中5项达成共识(支持率>75%)(表1),另有1项因不符合GRADE标准被剔除。
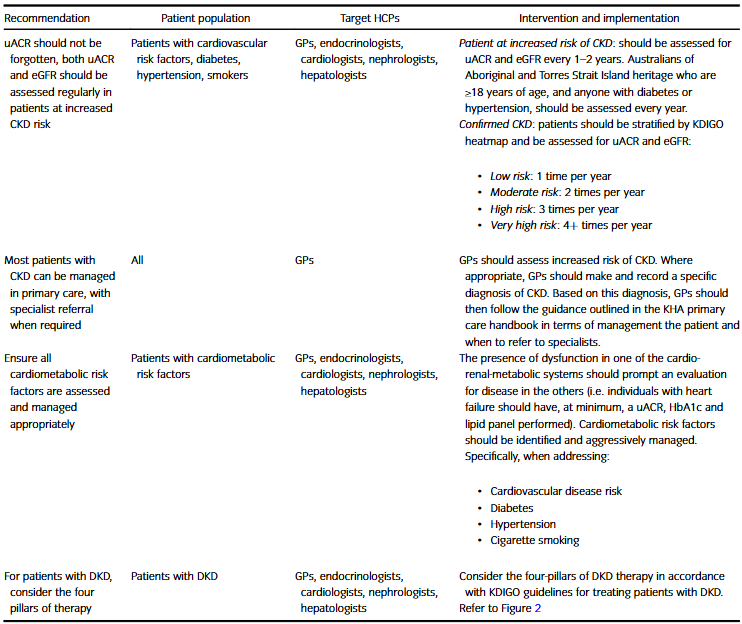
表1. 澳大利亚针对HCP提升慢性肾病患者护理标准的建议
推荐1:对于慢性肾病高危患者,应定期评估尿白蛋白/肌酐比值(uACR)与估算肾小球滤过率(eGFR)
慢性肾病(CKD)因其极强的隐匿性被称为“沉默的杀手”,患者在出现明显症状之前,肾功能可能已经丧失了高达90%。因此,在症状显现之前进行早期识别与干预至关重要,及时的发现与管理甚至可以将疾病进展的风险降低50%。
目前的筛查策略主要依赖三大核心指标:血压(BP)、uACR及eGFR。
eGFR是评估肾功能的关键指标,澳大利亚病理实验室通常依据≥18岁患者的血清肌酐,通过CKD-EPI预测方程自动计算并报告该数值。尽管该方程已在多种人群中得到验证,但在老年人或肌肉量异常者中可能存在偏差,此时若条件允许,可联合检测半胱氨酸蛋白酶抑制剂C以提高准确性;
uACR被视为肾损伤的敏感标志物,其数值升高预示着肾脏及心血管风险的增加,但在实际临床检查中常被低估。
在临床实践中,应根据患者情况制定个性化的筛查计划。
对于心血管疾病(或家族史)、年龄>50岁、肥胖、糖尿病、高血压及吸烟等CKD高危人群,建议每1~2年测量一次eGFR和uACR;
对于≥18岁的澳大利亚原住民和托雷斯海峡岛民,鉴于其较高的患病风险,建议将筛查频率提高至每年一次
对于已经确诊的CKD患者,则应严格依据KDIGO CKD热图进行风险分层监测(图1):低风险患者每年监测1次,中等风险每年2次,高风险每年3次,而极高风险患者则需要每年进行4次及以上的监测。
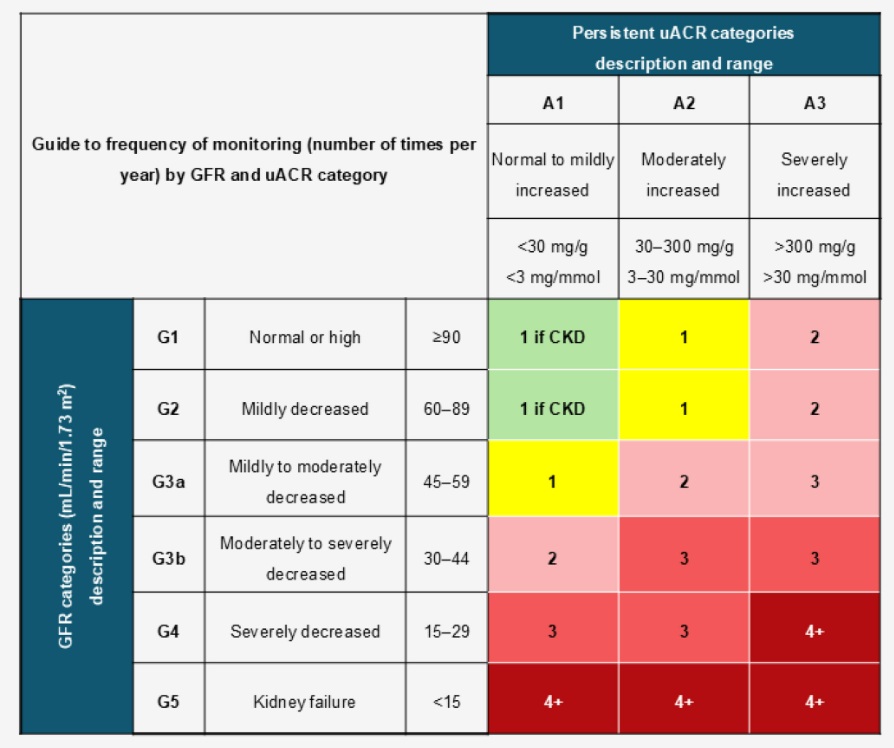
图1. eGFR和uACR热图显示患者每年推荐的评估频率。绿色表示低风险,黄色表示风险增加,粉色表示中等风险,红色表示高风险,深红色表示极高风险。
推荐2:大多数CKD患者均可在初级医疗中接受管理,必要时进行转诊
鉴于CKD巨大的公共卫生负担,其管理不应局限于专科。初级保健从业者(如全科医生、护士、药剂师)处于早期发现与干预的第一线,这不仅能为患者争取改变生活方式、延缓疾病进展及降低心血管风险的时间,更具有显著的经济效益——模型显示,每投入1美元进行早期干预,可节省45美元的肾衰竭及相关治疗费用。尽管2020年启动的《国家肾病战略行动计划》已将早期发现列为关键目标,但目前初级保健中仍有超过90%的3期CKD病例未被确诊。因此,提升初级保健医生的诊断与管理能力,并在必要时精准转诊,已成为当务之急。
初级保健从业者应依据推荐1对高危人群进行评估。确诊后,需明确CKD分期(1~5期)及白蛋白尿分级,并遵循KHA慢性肾病手册实施管理计划,但要注意的是,如果患者出现以下情况应及时转诊至肾脏专科:
肾功能急剧恶化:3个月内eGFR下降>15%,或12个月内持续下降≥25%,或eGFR降至<30 ml/min/1.73 m2(甚至<15 ml/min/1.73 m2);
临床表现复杂:出现急性肾炎症状(如少尿、血尿、水肿)、难治性高血压(≥3种药物控制不佳)或持续性重度白蛋白尿(uACR≥30 mg/mmol)。
特殊人群:包括青少年、有家族史者及原住民和托雷斯海峡岛民。
关于转诊决策,可使用肾衰竭风险方程(KFRE)等肾衰竭风险预测工具辅助判断。
推荐3:适当评估和管理心脏代谢风险因素
肾脏、心肺与内分泌系统紧密关联,致使高血压、糖尿病、血脂异常、心力衰竭及吸烟等传统心血管代谢风险因素在慢性肾病患者中极为普遍,并显著加速疾病进展及不良结局。肥胖虽为心脏代谢风险的上游驱动因素,但其过量脂肪组织亦独立关联于肾脏血流动力学及结构性异常。因此,识别并管理肥胖及相关心血管代谢风险因素是慢性肾病管理的核心。KDIGO-CARI指南为脂质管理提供了全面建议,综合风险因素管理已被证实能减少心血管事件并延缓慢性肾病进展。
心-肾-代谢系统中任一系统患病,均应引发对其他系统的评估(如心力衰竭患者应检测尿白蛋白/肌酐比值、糖化血红蛋白及血脂):
心血管疾病风险:当eGFR<45 ml/min/1.73 m2,无需正式风险评估,应直接启动降脂、降压治疗;若eGFR 45~59 ml/min/1.73 m2伴微量白蛋白尿,则视为风险增强因素,应将患者重新归类至更高风险层级;对于无临床动脉粥样硬化性心血管疾病的患者,低密度脂蛋白胆固醇控制目标应至少<1.8 mmol/L。
糖尿病:糖化血红蛋白(HbA1c)目标值应在6.5%至8%之间,并依据估算肾小球滤过率、患者偏好及合并症特征进行个体化调整。
高血压:血压测量应采用标准化技术,并结合门诊与家庭血压监测;对于非透析患者,若可耐受,血压控制目标应为低于130/80 mmHg。
吸烟:戒烟已被证实能减缓慢性肾病进展,应作为优先事项;尽管尼古丁替代疗法及辅助药物治疗尚未在慢性肾病患者中专门研究,但预期获益与其他人群相当,通常推荐使用。
推荐4:对于患有DKD的患者,巧用四大支柱
针对心血管代谢风险因素的管理虽是慢性肾病治疗的核心,但药理学领域的突破已为临床提供了更丰富的工具,特别是在糖尿病肾病管理方面,目前已形成了针对四种不同病理机制的“四支柱”疗法(图2)。
第一支柱为肾素-血管紧张素系统抑制剂(RASi),包括血管紧张素转换酶抑制剂(ACEi)或血管紧张素II受体阻滞剂(ARB),通过降低肾小球内压和血压,长期数据显示其能有效减缓白蛋白尿及疾病进展。
第二支柱是钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i),通过抑制近端小管对钠和葡萄糖的重吸收,恢复管球反馈,减少高滤过状态,除降糖外,还能显著降低心血管风险及预防心力衰竭。
第三支柱是非甾体盐皮质激素受体拮抗剂(ns-MRA),主要针对2型糖尿病(T2DM)合并CKD,旨在纠正醛固酮失调,尽管在1型糖尿病(T1DM)及非糖尿病肾病中的证据尚在积累中。
第四支柱为胰高血糖素样肽-1受体激动剂(GLP-1RA),在降糖和减重的同时改善心血管代谢结局,最新研究证实其能降低疾病进展或心脏死亡风险,这种获益被认为与减少氧化应激、炎症及纤维化有关。
鉴于糖尿病肾病的复杂性,虽然最佳给药顺序或联合方案尚未完全定论,但精算分析提示SGLT2i、ns-MRA和GLP-1RA的联合使用可能提升无事件生存率。因此,共识建议:
对于非糖尿病CKD患者,目前应将应将循证疗法如RASi和SGLT2i视为基础治疗作为基础治疗。
对于合并高血压及白蛋白尿的患者,应启动ACEi或ARB(RASi)治疗,并将剂量滴定至患者可耐受的最高批准剂量。
对于已接受其他降糖药物治疗的T2DM合并CKD患者,若eGFR≥20 ml/min/1.73 m2,建议在现有治疗方案中加用SGLT2i。
对于T2DM患者,若eGFR≥25 ml/min/1.73 m2、血清钾浓度正常,且在RASi最大耐受剂量下仍存在白蛋白尿(≥30 mg/g,即≥3 mg/mmol),可在RASi和SGLT2i基础上加用nsMRA。
对于使用二甲双胍和SGLT2i治疗后仍未达到个体化血糖控制目标,或无法使用上述药物的T2D合并CKD患者,推荐使用GLP-1RA。
结语
澳大利亚慢性肾病负担的日益加重,凸显了制定标准化、循证管理策略的迫切需求——这些策略需整合多学科护理模式并充分利用新兴疗法。为应对这一挑战,本共识建议提供了一个可操作的框架,该框架针对澳大利亚独特的医疗环境量身定制,优先保障医疗公平、以患者为中心的护理以及对合并症的积极管理。通过实施这些策略,临床医生能够改善患者预后,减少CKD相关并发症,并帮助缓解CKD对个人和医疗系统造成的社会经济压力。
参考文献
Schlaich MP, et al. Intern Med J. 2026 Mar 18. 2 comments
在澳大利亚,慢性肾脏病(CKD)的患病情况呈现出严峻的种族差异与高死亡率特征。数据显示,每8名土著居民中就有1人受此病困扰,其死亡率更是高达非原住民的3倍。放眼全球,心血管疾病已取代其他并发症,成为晚期肾病患者死亡的首要原因,占比高达40%~50%。面对这一复杂的公共卫生挑战,传统的单一学科诊疗模式已显得力不从心。近日,一场由肾脏科、心内科、内分泌科及全科医学领域8位顶尖专家共同参与的学术行动,为CKD管理带来了全新的“澳大利亚方案”。这份划时代的专家共识,旨在打破学科壁垒,重塑治疗路径。今天,我们将深度解读这份重磅指南,剖析其如何通过多学科协作,重新定义慢性肾病的治疗标准。
肾脏不是孤岛!
慢性肾病如何引爆全身“多米诺骨牌”
CKD不仅是肾功能逐渐恶化的局部疾病,更是一场波及全身的系统性危机。肾脏、心血管与代谢系统间的病理生理相互作用,导致多种合并症共存,使得晚期患者的心血管死亡率高达40%-50%(远超正常人群的26%)。因此,整合多学科资源、统筹管理合并症已成为改善预后的关键。
在澳大利亚,CKD已成为严峻的公共卫生负担。截至2021年,超200万人患病,造成约5.6万残疾调整生命年损失,占当年全国死亡总数的11%,并带来每年99亿美元的经济损失。尤为痛心的是健康不平等现象:土著和托雷斯海峡岛民群体的CKD患病率是非原住民的8倍,住院率和致死率更是分别高出8倍和3倍。
尽管过去十年间,针对糖尿病肾病(DKD)及特定肾病的新型药物(如内皮素受体拮抗剂等)取得了显著突破,但现有的管理指南仍存局限:国际指南(如KDIGO)缺乏本土适应性;旧版《CARI指南》已滞后;而初级保健手册则难以覆盖各级医疗服务的协同需求。
为填补这一空白,澳大利亚召集了涵盖肾脏科、心内科、内分泌科及全科医学的多学科专家团队。旨在制定一套简单、切实可行、基于证据且完全契合澳大利亚国情的共识建议,以优化医疗资源配置,缩小健康差距,并最终改善患者的治疗效果。
共识推荐:
从筛查监测到综合管理的临床实践路径
为确保指南的科学性与临床实用性,我们汇聚了来自澳大利亚各地的8位顶尖专家,组建了涵盖肾脏科、心内科、内分泌科及全科医学的多学科团队,以全面应对慢性肾病(CKD)复杂的合并症管理需求。研究采用改良版虚拟名义组技术:专家们首先依据GRADE标准独立提交建议,经去重整理后,在Microsoft Teams虚拟会议中进行深度阐述与辩论,并通过1-5分制进行匿名评分。最终,严格遵循国际共识程序,仅将支持率超过75%(平均分≥3.5)的建议纳入指南,确保每一条推荐都经得起推敲,真正服务于澳大利亚的临床实践。作者组初拟21条建议,经整合去重形成9项独立推荐。其中5项达成共识(支持率>75%)(表1),另有1项因不符合GRADE标准被剔除。
表1. 澳大利亚针对HCP提升慢性肾病患者护理标准的建议

推荐1:对于慢性肾病高危患者,应定期评估尿白蛋白/肌酐比值(uACR)与估算肾小球滤过率(eGFR)
慢性肾病(CKD)因其极强的隐匿性被称为“沉默的杀手”,患者在出现明显症状之前,肾功能可能已经丧失了高达90%。因此,在症状显现之前进行早期识别与干预至关重要,及时的发现与管理甚至可以将疾病进展的风险降低50%。
目前的筛查策略主要依赖三大核心指标:血压(BP)、uACR及eGFR。
eGFR是评估肾功能的关键指标,澳大利亚病理实验室通常依据≥18岁患者的血清肌酐,通过CKD-EPI预测方程自动计算并报告该数值。尽管该方程已在多种人群中得到验证,但在老年人或肌肉量异常者中可能存在偏差,此时若条件允许,可联合检测半胱氨酸蛋白酶抑制剂C以提高准确性;
uACR被视为肾损伤的敏感标志物,其数值升高预示着肾脏及心血管风险的增加,但在实际临床检查中常被低估。
在临床实践中,应根据患者情况制定个性化的筛查计划。
对于心血管疾病(或家族史)、年龄>50岁、肥胖、糖尿病、高血压及吸烟等CKD高危人群,建议每1~2年测量一次eGFR和uACR;
对于≥18岁的澳大利亚原住民和托雷斯海峡岛民,鉴于其较高的患病风险,建议将筛查频率提高至每年一次
对于已经确诊的CKD患者,则应严格依据KDIGO CKD热图进行风险分层监测(图1):低风险患者每年监测1次,中等风险每年2次,高风险每年3次,而极高风险患者则需要每年进行4次及以上的监测。

图1. eGFR和uACR热图显示患者每年推荐的评估频率。绿色表示低风险,黄色表示风险增加,粉色表示中等风险,红色表示高风险,深红色表示极高风险。
推荐2:大多数CKD患者均可在初级医疗中接受管理,必要时进行转诊
鉴于CKD巨大的公共卫生负担,其管理不应局限于专科。初级保健从业者(如全科医生、护士、药剂师)处于早期发现与干预的第一线,这不仅能为患者争取改变生活方式、延缓疾病进展及降低心血管风险的时间,更具有显著的经济效益——模型显示,每投入1美元进行早期干预,可节省45美元的肾衰竭及相关治疗费用。尽管2020年启动的《国家肾病战略行动计划》已将早期发现列为关键目标,但目前初级保健中仍有超过90%的3期CKD病例未被确诊。因此,提升初级保健医生的诊断与管理能力,并在必要时精准转诊,已成为当务之急。
初级保健从业者应依据推荐1对高危人群进行评估。确诊后,需明确CKD分期(1~5期)及白蛋白尿分级,并遵循KHA慢性肾病手册实施管理计划,但要注意的是,如果患者出现以下情况应及时转诊至肾脏专科:
肾功能急剧恶化:3个月内eGFR下降>15%,或12个月内持续下降≥25%,或eGFR降至<30 ml/min/1.73 m2(甚至<15 ml/min/1.73 m2);
临床表现复杂:出现急性肾炎症状(如少尿、血尿、水肿)、难治性高血压(≥3种药物控制不佳)或持续性重度白蛋白尿(uACR≥30 mg/mmol)。
特殊人群:包括青少年、有家族史者及原住民和托雷斯海峡岛民。
关于转诊决策,可使用肾衰竭风险方程(KFRE)等肾衰竭风险预测工具辅助判断。
推荐3:适当评估和管理心脏代谢风险因素
肾脏、心肺与内分泌系统紧密关联,致使高血压、糖尿病、血脂异常、心力衰竭及吸烟等传统心血管代谢风险因素在慢性肾病患者中极为普遍,并显著加速疾病进展及不良结局。肥胖虽为心脏代谢风险的上游驱动因素,但其过量脂肪组织亦独立关联于肾脏血流动力学及结构性异常。因此,识别并管理肥胖及相关心血管代谢风险因素是慢性肾病管理的核心。KDIGO-CARI指南为脂质管理提供了全面建议,综合风险因素管理已被证实能减少心血管事件并延缓慢性肾病进展。
心-肾-代谢系统中任一系统患病,均应引发对其他系统的评估(如心力衰竭患者应检测尿白蛋白/肌酐比值、糖化血红蛋白及血脂):
心血管疾病风险:当eGFR<45 ml/min/1.73 m2,无需正式风险评估,应直接启动降脂、降压治疗;若eGFR 45~59 ml/min/1.73 m2伴微量白蛋白尿,则视为风险增强因素,应将患者重新归类至更高风险层级;对于无临床动脉粥样硬化性心血管疾病的患者,低密度脂蛋白胆固醇控制目标应至少<1.8 mmol/L。
糖尿病:糖化血红蛋白(HbA1c)目标值应在6.5%至8%之间,并依据估算肾小球滤过率、患者偏好及合并症特征进行个体化调整。
高血压:血压测量应采用标准化技术,并结合门诊与家庭血压监测;对于非透析患者,若可耐受,血压控制目标应为低于130/80 mmHg。
吸烟:戒烟已被证实能减缓慢性肾病进展,应作为优先事项;尽管尼古丁替代疗法及辅助药物治疗尚未在慢性肾病患者中专门研究,但预期获益与其他人群相当,通常推荐使用。
推荐4:对于患有DKD的患者,巧用四大支柱
针对心血管代谢风险因素的管理虽是慢性肾病治疗的核心,但药理学领域的突破已为临床提供了更丰富的工具,特别是在糖尿病肾病管理方面,目前已形成了针对四种不同病理机制的“四支柱”疗法(图2)。

第一支柱为肾素-血管紧张素系统抑制剂(RASi),包括血管紧张素转换酶抑制剂(ACEi)或血管紧张素II受体阻滞剂(ARB),通过降低肾小球内压和血压,长期数据显示其能有效减缓白蛋白尿及疾病进展。
第二支柱是钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i),通过抑制近端小管对钠和葡萄糖的重吸收,恢复管球反馈,减少高滤过状态,除降糖外,还能显著降低心血管风险及预防心力衰竭。
第三支柱是非甾体盐皮质激素受体拮抗剂(ns-MRA),主要针对2型糖尿病(T2DM)合并CKD,旨在纠正醛固酮失调,尽管在1型糖尿病(T1DM)及非糖尿病肾病中的证据尚在积累中。
第四支柱为胰高血糖素样肽-1受体激动剂(GLP-1RA),在降糖和减重的同时改善心血管代谢结局,最新研究证实其能降低疾病进展或心脏死亡风险,这种获益被认为与减少氧化应激、炎症及纤维化有关。
鉴于糖尿病肾病的复杂性,虽然最佳给药顺序或联合方案尚未完全定论,但精算分析提示SGLT2i、ns-MRA和GLP-1RA的联合使用可能提升无事件生存率。因此,共识建议:
对于非糖尿病CKD患者,目前应将应将循证疗法如RASi和SGLT2i视为基础治疗作为基础治疗。
对于合并高血压及白蛋白尿的患者,应启动ACEi或ARB(RASi)治疗,并将剂量滴定至患者可耐受的最高批准剂量。
对于已接受其他降糖药物治疗的T2DM合并CKD患者,若eGFR≥20 ml/min/1.73 m2,建议在现有治疗方案中加用SGLT2i。
对于T2DM患者,若eGFR≥25 ml/min/1.73 m2、血清钾浓度正常,且在RASi最大耐受剂量下仍存在白蛋白尿(≥30 mg/g,即≥3 mg/mmol),可在RASi和SGLT2i基础上加用nsMRA。
对于使用二甲双胍和SGLT2i治疗后仍未达到个体化血糖控制目标,或无法使用上述药物的T2D合并CKD患者,推荐使用GLP-1RA。
结语
澳大利亚慢性肾病负担的日益加重,凸显了制定标准化、循证管理策略的迫切需求——这些策略需整合多学科护理模式并充分利用新兴疗法。为应对这一挑战,本共识建议提供了一个可操作的框架,该框架针对澳大利亚独特的医疗环境量身定制,优先保障医疗公平、以患者为中心的护理以及对合并症的积极管理。通过实施这些策略,临床医生能够改善患者预后,减少CKD相关并发症,并帮助缓解CKD对个人和医疗系统造成的社会经济压力。
参考文献
Schlaich MP, et al. Intern Med J. 2026 Mar 18. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言