编者按
妇女健康是促进女性全面发展的基石。《中国妇女发展纲要(2021-2030年)》[1]明确提出建立妇女全生命周期健康管理模式。多囊卵巢综合征(PCOS)作为女性常见的生殖内分泌代谢性疾病,其管理贯穿从青春期至围绝经期的全过程,与全生命周期健康理念高度契合。自1935年首次报道以来,PCOS诊断标准不断演进。二甲双胍自1994年被首次系统报道用于PCOS治疗后,已积累大量循证医学证据[2-6],但目前仍属超说明书用药,其适用情况、疗程、剂量及不良反应监测等有待规范。为此,中华医学会内分泌学分会牵头发布了国内外首部《二甲双胍在多囊卵巢综合征中的临床应用专家共识》[7](以下简称“《共识》”)。本期默讲堂,中山大学孙逸仙纪念医院严励教授将结合该最新共识,深入解读二甲双胍在PCOS治疗中的规范应用。
专家简介

严励 教授
中山大学孙逸仙纪念医院
中山大学名医,二级教授,博士研究生导师
国务院政府特殊津贴专家
中山大学孙逸仙纪念医院内分泌内科学科带头人
中华医学会内分泌学分会第十一届副主委、肥胖学组组长
中国医师协会内分泌代谢科医师分会副会长、血脂学组组长
中国老年保健医学研究会老年内分泌与代谢病分会主委
中国女医师协会糖尿病专委会副主委
广东省糖尿病临床医学研究中心主任
国家临床医学研究中心广东分中心主任
广州市代谢性疾病重点实验室主任
广东省医师协会内分泌科医师分会第三届主委
广东省医学会内分泌分会第八届主委
PCOS流行病学、病理机制及危害
PCOS全球患病率高达11%~13%,是威胁女性健康的主要疾病之一[7]。然而,其认知与管理仍面临挑战,约70%患者未被诊断,超过1/3诊断延迟[8]。值得关注的是,我国PCOS发病率上升迅速,2007~2017年间年龄标化发病率增幅位居全球第三[9]。
PCOS病因尚不明确,与遗传及环境因素均密切相关,涉及神经、内分泌与免疫系统的复杂调控[7]。胰岛素抵抗(IR)被认为是驱动其多系统紊乱的核心病理生理机制[10]。数据显示,约50%~80%的PCOS患者存在IR,即使在非肥胖患者中该比例也高达75%;约40%~80%患者伴有高雄激素血症[7]。IR通过诱发高胰岛素血症,干扰下丘脑-垂体节律,协同黄体生成素(LH)升高卵巢雄激素水平,同时抑制肝脏合成性激素结合球蛋白(SHBG),使游离雄激素活性增强,而高雄激素血症又进一步加重IR,形成自我延续的病理闭环[10]。
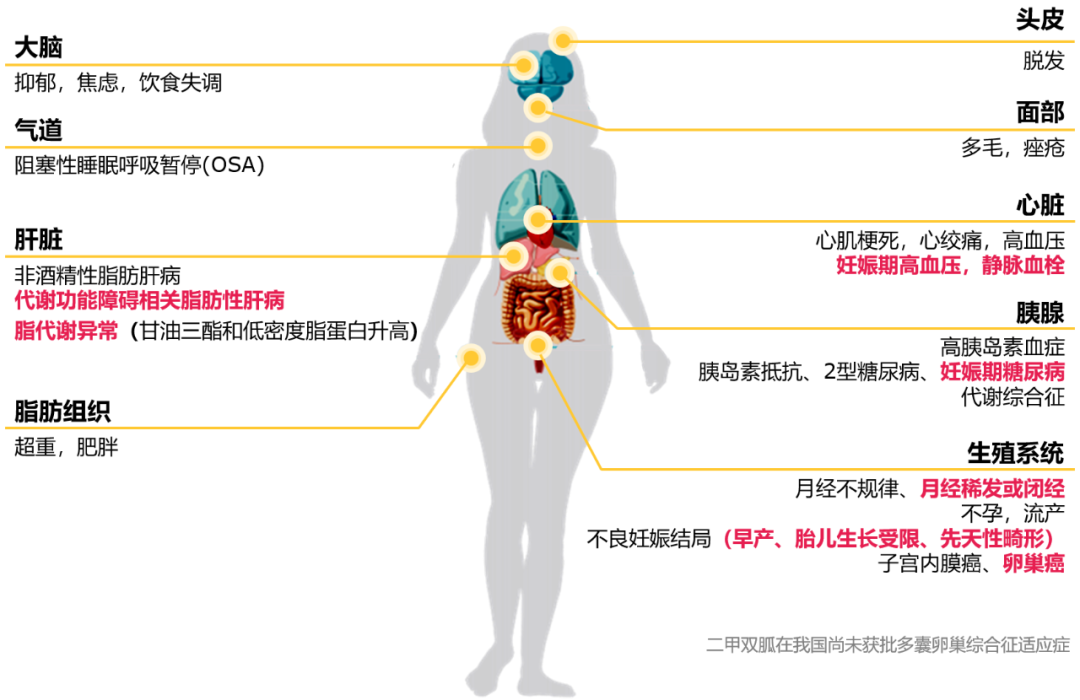
PCOS不仅影响女性生殖与代谢功能,还显著增加心血管疾病、肿瘤等远期风险,并可能对后代健康产生不利影响[7](图1)。相比非PCOS女性,PCOS女性生殖健康异常(月经紊乱、子宫内膜异位症、不孕、体外受精)和妊娠并发症(流产、妊娠期糖尿病、妊娠期高血压、早产、剖宫产、巨大儿)发生率明显升高[11,12],肥胖、2型糖尿病和代谢相关脂肪性肝病(MASLD)等代谢性疾病风险约为2.2~4.7倍[11,13,14],高血压、缺血性心脏病等心脑血管疾病风险约为2.6~3.2倍[11]。
二甲双胍在PCOS中的作用机制
二甲双胍通过全身与局部效应在PCOS中发挥作用。全身层面,其可改善胰岛素敏感性,改善高雄激素血症与抗苗勒管激素水平,改善多囊卵巢形态;通过抑制肝糖异生与糖输出、促进外周组织摄取利用葡萄糖、抑制肠道葡萄糖吸收并促进GLP-1分泌,改善糖代谢异常;降低游离脂肪酸生成,改善肠道脂蛋白代谢,纠正脂代谢紊乱;还能提高排卵及月经周期频率,促进体重减轻、改善慢性低度炎症、改善肠道菌群,增加菌群丰度、减少条件致病菌,并降低粪便乙酰乙酸水平[7,15]。局部层面,二甲双胍一方面通过抑制雄激素受体表达并促使其介导的基因转录正常化,发挥激素调节作用;另一方面改善胰岛素信号传导,调控雄激素对InRS-1及GLUT-4的作用,增强代谢敏感性;其还可调节多种炎症因子水平,发挥抗炎及调节免疫作用,并改善子宫血管分布及内膜下血流[7]。
针对高雄激素血症,二甲双胍兼具直接与间接调控效应(图2)。直接作用体现在改善下丘脑信号网络功能,促进GnRH脉冲分泌、LH和LH/FSH比值正常化,并通过激活卵巢AMPK通路,减少卵巢细胞雄激素合成;间接作用则通过改善IR,增加胰岛素敏感性和提升IGFBP-1水平,降低高胰岛素对卵巢类固醇生成的刺激,并使SHBG水平正常化,从而减轻高雄激素血症[16]。
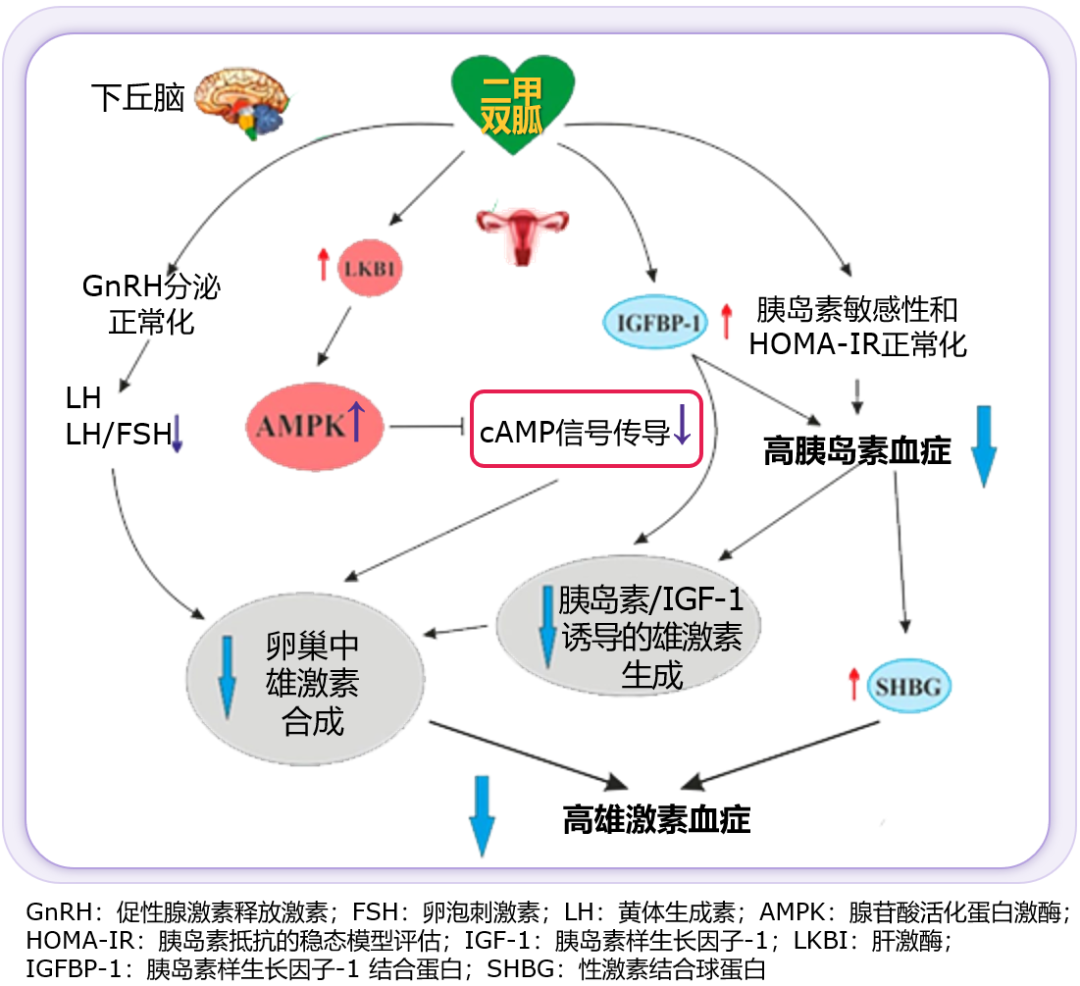
图2. 二甲双胍抑制PCOS高雄激素血症相关通路
二甲双胍在PCOS女性生命周期的应用推荐
《共识》围绕二甲双胍在PCOS女性青春期、育龄期[无生育计划与有生育计划(备孕期、妊娠期、哺乳期)]至围绝经期的应用,共提出20条推荐意见。
1、无生育计划的育龄期PCOS女性
《共识》相关推荐见表1,同时明确了该人群的生殖指标、体重及胰岛素抵抗的评价标准,以利于后续评估治疗方案的合理性与效果。研究显示,二甲双胍不仅可直接作用于子宫内膜,改善PCOS患者子宫内膜病变[17,18],还能改善IR,显著降低睾酮水平,并有效改善糖脂代谢、减轻体重[19]。此外,该药可降低心血管疾病风险,改善颈动脉内膜中层厚度及血管内皮功能,并对MASLD相关肝脂肪变性具有改善作用[20-22]。
表1. 无生育计划的育龄期PCOS女性中二甲双胍应用推荐

临床应用二甲双胍时,建议从小剂量起始,逐渐增至1000~2000 mg/d或最大耐受剂量,且剂量越高,降低体重和改善血脂疗效越强,尤其在PCOS患者中;疗程至少3~6个月,长期应用通常是安全的。当然,也要充分知情同意,监测并处理可能的不良反应(图3)[7]。
2、有生育计划的育龄期PCOS女性
备孕期
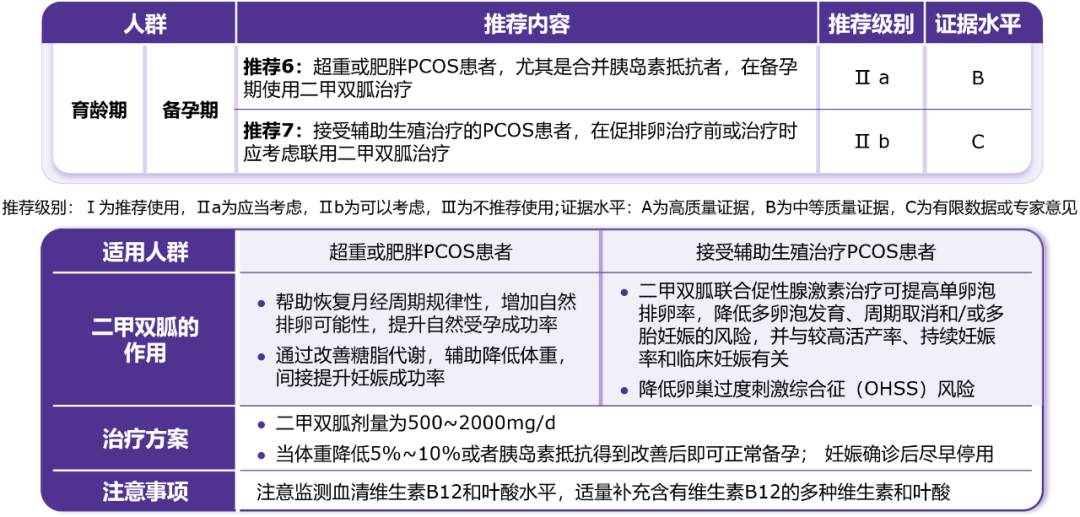
备孕期PCOS患者中,超重或肥胖者尤其是合并IR者,推荐使用二甲双胍以恢复月经周期规律性、增加自然排卵及受孕机会;接受辅助生殖治疗的患者,在促排卵治疗前或治疗时联用二甲双胍可提高单卵泡排卵率,降低多卵泡发育、周期取消及多胎妊娠风险,并显著降低卵巢过度刺激综合征的发生率。二甲双胍的剂量为500~2000 mg/d,待体重下降5%~10%或IR改善后即可备孕,妊娠确诊后应尽早停用(表2)[7]。研究表明,二甲双胍可改善PCOS女性的生殖健康,提高妊娠率[19,23]。
表2. PCOS女性备孕期二甲双胍的应用推荐及治疗细则
《共识》相关推荐见表3。研究表明,二甲双胍可改善PCOS女性妊娠结局,显著降低早产风险,减少母体孕期体重增加,促进足月产[19];对新生儿出生体重无显著影响,不增加畸形风险[24,25]。二甲双胍对后代的长期影响尚不确定[26-29],目前仍缺乏针对后代进入青春期及成年后的观察性研究。
表3. PCOS女性妊娠期二甲双胍的应用推荐

二甲双胍起始剂量是500 mg/d,通常用量为1000~2000 mg/d,可分次口服。根据PCOS患者使用二甲双胍治疗目的不同,在患者知情同意后,二甲双胍可在孕前和妊娠期任一时间起始,并于妊娠全程使用(图4)[7]。

图4. PCOS女性妊娠期二甲双胍的临床治疗细则
表4. PCOS女性哺乳期二甲双胍的应用推荐及治疗细则

3、青春期与围绝经期PCOS女性
青春期PCOS患者以代谢异常表型为主者,在生活方式干预基础上可联合二甲双胍治疗,有助于改善体重指数、血脂和糖代谢,恢复月经周期,降低雄激素水平[7,30,31]。推荐剂量为1500~2000 mg/d,疗程至少3~6个月,可用于10岁及以上青少年(表5)[7]。
围绝经期PCOS患者常伴有多种合并症,二甲双胍可改善其代谢异常,但需注意多药联用及肝肾功能监测(表5)[7]。
表5. 青春期与围绝经期PCOS女性二甲双胍的应用推荐及治疗细则

4、联合治疗策略
针对PCOS患者不同临床特征及治疗反应,可在二甲双胍基础上联用改善IR或促排卵药物,部分方案需充分知情同意。《共识》相关推荐见表6。
表6. 二甲双胍与其他药物的联合应用推荐

综上,二甲双胍在PCOS女性全生命周期中的应用需结合患者代谢状态、生育需求及治疗反应,综合权衡获益与潜在风险,进行个体化管理(图5)。
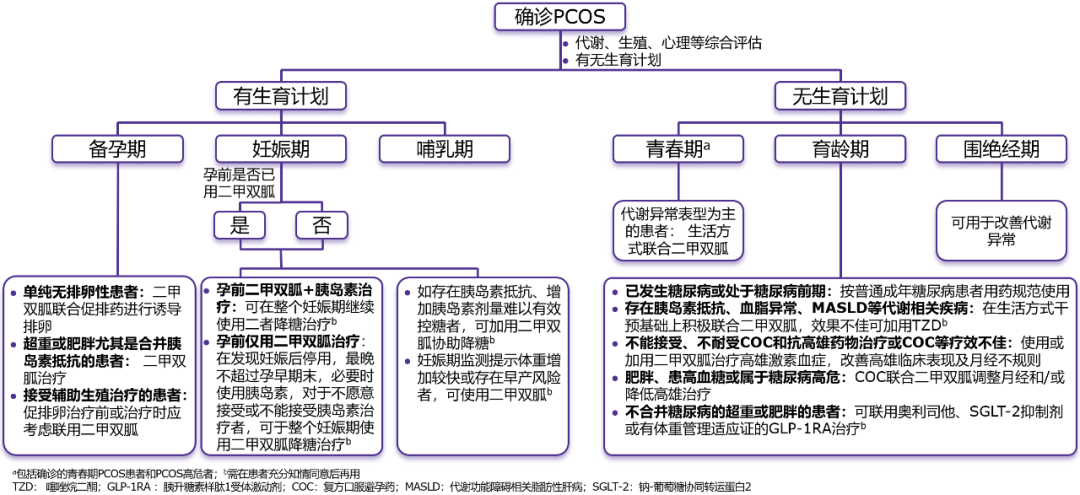
图5.《共识》中二甲双胍在PCOS女性全生命周期应用的临床路径
总结
我国PCOS发病率增长迅速,其核心病理生理机制为IR,可驱动全身多系统功能紊乱,导致代谢异常、生殖功能受损等多种疾病,严重影响女性健康。二甲双胍通过改善IR,在PCOS疾病管理中发挥多重关键作用,包括纠正生殖内分泌紊乱、改善代谢异常、提高整体健康水平及改善妊娠结局等。在PCOS女性生命周期的不同阶段合理使用二甲双胍,可为患者带来多重获益。
注:二甲双胍在我国尚未获批PCOS、减重、糖尿病前期、妊娠糖尿病、MASLD等适应症;在二甲双胍治疗期间不推荐哺乳。本文仅供医疗卫生人士学术交流。
参考文献
1.《中国妇女发展纲要(2021-2030年)》. https://www.gov.cn/gongbao/content/2021/content_5643262.htm
2. 中国医师协会内分泌代谢科医师分会. 中华内分泌代谢杂志. 2018; 34(1): 1-7.
3. 王娅洁, 龙晓宇. 中华生殖与避孕杂志. 2025; 45(10): 1058-1066.
4. Velazquez EM, et al. Metabolism. 1994; 43(5): 647-654.
5. Salley KE, et al. J Clin Endocrinol Metab. 2007; 92(12): 4546-4556.
6. Teede HJ, et al. J Clin Endocrinol Metab. 2023; 108(10): 2447-2469.
7. 中华医学会内分泌学分会.中华内分泌代谢杂志. 2025; 41(12): 979-991.
8. 多囊卵巢综合征诊治路径专家共识编写组. 中华生殖与避孕杂志. 2023; 43(4): 337-345.
9. Liu J, et al. Hum Reprod. 2021; 36(4): 1108-1119.
10. Zhao H, et al. J Ovarian Res. 2023; 16(1): 9.
11. Hart R. J Clin Endocrinol Metab. 2015; 100(3): 911-919.
12. 王婷婷, 等. 中南大学学报(医学版). 2017; 42(11): 1300-1310.
13. Kakoly NS, et al. Diabetes Care. 2019; 42(4): 560-567.
14. Kumarendran B, et al. PLoS Med. 2018; 15(3): e1002542.
15. Palomba S, et al. Hum Reprod Update. 2021; 27(3): 584-618.
16. Shpakov AO. Pharmaceuticals (Basel). 2021; 14(1): 42.
17. Eriksson G, et al. Nat Med. 2025; 31(6): 1925-1938.
18. Tan BK, et al. J Clin Endocrinol Metab. 2011; 96(3): 808-816.
19. Mousa, Aya, et al. 2023. Technical Report for the 2023 International Evidence-based Guideline for the Assessment and Management of Polycystic Ovary Syndrome. Monash University. Report.
20. Wang F, et al. BMC Womens Health. 2024; 24(1): 426.
21. Heidari B, et al. Mayo Clin Proc. 2019; 94(12): 2455-2466.
22. Riemann A, et al. J Clin Med. 2022; 11(15): 4294.
23. Morley LC, et al. Cochrane Database Syst Rev. 2017; 11(11): CD003053.
24. Løvvik TS, et al. Lancet Diabetes Endocrinol. 2019; 7(4): 256-266.
25. 王蕴慧, 等. 中华围产医学杂志. 2011; 14(10): 592-597.
26. Greger HK, et al. BMC Pediatr. 2020; 20(1): 60.
27. Nilsen GØ, et al. Acta Obstet Gynecol Scand. 2024; 103(1): 176-187.
28. Hanem L, et al. J Clin Endocrinol Metab. 2018; 103(4): 1612-1621.
29. Hanem L, et al. Lancet Child Adolesc Health. 2019; 3(3): 166-174.
30. Al Khalifah RA, et al. Pediatrics. 2016; 137(5): e20154089.
31. Allen HF, et al. J Pediatr Endocrinol Metab. 2005; 18(8): 761-768. 2 comments
妇女健康是促进女性全面发展的基石。《中国妇女发展纲要(2021-2030年)》[1]明确提出建立妇女全生命周期健康管理模式。多囊卵巢综合征(PCOS)作为女性常见的生殖内分泌代谢性疾病,其管理贯穿从青春期至围绝经期的全过程,与全生命周期健康理念高度契合。自1935年首次报道以来,PCOS诊断标准不断演进。二甲双胍自1994年被首次系统报道用于PCOS治疗后,已积累大量循证医学证据[2-6],但目前仍属超说明书用药,其适用情况、疗程、剂量及不良反应监测等有待规范。为此,中华医学会内分泌学分会牵头发布了国内外首部《二甲双胍在多囊卵巢综合征中的临床应用专家共识》[7](以下简称“《共识》”)。本期默讲堂,中山大学孙逸仙纪念医院严励教授将结合该最新共识,深入解读二甲双胍在PCOS治疗中的规范应用。
专家简介

严励 教授
中山大学孙逸仙纪念医院
中山大学名医,二级教授,博士研究生导师
国务院政府特殊津贴专家
中山大学孙逸仙纪念医院内分泌内科学科带头人
中华医学会内分泌学分会第十一届副主委、肥胖学组组长
中国医师协会内分泌代谢科医师分会副会长、血脂学组组长
中国老年保健医学研究会老年内分泌与代谢病分会主委
中国女医师协会糖尿病专委会副主委
广东省糖尿病临床医学研究中心主任
国家临床医学研究中心广东分中心主任
广州市代谢性疾病重点实验室主任
广东省医师协会内分泌科医师分会第三届主委
广东省医学会内分泌分会第八届主委
PCOS流行病学、病理机制及危害
PCOS全球患病率高达11%~13%,是威胁女性健康的主要疾病之一[7]。然而,其认知与管理仍面临挑战,约70%患者未被诊断,超过1/3诊断延迟[8]。值得关注的是,我国PCOS发病率上升迅速,2007~2017年间年龄标化发病率增幅位居全球第三[9]。
PCOS病因尚不明确,与遗传及环境因素均密切相关,涉及神经、内分泌与免疫系统的复杂调控[7]。胰岛素抵抗(IR)被认为是驱动其多系统紊乱的核心病理生理机制[10]。数据显示,约50%~80%的PCOS患者存在IR,即使在非肥胖患者中该比例也高达75%;约40%~80%患者伴有高雄激素血症[7]。IR通过诱发高胰岛素血症,干扰下丘脑-垂体节律,协同黄体生成素(LH)升高卵巢雄激素水平,同时抑制肝脏合成性激素结合球蛋白(SHBG),使游离雄激素活性增强,而高雄激素血症又进一步加重IR,形成自我延续的病理闭环[10]。
PCOS不仅影响女性生殖与代谢功能,还显著增加心血管疾病、肿瘤等远期风险,并可能对后代健康产生不利影响[7](图1)。相比非PCOS女性,PCOS女性生殖健康异常(月经紊乱、子宫内膜异位症、不孕、体外受精)和妊娠并发症(流产、妊娠期糖尿病、妊娠期高血压、早产、剖宫产、巨大儿)发生率明显升高[11,12],肥胖、2型糖尿病和代谢相关脂肪性肝病(MASLD)等代谢性疾病风险约为2.2~4.7倍[11,13,14],高血压、缺血性心脏病等心脑血管疾病风险约为2.6~3.2倍[11]。
二甲双胍在PCOS中的作用机制
二甲双胍通过全身与局部效应在PCOS中发挥作用。全身层面,其可改善胰岛素敏感性,改善高雄激素血症与抗苗勒管激素水平,改善多囊卵巢形态;通过抑制肝糖异生与糖输出、促进外周组织摄取利用葡萄糖、抑制肠道葡萄糖吸收并促进GLP-1分泌,改善糖代谢异常;降低游离脂肪酸生成,改善肠道脂蛋白代谢,纠正脂代谢紊乱;还能提高排卵及月经周期频率,促进体重减轻、改善慢性低度炎症、改善肠道菌群,增加菌群丰度、减少条件致病菌,并降低粪便乙酰乙酸水平[7,15]。局部层面,二甲双胍一方面通过抑制雄激素受体表达并促使其介导的基因转录正常化,发挥激素调节作用;另一方面改善胰岛素信号传导,调控雄激素对InRS-1及GLUT-4的作用,增强代谢敏感性;其还可调节多种炎症因子水平,发挥抗炎及调节免疫作用,并改善子宫血管分布及内膜下血流[7]。
针对高雄激素血症,二甲双胍兼具直接与间接调控效应(图2)。直接作用体现在改善下丘脑信号网络功能,促进GnRH脉冲分泌、LH和LH/FSH比值正常化,并通过激活卵巢AMPK通路,减少卵巢细胞雄激素合成;间接作用则通过改善IR,增加胰岛素敏感性和提升IGFBP-1水平,降低高胰岛素对卵巢类固醇生成的刺激,并使SHBG水平正常化,从而减轻高雄激素血症[16]。

图2. 二甲双胍抑制PCOS高雄激素血症相关通路
二甲双胍在PCOS女性生命周期的应用推荐
《共识》围绕二甲双胍在PCOS女性青春期、育龄期[无生育计划与有生育计划(备孕期、妊娠期、哺乳期)]至围绝经期的应用,共提出20条推荐意见。
1、无生育计划的育龄期PCOS女性
《共识》相关推荐见表1,同时明确了该人群的生殖指标、体重及胰岛素抵抗的评价标准,以利于后续评估治疗方案的合理性与效果。研究显示,二甲双胍不仅可直接作用于子宫内膜,改善PCOS患者子宫内膜病变[17,18],还能改善IR,显著降低睾酮水平,并有效改善糖脂代谢、减轻体重[19]。此外,该药可降低心血管疾病风险,改善颈动脉内膜中层厚度及血管内皮功能,并对MASLD相关肝脂肪变性具有改善作用[20-22]。
表1. 无生育计划的育龄期PCOS女性中二甲双胍应用推荐

临床应用二甲双胍时,建议从小剂量起始,逐渐增至1000~2000 mg/d或最大耐受剂量,且剂量越高,降低体重和改善血脂疗效越强,尤其在PCOS患者中;疗程至少3~6个月,长期应用通常是安全的。当然,也要充分知情同意,监测并处理可能的不良反应(图3)[7]。

2、有生育计划的育龄期PCOS女性
备孕期
备孕期PCOS患者中,超重或肥胖者尤其是合并IR者,推荐使用二甲双胍以恢复月经周期规律性、增加自然排卵及受孕机会;接受辅助生殖治疗的患者,在促排卵治疗前或治疗时联用二甲双胍可提高单卵泡排卵率,降低多卵泡发育、周期取消及多胎妊娠风险,并显著降低卵巢过度刺激综合征的发生率。二甲双胍的剂量为500~2000 mg/d,待体重下降5%~10%或IR改善后即可备孕,妊娠确诊后应尽早停用(表2)[7]。研究表明,二甲双胍可改善PCOS女性的生殖健康,提高妊娠率[19,23]。
表2. PCOS女性备孕期二甲双胍的应用推荐及治疗细则
《共识》相关推荐见表3。研究表明,二甲双胍可改善PCOS女性妊娠结局,显著降低早产风险,减少母体孕期体重增加,促进足月产[19];对新生儿出生体重无显著影响,不增加畸形风险[24,25]。二甲双胍对后代的长期影响尚不确定[26-29],目前仍缺乏针对后代进入青春期及成年后的观察性研究。
表3. PCOS女性妊娠期二甲双胍的应用推荐

二甲双胍起始剂量是500 mg/d,通常用量为1000~2000 mg/d,可分次口服。根据PCOS患者使用二甲双胍治疗目的不同,在患者知情同意后,二甲双胍可在孕前和妊娠期任一时间起始,并于妊娠全程使用(图4)[7]。

图4. PCOS女性妊娠期二甲双胍的临床治疗细则
哺乳期
表4. PCOS女性哺乳期二甲双胍的应用推荐及治疗细则

3、青春期与围绝经期PCOS女性
青春期PCOS患者以代谢异常表型为主者,在生活方式干预基础上可联合二甲双胍治疗,有助于改善体重指数、血脂和糖代谢,恢复月经周期,降低雄激素水平[7,30,31]。推荐剂量为1500~2000 mg/d,疗程至少3~6个月,可用于10岁及以上青少年(表5)[7]。
围绝经期PCOS患者常伴有多种合并症,二甲双胍可改善其代谢异常,但需注意多药联用及肝肾功能监测(表5)[7]。
表5. 青春期与围绝经期PCOS女性二甲双胍的应用推荐及治疗细则

4、联合治疗策略
针对PCOS患者不同临床特征及治疗反应,可在二甲双胍基础上联用改善IR或促排卵药物,部分方案需充分知情同意。《共识》相关推荐见表6。
表6. 二甲双胍与其他药物的联合应用推荐

综上,二甲双胍在PCOS女性全生命周期中的应用需结合患者代谢状态、生育需求及治疗反应,综合权衡获益与潜在风险,进行个体化管理(图5)。

图5.《共识》中二甲双胍在PCOS女性全生命周期应用的临床路径
总结
我国PCOS发病率增长迅速,其核心病理生理机制为IR,可驱动全身多系统功能紊乱,导致代谢异常、生殖功能受损等多种疾病,严重影响女性健康。二甲双胍通过改善IR,在PCOS疾病管理中发挥多重关键作用,包括纠正生殖内分泌紊乱、改善代谢异常、提高整体健康水平及改善妊娠结局等。在PCOS女性生命周期的不同阶段合理使用二甲双胍,可为患者带来多重获益。
注:二甲双胍在我国尚未获批PCOS、减重、糖尿病前期、妊娠糖尿病、MASLD等适应症;在二甲双胍治疗期间不推荐哺乳。本文仅供医疗卫生人士学术交流。
参考文献
1.《中国妇女发展纲要(2021-2030年)》. https://www.gov.cn/gongbao/content/2021/content_5643262.htm
2. 中国医师协会内分泌代谢科医师分会. 中华内分泌代谢杂志. 2018; 34(1): 1-7.
3. 王娅洁, 龙晓宇. 中华生殖与避孕杂志. 2025; 45(10): 1058-1066.
4. Velazquez EM, et al. Metabolism. 1994; 43(5): 647-654.
5. Salley KE, et al. J Clin Endocrinol Metab. 2007; 92(12): 4546-4556.
6. Teede HJ, et al. J Clin Endocrinol Metab. 2023; 108(10): 2447-2469.
7. 中华医学会内分泌学分会.中华内分泌代谢杂志. 2025; 41(12): 979-991.
8. 多囊卵巢综合征诊治路径专家共识编写组. 中华生殖与避孕杂志. 2023; 43(4): 337-345.
9. Liu J, et al. Hum Reprod. 2021; 36(4): 1108-1119.
10. Zhao H, et al. J Ovarian Res. 2023; 16(1): 9.
11. Hart R. J Clin Endocrinol Metab. 2015; 100(3): 911-919.
12. 王婷婷, 等. 中南大学学报(医学版). 2017; 42(11): 1300-1310.
13. Kakoly NS, et al. Diabetes Care. 2019; 42(4): 560-567.
14. Kumarendran B, et al. PLoS Med. 2018; 15(3): e1002542.
15. Palomba S, et al. Hum Reprod Update. 2021; 27(3): 584-618.
16. Shpakov AO. Pharmaceuticals (Basel). 2021; 14(1): 42.
17. Eriksson G, et al. Nat Med. 2025; 31(6): 1925-1938.
18. Tan BK, et al. J Clin Endocrinol Metab. 2011; 96(3): 808-816.
19. Mousa, Aya, et al. 2023. Technical Report for the 2023 International Evidence-based Guideline for the Assessment and Management of Polycystic Ovary Syndrome. Monash University. Report.
20. Wang F, et al. BMC Womens Health. 2024; 24(1): 426.
21. Heidari B, et al. Mayo Clin Proc. 2019; 94(12): 2455-2466.
22. Riemann A, et al. J Clin Med. 2022; 11(15): 4294.
23. Morley LC, et al. Cochrane Database Syst Rev. 2017; 11(11): CD003053.
24. Løvvik TS, et al. Lancet Diabetes Endocrinol. 2019; 7(4): 256-266.
25. 王蕴慧, 等. 中华围产医学杂志. 2011; 14(10): 592-597.
26. Greger HK, et al. BMC Pediatr. 2020; 20(1): 60.
27. Nilsen GØ, et al. Acta Obstet Gynecol Scand. 2024; 103(1): 176-187.
28. Hanem L, et al. J Clin Endocrinol Metab. 2018; 103(4): 1612-1621.
29. Hanem L, et al. Lancet Child Adolesc Health. 2019; 3(3): 166-174.
30. Al Khalifah RA, et al. Pediatrics. 2016; 137(5): e20154089.
31. Allen HF, et al. J Pediatr Endocrinol Metab. 2005; 18(8): 761-768. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言