编者按:骨质疏松症的全程管理离不开对骨代谢动态变化的精准评估,而骨转换标志物在其中扮演着不可或缺的角色。3月21~22日,第十二届老年骨质疏松与糖尿病新进展交流大会在北京顺利召开,来自复旦大学附属华东医院的程群教授以“骨转换指标与骨质疏松管理”为题做了精彩主题报告,系统梳理了骨转换标志物(BTM)在流行病学评估、诊断鉴别、治疗监测及不良事件预警中的核心作用,并结合国内外最新研究进展,深入探讨了其在临床实践中的规范化应用。

一、骨质疏松症流行病学
骨质疏松症已成为全球范围内日益严峻的公共卫生挑战。据估计,全球骨质疏松症患者已超过2亿[1],且患病率随年龄增长而显著增加[2]。一项基于美国国家健康与营养调查(NHANES)Ⅲ数据的研究[2],采用股骨颈或腰椎骨密度标准,对北美、欧洲、日本及澳大利亚等多个国家/地区的骨质疏松症患病率进行了估算。结果显示(图1),女性患病率基于股骨颈骨密度介于9%(英国)至15%(法国、德国)之间,纳入腰椎数据后扩大至16%(美国)至38%(日本)。男性患病率基于股骨颈骨密度为1%(英国)至4%(日本),纳入腰椎数据后为3%(加拿大)至8%(法国、德国、意大利、西班牙)。总体而言,上述地区符合世界卫生组织骨质疏松症诊断标准者高达4900万。
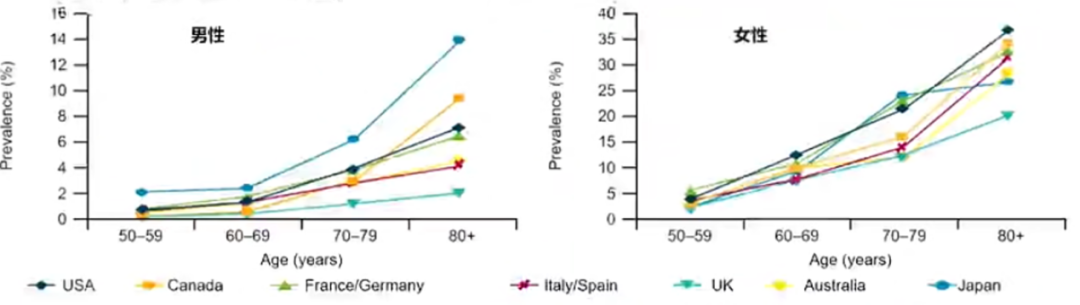
图1. 不同国家骨质疏松症患病率
骨质疏松症的核心危害在于增加脆性骨折风险,并带来沉重的疾病负担。以欧盟为例,2010年约2750万骨质疏松患者,其中新发骨折350万例,经济负担高达370亿欧元,新发骨折费用占66%,长期照护占29%,药物预防仅占5%[3]。骨折导致118万质量调整生命年损失,预计2025年相关费用再增25%。然而,绝大多数骨折患者或高骨折风险人群未接受规范治疗,且治疗率呈下降趋势。转向国内,我国形势同样严峻,目前骨质疏松症患者达1.26亿,骨量减少人群高达8.1亿,骨量减少前期状态者亦有2.1亿。但需注意的是,这一数据可能被低估,现有调查多集中于大城市,广大边远地区的筛查覆盖仍存空白。
二、骨转换标志物与诊断评估
骨转换标志物(bone turnover markers,BTM)是反映骨骼代谢动态状况的关键生化指标。具体而言,骨形成标志物如P1NP(Ⅰ型前胶原氨基端前肽)反映成骨细胞活性;骨吸收标志物如CTX(Ⅰ型胶原羧基端肽)反映破骨细胞介导的胶原降解(图2)[4]。胶原合成始于N端、降解始于C端,因此选择P1NP与CTX能够实现骨形成与骨吸收过程的“端对端”精准匹配,具有更好的机制互补性与特异性。基于此,2010年国际骨质疏松基金会(IOF)[5]推荐血清CTX与P1NP作为参考标志物;2012年美国骨健康联盟联合美国临床化学协会[6]进一步明确血清CTX为优选的骨吸收标志物,P1NP为优选的骨形成标志物。在疾病诊断和治疗过程中,至少选择一个骨形成标志物和一个骨吸收标志物[7]。
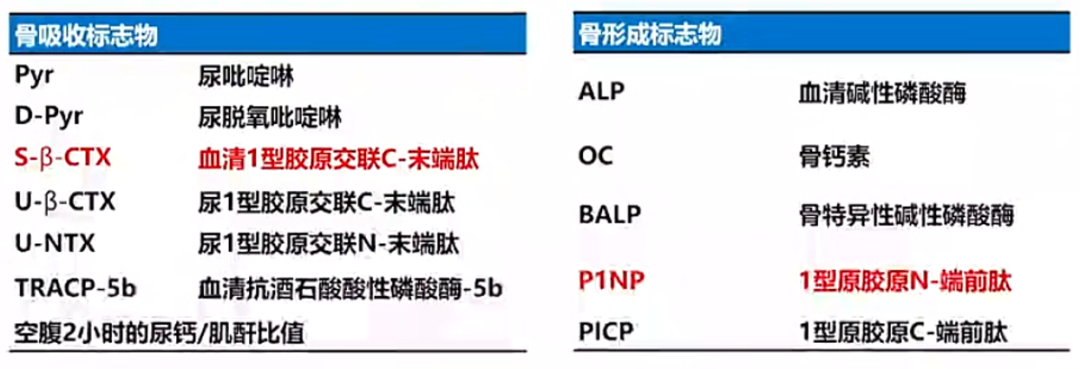
图2. 骨转换标志物种类
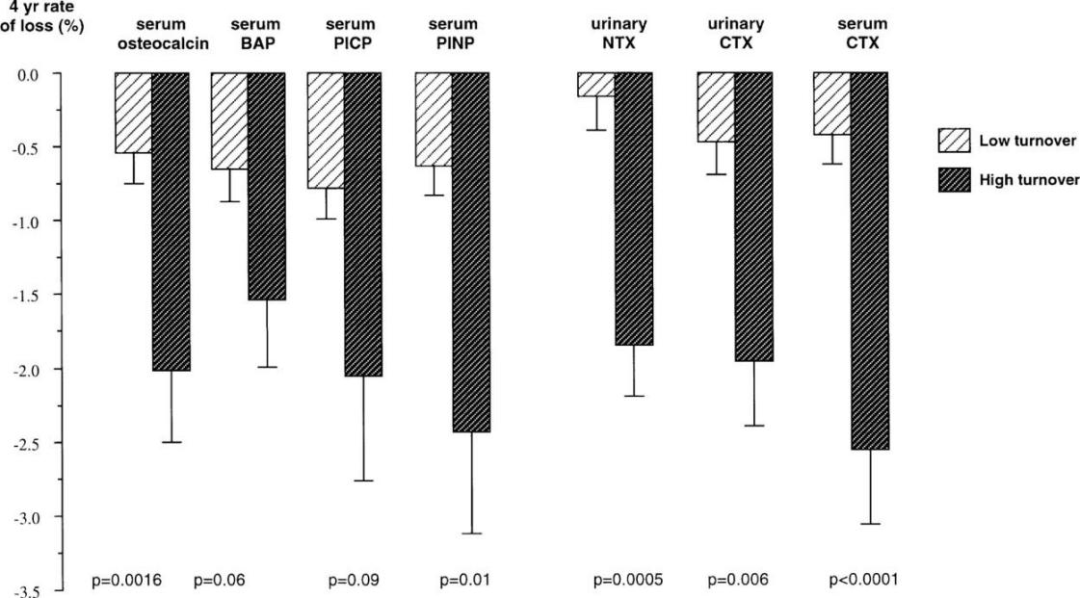
BTM代表全身骨骼代谢的动态状况,可预测骨丢失,反映未来骨质疏松的风险。一项前瞻性队列研究(OFELY)[8]纳入305例50~88岁的健康绝经后女性,检测基线血清骨钙素、P1NP、P1CP、BALP、CTX和尿液NTX、CTX等多项骨转换标志物,并评估其对4年内桡骨远端及中段骨密度变化的预测作用。结果显示(图3),与BTM水平较低的绝经后女性相比,BTM高于绝经前参考范围上限的患者,桡骨中段骨量流失多4~6倍,桡骨远端骨量流失多1.8~2倍。该研究证实,BTM水平升高可有效预测骨量加速流失,为临床早期识别高风险人群提供了重要依据。
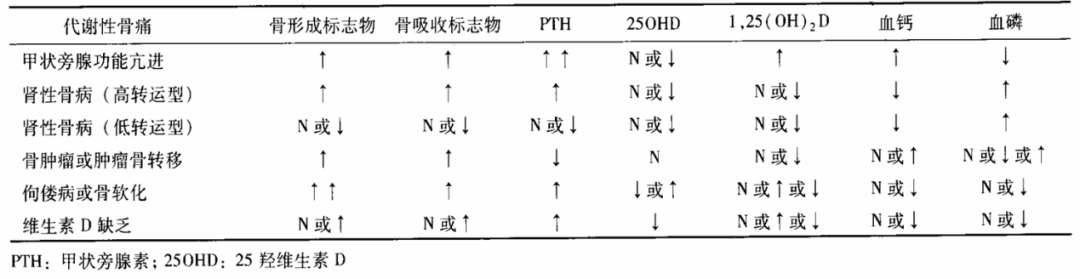
BTM在鉴别诊断中具有重要价值,有助于区分不同类型骨代谢疾病。在临床实践中,若BTM水平超过参考范围上限的1.5倍,提示骨转换率明显升高,这一特征常见于新发骨折、甲状旁腺功能亢进症、多发性骨髓瘤或骨质疏松症等疾病。如下表[4]所示,表1汇总了常见代谢性骨病骨代谢生化标志物的变化特征,可为临床鉴别诊断提供重要参考依据。
表1. 常见代谢性骨病骨代谢生化标志物变化
三、骨转换标志物与治疗监测
如前所述,BTM的检测不仅有助于骨代谢疾病的鉴别诊断,还可用于监测药物疗效及治疗依从性等。值得注意的是,维生素D是抗骨质疏松治疗的基础用药,AACE/ACE绝经后骨质疏松临床实践指南[7]建议:维生素D缺乏风险人群,尤其骨质疏松患者需监测25-羟基维生素D(25OHD)水平(B级;BEL 2);骨质疏松患者应每日补充1000~2000 IU维生素D,将血清25OHD水平维持在30 ng/ml以上(A级;BEL1)。研究显示,血清维生素D水平每降低1 ng/ml,双膦酸盐的治疗反应下降5%(OR=0.95,95%CI:0.92~0.98;P=0.0006)[9]。
在明确维生素D状态后,可通过BTM降低超过最小有意义变化(LSC)或降至参考区间几何均值以下来评估治疗疗效或依从性。具体阈值如下[10]:
抗骨吸收药物治疗时,P1NP降低>10 μg/L(LSC),或降低至<35 μg/L(目标值);CTX降低>100 ng/L(LSC),或降低至<280 ng/L(目标值);
促骨形成药物治疗时,P1NP升高幅度>10 μg/L(LSC),或升高至>69 μg/L(目标值)。
在监测频率方面,临床实践中推荐每3~6个月监测一次BTM,包括P1NP、CTX、维生素D、血钙、血磷等。从变化趋势来看,抗骨吸收药物治疗后,P1NP与CTX均下降,其中CTX下降更为显著;促骨形成药物则使P1NP、CTX均上升,P1NP上升幅度更大,形成“骨形成升窗”(图4)[11-13]。
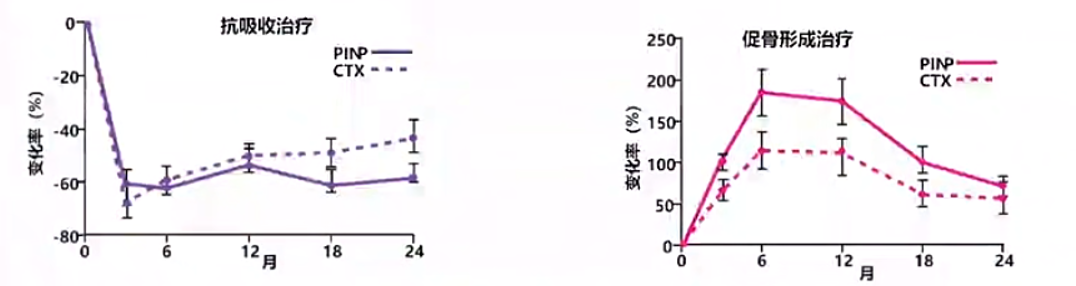
图4. 使用抗吸收治疗(紫色)和促骨形成治疗(粉色)后BTM的变化幅度均值
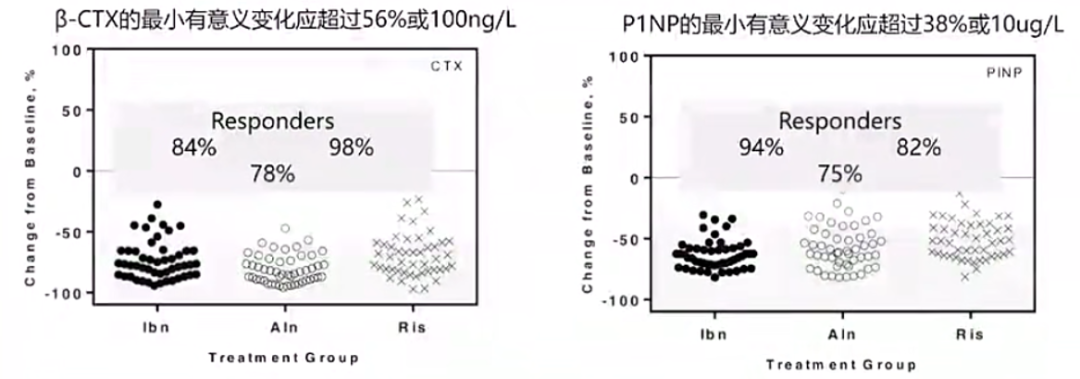
关于应答判断标准,判断治疗应答需关注最小有意义变化(LSC)。一项纳入172例绝经后骨质疏松妇女的开放性随机对照干预性研究(TRIO研究)[14-16],评估了3种双膦酸盐(伊班膦酸钠、阿仑膦酸钠、利塞膦酸钠)的疗效,采用BTM的两种目标反应定义进行评估:一是降至参考区间几何均值以下,二是变化超过LSC。研究结果显示,CTX下降需超过56%、P1NP下降需超过38%方可认为充分应答(图5)。无论采用哪种目标反应定义,70%~100%女性的CTX和P1NP均能达到治疗达标标准。相反,若BTM无明显变化,则提示患者依从性差或用药方法不当。
在指导序贯治疗方案方面,一项纳入161例绝经后女性的回顾性研究显示,地舒单抗停药2年的骨密度(BMD)丢失与血清Ⅰ型胶原C端肽(sCTX)升高显著相关(P<0.001),提示sCTX是预测停药后骨量丢失的有效指标;经ROC曲线分析,停药1年内将sCTX控制在正常值上限的49.1%(≈281.3 ng/L)以下,可有效预防2年后腰椎BMD丢失[17],为临床序贯治疗及病情监测提供了量化管控目标,可据此指导抗骨吸收药物序贯,有效预防停药后骨量快速反弹与丢失,降低骨折风险。
此外,BTM还可协助评估药物不良事件。地舒单抗治疗后可能出现低钙血症,基线BTM水平较高的患者更易发生,需积极补充钙+维生素D。同时,关于非典型股骨骨折与下颌骨坏死风险,有研究提出血清CTX水平低于150 ng/L时拔牙或种植牙风险可能增加,尽管这一阈值尚未形成共识,但可为临床提供参考[18]。
关于治疗选择,治疗开始前的BTM水平是否有助于选择最佳治疗方案,目前尚存争议[19]。数据显示,基线高P1NP水平与阿仑膦酸钠治疗减少非椎体骨折相关,但该关联未在其他标志物或骨折类型中得到验证;基线BTM水平与特立帕肽疗效无关;低P1NP者对唑来膦酸反应欠佳。因此,药物选择应基于骨折风险分层而非BTM水平。这表明,BTM在指导初始药物选择方面的价值有限,其核心应用仍聚焦于治疗过程中的疗效评价与依从性监测。
四、骨转换标志物的生物学变异与临床应用局限性
1. 生物学变异与检测标准化
BTM的检测结果受多种生物学因素影响,为确保检测结果的准确性,临床采样需遵循标准化流程:
采样时间与饮食:骨吸收标志物(如CTX)具有显著的昼夜节律(夜间最高,下午最低)及进餐抑制效应(早餐后下降约50%)。建议受试者隔夜禁食后,于清晨07:30-10:00采集空腹血样。
人口学因素:需考虑年龄(儿童及青春期较高,随年龄增长波动)、性别(<35岁年轻男性与绝经后女性差异)及绝经年限的影响,建议使用基于年龄和性别特异的参考区间。
生理状态:妊娠期、哺乳期及月经周期(黄体期)可导致指标波动;生活方式如吸烟(升高)、饮酒(降低)及剧烈运动(采样前1天应避免)亦需注意。
病理与药物干扰:
肝肾功能:慢性肾脏病(尤其是继发性甲旁亢或无动力性骨病)及肝脏疾病(纤维化阶段)会显著改变BTM水平;经肾脏排泄的标志物(如CTX、骨钙素)在肾功能不全时可能假性升高。
药物影响:糖皮质激素、抗惊厥药、肝素等可升高或降低BTM;钙剂与维生素D补充可能轻微降低骨转换;特定抗骨质疏松药物(如双膦酸盐、地舒单抗、特立帕肽)则会产生显著的特异性改变。
2. 临床应用的局限性与综合判读原则
尽管BTM是评估骨代谢动态变化的敏感指标,但在临床应用中存在以下局限性,需结合其他检查进行综合判读:
不能替代骨密度诊断:BTM反映的是骨转换的速率,而非骨骼的矿化程度或骨微结构。它不能替代BMD作为骨质疏松诊断的金标准。
缺乏定位特异性:BTM骨转换过程中产生的中间代谢产物或酶类,无法定位具体的局部骨病变(如单发的骨肿瘤或局部感染)。
特异性有限:BTM轻度升高缺乏疾病特异性,可见于生理波动或多种代谢性骨病(如继发性甲旁亢、多发性骨髓瘤、骨质疏松等),需结合临床背景鉴别。
综合判读原则:临床决策应遵循“BTM+BMD+临床风险因素”的综合判读模式。即结合生化标志物的动态变化、影像学的骨量评估以及患者的骨折风险因素,以实现骨质疏松症的精准管理与疗效监测。
五、结语
BTM不仅可用于骨折风险评估、鉴别诊断、疗效监测与依从性评估,还能在序贯治疗中监测病情,同时协助评价药物不良事件。检测技术的进步,为临床应用提供了可靠工具。尽管如此,临床应用中仍需注意其生物学变异及检测标准化等局限性,应结合骨密度及临床风险因素进行综合判读。
专家简介
复旦大学附属华东医院
骨质疏松科主任、医学博士、主任医师、教授、博士生导师
上海市医学会骨质疏松专科分会前任主任委员
中华医学会骨质疏松和骨矿盐疾病分会常委
中国老年保健医学研究会骨质疏松分会副主任委员
中华医学会老年医学分会骨代谢病学组副组长
复旦大学骨关节研究所副所长
参考文献
[1] Reginster JY, Burlet N. Osteoporosis: a still increasing prevalence. Bone 2006; 38 (2 Suppl 1): S4-9.
[2] Wade SW, Strader C, Fitzpatrick LA et al. Estimating prevalence of osteoporosis: examples from industrialized countries. Arch Osteoporos 2014; 9: 182.
[3] Hernlund E, Svedbom A, Iverg?rd M et al. Osteoporosis in the European Union: medical management, epidemiology and economic burden. A report prepared in collaboration with the International Osteoporosis Foundation (IOF) and the European Federation of Pharmaceutical Industry Associations (EFPIA). Arch Osteoporos 2013; 8 (1): 136.
[4] 中华医学会骨质疏松和骨矿盐疾病分会. 中华骨质疏松和骨盐疾病杂志, 2015; 8(4): 283-293.
[5] Vasikaran S, Eastell R, Bruyère O et al. Markers of bone turnover for the prediction of fracture risk and monitoring of osteoporosis treatment: a need for international reference standards. Osteoporos Int 2011; 22 (2): 391-420.
[6] Bauer D, Krege J, Lane N et al. National Bone Health Alliance Bone Turnover Marker Project: current practices and the need for US harmonization, standardization, and common reference ranges. Osteoporos Int 2012; 23 (10): 2425-2433.
[7] Camacho PM, Petak SM, Binkley N et al. AMERICAN ASSOCIATION OF CLINICAL ENDOCRINOLOGISTS/AMERICAN COLLEGE OF ENDOCRINOLOGY CLINICAL PRACTICE GUIDELINES FOR THE DIAGNOSIS AND TREATMENT OF POSTMENOPAUSAL OSTEOPOROSIS-2020 UPDATE. Endocr Pract 2020; 26 (Suppl 1): 1-46.
[8] Garnero P, Sornay-Rendu E, Duboeuf F et al. Markers of bone turnover predict postmenopausal forearm bone loss over 4 years: the OFELY study. J Bone Miner Res 1999; 14 (9): 1614-1621.
[9] Carmel AS, Shieh A, Bang H et al. The 25(OH)D level needed to maintain a favorable bisphosphonate response is ≥33 ng/ml. Osteoporos Int 2012; 23 (10): 2479-2487.
[10]Eastell R, Pigott T, Gossiel F, Naylor KE, Walsh JS, Peel NFA. DIAGNOSIS OF ENDOCRINE DISEASE: Bone turnover markers: are they clinically useful?. Eur J Endocrinol. 2018;178(1):R19-R31.
[12] Greenspan SL, Parker RA, Ferguson L et al. Early Changes in Biochemical Markers of Bone Turnover Predict the Long-Term Response to Alendronate Therapy in Representative Elderly Women: A Randomized Clinical Trial. Journal of Bone and Mineral Research 1998; 13 (9): 1431-1438
[13] Watts NB, Cooper C, Lindsay R et al. Relationship between changes in bone mineral density and vertebral fracture risk associated with risedronate: greater increases in bone mineral density do not relate to greater decreases in fracture risk. J Clin Densitom 2004; 7 (3): 255-261.
[14] Eastell R, Barton I, Hannon RA et al. Relationship of early changes in bone resorption to the reduction in fracture risk with risedronate. J Bone Miner Res 2003; 18 (6): 1051-1056.
[15] Paggiosi MA, Peel N, McCloskey E et al. Comparison of the effects of three oral bisphosphonate therapies on the peripheral skeleton in postmenopausal osteoporosis: the TRIO study. Osteoporos Int 2014; 25 (12): 2729-2741.
[16] Naylor KE, Jacques RM, Paggiosi M et al. Response of bone turnover markers to three oral bisphosphonate therapies in postmenopausal osteoporosis: the TRIO study. Osteoporos Int 2016; 27 (1): 21-31.
[17] Eastell R, Pigott T, Gossiel F et al. DIAGNOSIS OF ENDOCRINE DISEASE: Bone turnover markers: are they clinically useful Eur J Endocrinol 2018; 178 (1): R19-r31.
[16] Baim S, Miller PD. Assessing the clinical utility of serum CTX in postmenopausal osteoporosis and its use in predicting risk of osteonecrosis of the jaw. J Bone Miner Res 2009; 24 (4): 561-574.
[19] Eastell R, Szulc P. Use of bone turnover markers in postmenopausal osteoporosis. Lancet Diabetes Endocrinol 2017; 5 (11): 908-923. 2 comments

一、骨质疏松症流行病学
骨质疏松症已成为全球范围内日益严峻的公共卫生挑战。据估计,全球骨质疏松症患者已超过2亿[1],且患病率随年龄增长而显著增加[2]。一项基于美国国家健康与营养调查(NHANES)Ⅲ数据的研究[2],采用股骨颈或腰椎骨密度标准,对北美、欧洲、日本及澳大利亚等多个国家/地区的骨质疏松症患病率进行了估算。结果显示(图1),女性患病率基于股骨颈骨密度介于9%(英国)至15%(法国、德国)之间,纳入腰椎数据后扩大至16%(美国)至38%(日本)。男性患病率基于股骨颈骨密度为1%(英国)至4%(日本),纳入腰椎数据后为3%(加拿大)至8%(法国、德国、意大利、西班牙)。总体而言,上述地区符合世界卫生组织骨质疏松症诊断标准者高达4900万。

图1. 不同国家骨质疏松症患病率
骨质疏松症的核心危害在于增加脆性骨折风险,并带来沉重的疾病负担。以欧盟为例,2010年约2750万骨质疏松患者,其中新发骨折350万例,经济负担高达370亿欧元,新发骨折费用占66%,长期照护占29%,药物预防仅占5%[3]。骨折导致118万质量调整生命年损失,预计2025年相关费用再增25%。然而,绝大多数骨折患者或高骨折风险人群未接受规范治疗,且治疗率呈下降趋势。转向国内,我国形势同样严峻,目前骨质疏松症患者达1.26亿,骨量减少人群高达8.1亿,骨量减少前期状态者亦有2.1亿。但需注意的是,这一数据可能被低估,现有调查多集中于大城市,广大边远地区的筛查覆盖仍存空白。
二、骨转换标志物与诊断评估
骨转换标志物(bone turnover markers,BTM)是反映骨骼代谢动态状况的关键生化指标。具体而言,骨形成标志物如P1NP(Ⅰ型前胶原氨基端前肽)反映成骨细胞活性;骨吸收标志物如CTX(Ⅰ型胶原羧基端肽)反映破骨细胞介导的胶原降解(图2)[4]。胶原合成始于N端、降解始于C端,因此选择P1NP与CTX能够实现骨形成与骨吸收过程的“端对端”精准匹配,具有更好的机制互补性与特异性。基于此,2010年国际骨质疏松基金会(IOF)[5]推荐血清CTX与P1NP作为参考标志物;2012年美国骨健康联盟联合美国临床化学协会[6]进一步明确血清CTX为优选的骨吸收标志物,P1NP为优选的骨形成标志物。在疾病诊断和治疗过程中,至少选择一个骨形成标志物和一个骨吸收标志物[7]。

图2. 骨转换标志物种类
BTM代表全身骨骼代谢的动态状况,可预测骨丢失,反映未来骨质疏松的风险。一项前瞻性队列研究(OFELY)[8]纳入305例50~88岁的健康绝经后女性,检测基线血清骨钙素、P1NP、P1CP、BALP、CTX和尿液NTX、CTX等多项骨转换标志物,并评估其对4年内桡骨远端及中段骨密度变化的预测作用。结果显示(图3),与BTM水平较低的绝经后女性相比,BTM高于绝经前参考范围上限的患者,桡骨中段骨量流失多4~6倍,桡骨远端骨量流失多1.8~2倍。该研究证实,BTM水平升高可有效预测骨量加速流失,为临床早期识别高风险人群提供了重要依据。
BTM在鉴别诊断中具有重要价值,有助于区分不同类型骨代谢疾病。在临床实践中,若BTM水平超过参考范围上限的1.5倍,提示骨转换率明显升高,这一特征常见于新发骨折、甲状旁腺功能亢进症、多发性骨髓瘤或骨质疏松症等疾病。如下表[4]所示,表1汇总了常见代谢性骨病骨代谢生化标志物的变化特征,可为临床鉴别诊断提供重要参考依据。
表1. 常见代谢性骨病骨代谢生化标志物变化

三、骨转换标志物与治疗监测
如前所述,BTM的检测不仅有助于骨代谢疾病的鉴别诊断,还可用于监测药物疗效及治疗依从性等。值得注意的是,维生素D是抗骨质疏松治疗的基础用药,AACE/ACE绝经后骨质疏松临床实践指南[7]建议:维生素D缺乏风险人群,尤其骨质疏松患者需监测25-羟基维生素D(25OHD)水平(B级;BEL 2);骨质疏松患者应每日补充1000~2000 IU维生素D,将血清25OHD水平维持在30 ng/ml以上(A级;BEL1)。研究显示,血清维生素D水平每降低1 ng/ml,双膦酸盐的治疗反应下降5%(OR=0.95,95%CI:0.92~0.98;P=0.0006)[9]。
在明确维生素D状态后,可通过BTM降低超过最小有意义变化(LSC)或降至参考区间几何均值以下来评估治疗疗效或依从性。具体阈值如下[10]:
抗骨吸收药物治疗时,P1NP降低>10 μg/L(LSC),或降低至<35 μg/L(目标值);CTX降低>100 ng/L(LSC),或降低至<280 ng/L(目标值);
促骨形成药物治疗时,P1NP升高幅度>10 μg/L(LSC),或升高至>69 μg/L(目标值)。
在监测频率方面,临床实践中推荐每3~6个月监测一次BTM,包括P1NP、CTX、维生素D、血钙、血磷等。从变化趋势来看,抗骨吸收药物治疗后,P1NP与CTX均下降,其中CTX下降更为显著;促骨形成药物则使P1NP、CTX均上升,P1NP上升幅度更大,形成“骨形成升窗”(图4)[11-13]。

图4. 使用抗吸收治疗(紫色)和促骨形成治疗(粉色)后BTM的变化幅度均值
关于应答判断标准,判断治疗应答需关注最小有意义变化(LSC)。一项纳入172例绝经后骨质疏松妇女的开放性随机对照干预性研究(TRIO研究)[14-16],评估了3种双膦酸盐(伊班膦酸钠、阿仑膦酸钠、利塞膦酸钠)的疗效,采用BTM的两种目标反应定义进行评估:一是降至参考区间几何均值以下,二是变化超过LSC。研究结果显示,CTX下降需超过56%、P1NP下降需超过38%方可认为充分应答(图5)。无论采用哪种目标反应定义,70%~100%女性的CTX和P1NP均能达到治疗达标标准。相反,若BTM无明显变化,则提示患者依从性差或用药方法不当。
在指导序贯治疗方案方面,一项纳入161例绝经后女性的回顾性研究显示,地舒单抗停药2年的骨密度(BMD)丢失与血清Ⅰ型胶原C端肽(sCTX)升高显著相关(P<0.001),提示sCTX是预测停药后骨量丢失的有效指标;经ROC曲线分析,停药1年内将sCTX控制在正常值上限的49.1%(≈281.3 ng/L)以下,可有效预防2年后腰椎BMD丢失[17],为临床序贯治疗及病情监测提供了量化管控目标,可据此指导抗骨吸收药物序贯,有效预防停药后骨量快速反弹与丢失,降低骨折风险。
此外,BTM还可协助评估药物不良事件。地舒单抗治疗后可能出现低钙血症,基线BTM水平较高的患者更易发生,需积极补充钙+维生素D。同时,关于非典型股骨骨折与下颌骨坏死风险,有研究提出血清CTX水平低于150 ng/L时拔牙或种植牙风险可能增加,尽管这一阈值尚未形成共识,但可为临床提供参考[18]。
关于治疗选择,治疗开始前的BTM水平是否有助于选择最佳治疗方案,目前尚存争议[19]。数据显示,基线高P1NP水平与阿仑膦酸钠治疗减少非椎体骨折相关,但该关联未在其他标志物或骨折类型中得到验证;基线BTM水平与特立帕肽疗效无关;低P1NP者对唑来膦酸反应欠佳。因此,药物选择应基于骨折风险分层而非BTM水平。这表明,BTM在指导初始药物选择方面的价值有限,其核心应用仍聚焦于治疗过程中的疗效评价与依从性监测。
四、骨转换标志物的生物学变异与临床应用局限性
1. 生物学变异与检测标准化
BTM的检测结果受多种生物学因素影响,为确保检测结果的准确性,临床采样需遵循标准化流程:
采样时间与饮食:骨吸收标志物(如CTX)具有显著的昼夜节律(夜间最高,下午最低)及进餐抑制效应(早餐后下降约50%)。建议受试者隔夜禁食后,于清晨07:30-10:00采集空腹血样。
人口学因素:需考虑年龄(儿童及青春期较高,随年龄增长波动)、性别(<35岁年轻男性与绝经后女性差异)及绝经年限的影响,建议使用基于年龄和性别特异的参考区间。
生理状态:妊娠期、哺乳期及月经周期(黄体期)可导致指标波动;生活方式如吸烟(升高)、饮酒(降低)及剧烈运动(采样前1天应避免)亦需注意。
病理与药物干扰:
肝肾功能:慢性肾脏病(尤其是继发性甲旁亢或无动力性骨病)及肝脏疾病(纤维化阶段)会显著改变BTM水平;经肾脏排泄的标志物(如CTX、骨钙素)在肾功能不全时可能假性升高。
药物影响:糖皮质激素、抗惊厥药、肝素等可升高或降低BTM;钙剂与维生素D补充可能轻微降低骨转换;特定抗骨质疏松药物(如双膦酸盐、地舒单抗、特立帕肽)则会产生显著的特异性改变。
2. 临床应用的局限性与综合判读原则
尽管BTM是评估骨代谢动态变化的敏感指标,但在临床应用中存在以下局限性,需结合其他检查进行综合判读:
不能替代骨密度诊断:BTM反映的是骨转换的速率,而非骨骼的矿化程度或骨微结构。它不能替代BMD作为骨质疏松诊断的金标准。
缺乏定位特异性:BTM骨转换过程中产生的中间代谢产物或酶类,无法定位具体的局部骨病变(如单发的骨肿瘤或局部感染)。
特异性有限:BTM轻度升高缺乏疾病特异性,可见于生理波动或多种代谢性骨病(如继发性甲旁亢、多发性骨髓瘤、骨质疏松等),需结合临床背景鉴别。
综合判读原则:临床决策应遵循“BTM+BMD+临床风险因素”的综合判读模式。即结合生化标志物的动态变化、影像学的骨量评估以及患者的骨折风险因素,以实现骨质疏松症的精准管理与疗效监测。
五、结语
BTM不仅可用于骨折风险评估、鉴别诊断、疗效监测与依从性评估,还能在序贯治疗中监测病情,同时协助评价药物不良事件。检测技术的进步,为临床应用提供了可靠工具。尽管如此,临床应用中仍需注意其生物学变异及检测标准化等局限性,应结合骨密度及临床风险因素进行综合判读。
专家简介

复旦大学附属华东医院
骨质疏松科主任、医学博士、主任医师、教授、博士生导师
上海市医学会骨质疏松专科分会前任主任委员
中华医学会骨质疏松和骨矿盐疾病分会常委
中国老年保健医学研究会骨质疏松分会副主任委员
中华医学会老年医学分会骨代谢病学组副组长
复旦大学骨关节研究所副所长
参考文献
[1] Reginster JY, Burlet N. Osteoporosis: a still increasing prevalence. Bone 2006; 38 (2 Suppl 1): S4-9.
[2] Wade SW, Strader C, Fitzpatrick LA et al. Estimating prevalence of osteoporosis: examples from industrialized countries. Arch Osteoporos 2014; 9: 182.
[3] Hernlund E, Svedbom A, Iverg?rd M et al. Osteoporosis in the European Union: medical management, epidemiology and economic burden. A report prepared in collaboration with the International Osteoporosis Foundation (IOF) and the European Federation of Pharmaceutical Industry Associations (EFPIA). Arch Osteoporos 2013; 8 (1): 136.
[4] 中华医学会骨质疏松和骨矿盐疾病分会. 中华骨质疏松和骨盐疾病杂志, 2015; 8(4): 283-293.
[5] Vasikaran S, Eastell R, Bruyère O et al. Markers of bone turnover for the prediction of fracture risk and monitoring of osteoporosis treatment: a need for international reference standards. Osteoporos Int 2011; 22 (2): 391-420.
[6] Bauer D, Krege J, Lane N et al. National Bone Health Alliance Bone Turnover Marker Project: current practices and the need for US harmonization, standardization, and common reference ranges. Osteoporos Int 2012; 23 (10): 2425-2433.
[7] Camacho PM, Petak SM, Binkley N et al. AMERICAN ASSOCIATION OF CLINICAL ENDOCRINOLOGISTS/AMERICAN COLLEGE OF ENDOCRINOLOGY CLINICAL PRACTICE GUIDELINES FOR THE DIAGNOSIS AND TREATMENT OF POSTMENOPAUSAL OSTEOPOROSIS-2020 UPDATE. Endocr Pract 2020; 26 (Suppl 1): 1-46.
[8] Garnero P, Sornay-Rendu E, Duboeuf F et al. Markers of bone turnover predict postmenopausal forearm bone loss over 4 years: the OFELY study. J Bone Miner Res 1999; 14 (9): 1614-1621.
[9] Carmel AS, Shieh A, Bang H et al. The 25(OH)D level needed to maintain a favorable bisphosphonate response is ≥33 ng/ml. Osteoporos Int 2012; 23 (10): 2479-2487.
[10]Eastell R, Pigott T, Gossiel F, Naylor KE, Walsh JS, Peel NFA. DIAGNOSIS OF ENDOCRINE DISEASE: Bone turnover markers: are they clinically useful?. Eur J Endocrinol. 2018;178(1):R19-R31.
[12] Greenspan SL, Parker RA, Ferguson L et al. Early Changes in Biochemical Markers of Bone Turnover Predict the Long-Term Response to Alendronate Therapy in Representative Elderly Women: A Randomized Clinical Trial. Journal of Bone and Mineral Research 1998; 13 (9): 1431-1438
[13] Watts NB, Cooper C, Lindsay R et al. Relationship between changes in bone mineral density and vertebral fracture risk associated with risedronate: greater increases in bone mineral density do not relate to greater decreases in fracture risk. J Clin Densitom 2004; 7 (3): 255-261.
[14] Eastell R, Barton I, Hannon RA et al. Relationship of early changes in bone resorption to the reduction in fracture risk with risedronate. J Bone Miner Res 2003; 18 (6): 1051-1056.
[15] Paggiosi MA, Peel N, McCloskey E et al. Comparison of the effects of three oral bisphosphonate therapies on the peripheral skeleton in postmenopausal osteoporosis: the TRIO study. Osteoporos Int 2014; 25 (12): 2729-2741.
[16] Naylor KE, Jacques RM, Paggiosi M et al. Response of bone turnover markers to three oral bisphosphonate therapies in postmenopausal osteoporosis: the TRIO study. Osteoporos Int 2016; 27 (1): 21-31.
[17] Eastell R, Pigott T, Gossiel F et al. DIAGNOSIS OF ENDOCRINE DISEASE: Bone turnover markers: are they clinically useful Eur J Endocrinol 2018; 178 (1): R19-r31.
[16] Baim S, Miller PD. Assessing the clinical utility of serum CTX in postmenopausal osteoporosis and its use in predicting risk of osteonecrosis of the jaw. J Bone Miner Res 2009; 24 (4): 561-574.
[19] Eastell R, Szulc P. Use of bone turnover markers in postmenopausal osteoporosis. Lancet Diabetes Endocrinol 2017; 5 (11): 908-923. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言