编者按:
糖尿病管理正从“控糖中心”逐步走向“并发症预防与器官保护”。在这一转变过程中,β细胞功能及其动态变化逐渐成为关注焦点。近期北京医院郭立新/潘琦教授团队发表在Diabetes/Metabolism Research and Reviews杂志的研究结果表明[1]:内源性空腹C肽恢复与泌汗相关小纤维功能障碍进展的临床显著降低相关,且呈阈值依赖性,支持将β细胞保护/恢复作为早期糖尿病神经病变的干预靶点。该研究的第一作者为来自北京协和医学院的蔡青云博士。
β细胞功能与神经并发症的再认识
胰腺β细胞功能衰退是糖尿病进展的核心特征。C肽作为胰岛素共分泌产物,是反映β细胞功能的重要指标,在1型糖尿病中因免疫破坏显著降低,在2型糖尿病中则随病程延长逐渐下降。研究表明,C肽不仅是生物标志物,还参与糖尿病微血管并发症(如神经病变、肾病和视网膜病变)的发生发展,其缺乏可通过多种机制促进神经损伤。因此,糖尿病管理正从单纯控糖转向并发症预防与β细胞功能保护。
内源性C肽可通过生活方式及药物干预改善,外源性补充在部分研究中亦显示神经保护作用,其机制可能包括改善微循环、增强一氧化氮生成、调节Na+/K+-ATP酶活性及减轻氧化应激。糖尿病周围神经病变(DPN)累及约30%~50%患者,其中小纤维神经病变(SFN)多为早期、亚临床损伤,可通过泌汗功能障碍反映。尽管既往研究多聚焦外源性C肽及大纤维指标,关于真实世界中内源性C肽恢复对小纤维神经功能的影响仍有限。本研究基于真实世界队列,探讨C肽恢复与泌汗相关小纤维功能恶化风险的关系,以评估其临床意义。
研究设计:
真实世界队列与多维度评估
本研究为回顾性真实世界队列,纳入2020年1月至2025年9月北京医院住院的成年2型糖尿病患者。纳入年龄≥18岁且符合诊断标准,排除使用显著影响C肽分泌药物、数据不完整、非糖尿病神经病变及严重合并情况者。收集基线与随访临床资料及实验室指标,包括空腹血糖、HbA1c、空腹C肽(FCP)、血脂及肾功能等。以ΔFCP(随访减基线)反映β细胞功能变化,糖尿病肾病进展定义为eGFR下降≥30%或白蛋白尿分级进展。
神经功能评估采用Sudoscan测量电化学皮肤电导(ESC)反映泌汗相关小纤维功能(ESCF),并结合神经传导检测评估大纤维功能(SNAP、SNCV)。以指标变化及最小可测变化(MDC)判定功能恶化,并结合最差15%变化定义进展。统计分析按ΔFCP三分位分组,采用Kaplan–Meier曲线和Cox模型评估其与泌汗功能恶化的关系,并通过样条分析、阈值分析、亚组、敏感性及中介分析验证结果的稳健性及潜在机制。
288例患者按ΔFCP分为三分位组(Q1最低、Q2中等、Q3最高),各组在年龄、性别、糖尿病病程、BMI、血压等方面总体相似,但部分代谢与肾功能指标存在差异:Q1组空腹血糖(FBG)和甘油三酯(TG)较高;Q2组高密度脂蛋白(HDL-C)和eGFR最高,同时TG和尿素最低;基线C肽(FCP)水平在三组间差异显著,Q2最低,Q1与Q3较高。各组糖尿病并发症(DPN、DKD、DR)患病率及降糖治疗情况无显著差异。
随访期间,仅泌汗相关小纤维功能结局与ΔFCP显著相关(P=0.038)(图1A);大纤维神经病变和DKD在不同分组间无显著差异(均P>0.05)(图1B/1C),提示ΔFCP的预后价值具有终点特异性,且泌汗功能指标较神经传导指标更敏感。
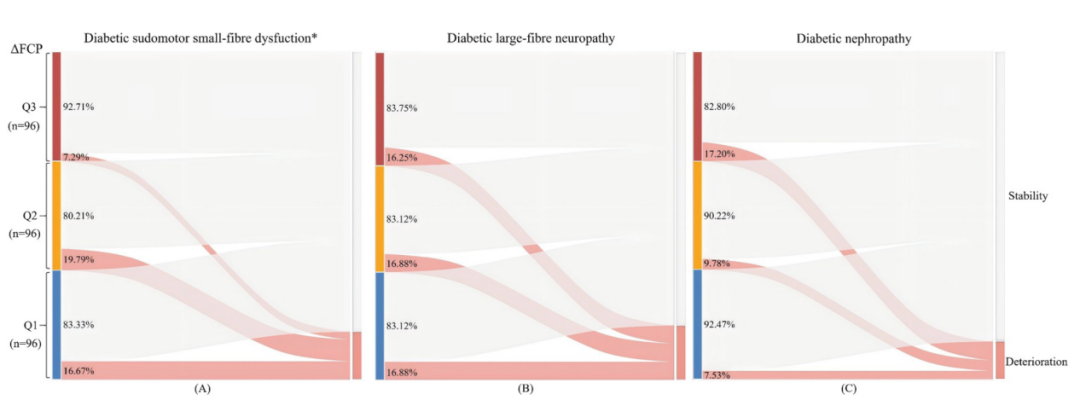
图1.按ΔFCP三分位分组的泌汗相关小纤维功能障碍(A)、LFN(B)及DKD(C)进展情况的Sankey(桑基图)。(红色带表示功能恶化,浅色带表示功能稳定。图中百分比表示各ΔFCP分组内发生相应结局的患者比例。)
二、ΔFCP与小纤维神经损伤风险的关联
Kaplan–Meier分析显示,不同ΔFCP三分位组的泌汗相关小纤维结局曲线明显分离,Q3组累积恶化发生率最低,Q1组最高(log-rank P<0.01)(图2A);而LFN及DKD曲线无显著差异(均P>0.05)。
多变量Cox回归(校正年龄、性别、BMI、糖尿病病程、吸烟、饮酒、HbA1c及高血压)结果显示,与Q1组相比,Q3组泌汗功能恶化风险显著降低(HR=0.16,95%CI:0.05~0.47,P<0.001),而Q2组与Q1组无显著差异(均P>0.05)(图2B)。采用相同校正模型,未发现ΔFCP三分位与LFN或DKD进展风险存在显著关联。
三、阈值效应:
非线性关系与最佳临界值
将ΔFCP作为连续变量纳入限制性立方样条分析,其与小纤维神经恶化风险存在显著整体关联(P=0.016),但呈非线性趋势。曲线显示,在中等ΔFCP水平附近穿越无效线,低于该水平时风险下降不明显,而超过该范围后风险明显降低;非线性检验P=0.086,虽未达统计学意义,但整体模式符合阈值效应而非线性剂量反应。
最大秩统计法确定最佳阈值为126.8 pmol/L。以此分组后,ΔFCP≥126.8 pmol/L患者小纤维神经恶化风险显著降低(HR=0.22,95%CI:0.09~0.54,P<0.001),Kaplan–Meier曲线明显分离(log-rank P=0.002),提示该阈值具有明确的临床意义。
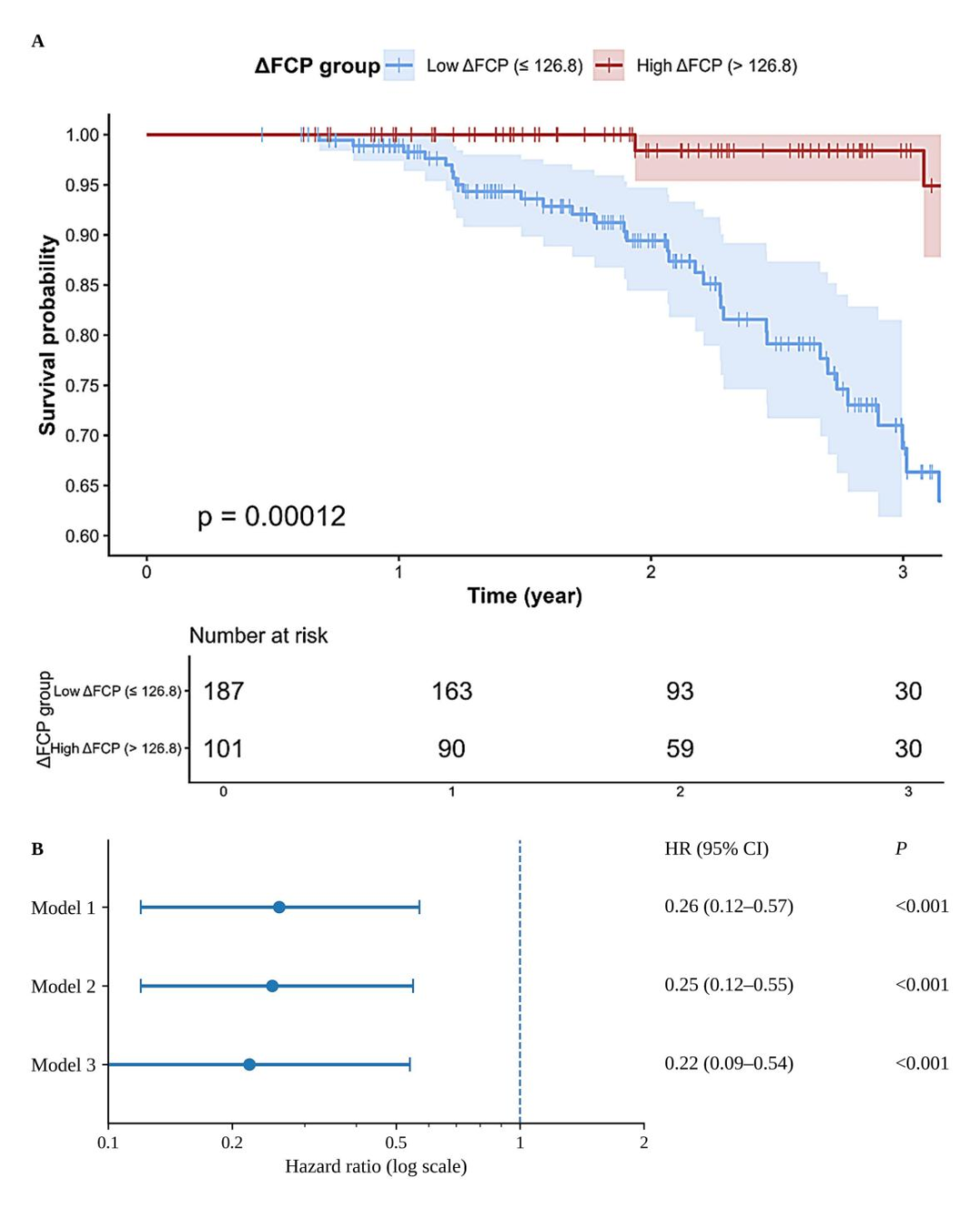
图2.(A)Kaplan–Meier曲线显示3年随访期间泌汗功能恶化的发生时间,按ΔFC=126.8pmol/L分组。实线表示估计的生存概率(即发生恶化的概率),阴影区域表示95%置信区间;刻度线表示删失数据。
(B)ΔFCP二分组与泌汗功能恶化风险的多变量Cox比例风险模型分析(以ΔFCP≤126.8poml/L为参照组)模型1为未校正模型;模型2校正年龄、性别和BMI;模型3在此基础上进一步校正糖尿病病程、吸烟、饮酒、HbA1c及高血压。图中点表示风险比(HR),横线表示95%置信区间。
四、时间依赖性与亚组分析:高风险人群获益更显著
比例风险假设检验显示,ΔFCP的保护效应具有时间依赖性(P=0.040)。在1年界标分析中(纳入1年无事件者),ΔFCP≥126.8 pmol/L仍显著降低后续风险(HR=0.33,95%CI 0.17~0.67,P=0.003),提示保护效应在随访后期仍然存在。
亚组分析显示,该保护作用在性别、年龄、肥胖、糖尿病病程及血糖控制等分层中均一致(交互P>0.05)。但在高风险人群中效应更强:DPN患者(HR=0.16,P=0.001;交互P=0.031)、高血压患者(HR=0.09,P<0.001;交互P=0.005)、心血管疾病患者(HR=0.11,P=0.002)、DKD患者(HR=0.07,P=0.002)及DR患者(HR=0.14,P=0.021)均表现出更强保护效应(图3)。
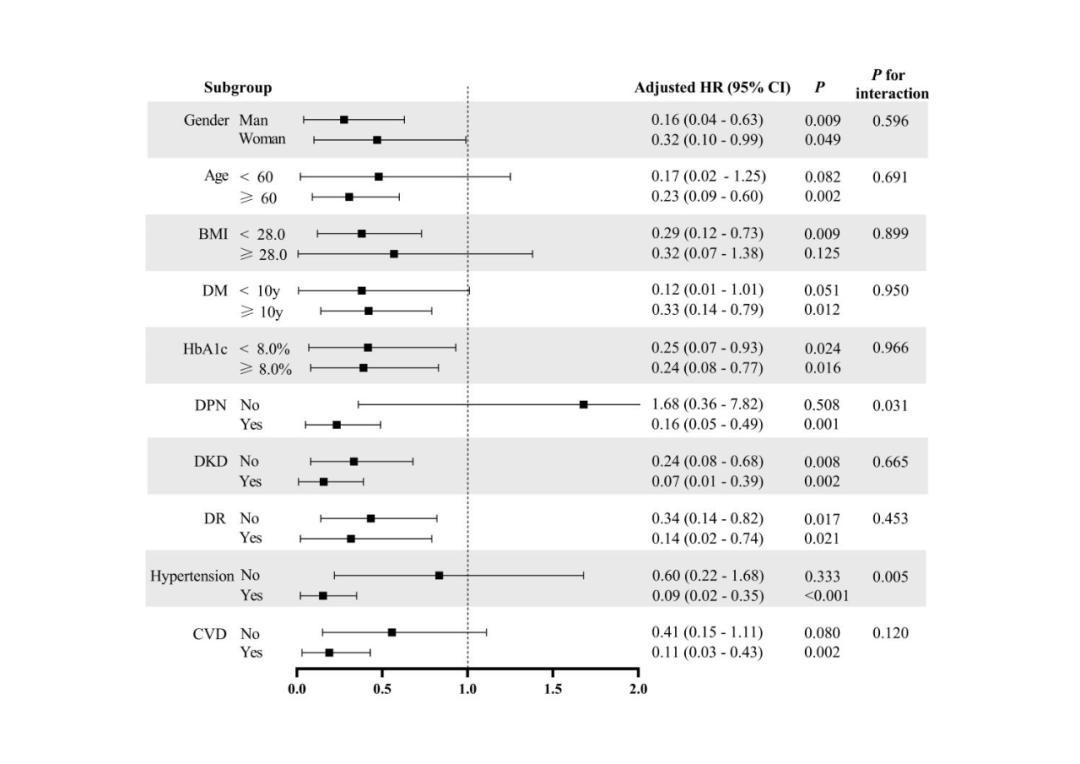
图3. 高△FCP(>126.8pmol/L)与泌汗相关小纤维神经功能恶化风险的亚组分析,垂直虚线标识HR = 1.0。HR通过Cox比例风险模型计算,调整协变量包括年龄、性别、BMI、糖尿病病程、吸烟状况、饮酒情况、HbA1c和高血压。
五、稳健性验证与中介分析
敏感性分析结果一致:无论采用25%或10%分位重新定义结局,或以ESCF下降≥75%/≥90%界定恶化,高ΔFCP均显示稳定保护作用(HR=0.42,P=0.002;HR=0.29,P=0.003),且Weibull模型结果与Cox模型一致(HR=0.356,P=0.003),提示结论稳健。中介分析显示,基线FCP仅解释约2%的效应,而约98%来自ΔFCP本身(HR=0.23,P=0.002),表明其保护作用基本独立于基线β细胞功能。
研究讨论
机制解释和临床意义
本研究的核心发现是:内源性C肽恢复与小纤维神经功能保护密切相关,且这种关系具有明确的阈值特征,并在高风险人群中更为显著。这一发现从临床角度支持了“β细胞保护”的重要性。从机制上看,小纤维神经对微循环和代谢环境变化更为敏感。C肽通过改善血管内皮功能、增加局部血流、降低氧化应激等作用,可能优先影响这些神经结构。而大纤维神经及肾脏损伤更多涉及结构性改变,可能需要更长期或不同机制的干预,因此在本研究较短随访中未观察到显著效果 。
本研究结果对临床实践及未来治疗策略具有重要启示:1)首先,支持2型糖尿病管理从单纯控糖转向更加重视β细胞功能的保护与恢复,将其纳入并发症预防的重要目标。尽管目前证据尚不足以将ΔFCP 126.8 pmol/L作为常规治疗靶值,但在特定人群(尤其已合并糖尿病并发症或心血管代谢合并症者)中,追求“有意义的C肽恢复”而非仅避免进一步下降,具有潜在临床价值。2)其次,联合应用Sudoscan等快速、无创工具动态监测泌汗相关小纤维功能及C肽变化,有助于识别对β细胞保护策略有反应的患者,并及时调整治疗方案。3)最后,本研究亦为未来干预研究提供依据,即需进一步验证通过改善β细胞功能的策略(如早期联合治疗、减重、代谢手术及新型β细胞靶向药物),在以C肽恢复为直接目标时,是否能够因果性地延缓或改变泌汗相关小纤维功能障碍的进展。
当然,研究也存在局限性,包括单中心回顾性设计、未测量刺激C肽以及未采用皮肤活检等结构性指标。但多种统计方法及敏感性分析结果一致,增强了结论的可靠性。
结语
综上,在该真实世界队列中,内源性C肽恢复与泌汗相关小纤维功能恶化风险显著降低相关,且超过一定阈值时保护作用更为明显,尤其在高风险人群中获益更大。该效应具有小纤维终点特异性,独立于基线C肽水平,并可持续至随访1年以后。结果支持将β细胞保护与恢复作为早期糖尿病神经病变的潜在干预方向,未来仍需前瞻性研究进一步验证其因果关系并明确临床目标。
参考文献:
1.Cai Q, Xie T, Gong H, Zhang W, Guo L, Pan Q. Endogenous Recovery of Fasting C-Peptide Decreases Progression of Sudomotor Small-Fibre Dysfunction in Adults With Diabetes: A Real-World Cohort Study. Diabetes Metab Res Rev. 2026 May;42(4):e70173. doi: 10.1002/dmrr.70173. PMID: 42047412; PMCID: PMC13123299. 2 comments
糖尿病管理正从“控糖中心”逐步走向“并发症预防与器官保护”。在这一转变过程中,β细胞功能及其动态变化逐渐成为关注焦点。近期北京医院郭立新/潘琦教授团队发表在Diabetes/Metabolism Research and Reviews杂志的研究结果表明[1]:内源性空腹C肽恢复与泌汗相关小纤维功能障碍进展的临床显著降低相关,且呈阈值依赖性,支持将β细胞保护/恢复作为早期糖尿病神经病变的干预靶点。该研究的第一作者为来自北京协和医学院的蔡青云博士。

β细胞功能与神经并发症的再认识
胰腺β细胞功能衰退是糖尿病进展的核心特征。C肽作为胰岛素共分泌产物,是反映β细胞功能的重要指标,在1型糖尿病中因免疫破坏显著降低,在2型糖尿病中则随病程延长逐渐下降。研究表明,C肽不仅是生物标志物,还参与糖尿病微血管并发症(如神经病变、肾病和视网膜病变)的发生发展,其缺乏可通过多种机制促进神经损伤。因此,糖尿病管理正从单纯控糖转向并发症预防与β细胞功能保护。
内源性C肽可通过生活方式及药物干预改善,外源性补充在部分研究中亦显示神经保护作用,其机制可能包括改善微循环、增强一氧化氮生成、调节Na+/K+-ATP酶活性及减轻氧化应激。糖尿病周围神经病变(DPN)累及约30%~50%患者,其中小纤维神经病变(SFN)多为早期、亚临床损伤,可通过泌汗功能障碍反映。尽管既往研究多聚焦外源性C肽及大纤维指标,关于真实世界中内源性C肽恢复对小纤维神经功能的影响仍有限。本研究基于真实世界队列,探讨C肽恢复与泌汗相关小纤维功能恶化风险的关系,以评估其临床意义。
研究设计:
真实世界队列与多维度评估
本研究为回顾性真实世界队列,纳入2020年1月至2025年9月北京医院住院的成年2型糖尿病患者。纳入年龄≥18岁且符合诊断标准,排除使用显著影响C肽分泌药物、数据不完整、非糖尿病神经病变及严重合并情况者。收集基线与随访临床资料及实验室指标,包括空腹血糖、HbA1c、空腹C肽(FCP)、血脂及肾功能等。以ΔFCP(随访减基线)反映β细胞功能变化,糖尿病肾病进展定义为eGFR下降≥30%或白蛋白尿分级进展。
神经功能评估采用Sudoscan测量电化学皮肤电导(ESC)反映泌汗相关小纤维功能(ESCF),并结合神经传导检测评估大纤维功能(SNAP、SNCV)。以指标变化及最小可测变化(MDC)判定功能恶化,并结合最差15%变化定义进展。统计分析按ΔFCP三分位分组,采用Kaplan–Meier曲线和Cox模型评估其与泌汗功能恶化的关系,并通过样条分析、阈值分析、亚组、敏感性及中介分析验证结果的稳健性及潜在机制。
研究结果
288例患者按ΔFCP分为三分位组(Q1最低、Q2中等、Q3最高),各组在年龄、性别、糖尿病病程、BMI、血压等方面总体相似,但部分代谢与肾功能指标存在差异:Q1组空腹血糖(FBG)和甘油三酯(TG)较高;Q2组高密度脂蛋白(HDL-C)和eGFR最高,同时TG和尿素最低;基线C肽(FCP)水平在三组间差异显著,Q2最低,Q1与Q3较高。各组糖尿病并发症(DPN、DKD、DR)患病率及降糖治疗情况无显著差异。
随访期间,仅泌汗相关小纤维功能结局与ΔFCP显著相关(P=0.038)(图1A);大纤维神经病变和DKD在不同分组间无显著差异(均P>0.05)(图1B/1C),提示ΔFCP的预后价值具有终点特异性,且泌汗功能指标较神经传导指标更敏感。

图1.按ΔFCP三分位分组的泌汗相关小纤维功能障碍(A)、LFN(B)及DKD(C)进展情况的Sankey(桑基图)。(红色带表示功能恶化,浅色带表示功能稳定。图中百分比表示各ΔFCP分组内发生相应结局的患者比例。)
二、ΔFCP与小纤维神经损伤风险的关联
Kaplan–Meier分析显示,不同ΔFCP三分位组的泌汗相关小纤维结局曲线明显分离,Q3组累积恶化发生率最低,Q1组最高(log-rank P<0.01)(图2A);而LFN及DKD曲线无显著差异(均P>0.05)。
多变量Cox回归(校正年龄、性别、BMI、糖尿病病程、吸烟、饮酒、HbA1c及高血压)结果显示,与Q1组相比,Q3组泌汗功能恶化风险显著降低(HR=0.16,95%CI:0.05~0.47,P<0.001),而Q2组与Q1组无显著差异(均P>0.05)(图2B)。采用相同校正模型,未发现ΔFCP三分位与LFN或DKD进展风险存在显著关联。
三、阈值效应:
非线性关系与最佳临界值
将ΔFCP作为连续变量纳入限制性立方样条分析,其与小纤维神经恶化风险存在显著整体关联(P=0.016),但呈非线性趋势。曲线显示,在中等ΔFCP水平附近穿越无效线,低于该水平时风险下降不明显,而超过该范围后风险明显降低;非线性检验P=0.086,虽未达统计学意义,但整体模式符合阈值效应而非线性剂量反应。
最大秩统计法确定最佳阈值为126.8 pmol/L。以此分组后,ΔFCP≥126.8 pmol/L患者小纤维神经恶化风险显著降低(HR=0.22,95%CI:0.09~0.54,P<0.001),Kaplan–Meier曲线明显分离(log-rank P=0.002),提示该阈值具有明确的临床意义。

图2.(A)Kaplan–Meier曲线显示3年随访期间泌汗功能恶化的发生时间,按ΔFC=126.8pmol/L分组。实线表示估计的生存概率(即发生恶化的概率),阴影区域表示95%置信区间;刻度线表示删失数据。
(B)ΔFCP二分组与泌汗功能恶化风险的多变量Cox比例风险模型分析(以ΔFCP≤126.8poml/L为参照组)模型1为未校正模型;模型2校正年龄、性别和BMI;模型3在此基础上进一步校正糖尿病病程、吸烟、饮酒、HbA1c及高血压。图中点表示风险比(HR),横线表示95%置信区间。
四、时间依赖性与亚组分析:高风险人群获益更显著
比例风险假设检验显示,ΔFCP的保护效应具有时间依赖性(P=0.040)。在1年界标分析中(纳入1年无事件者),ΔFCP≥126.8 pmol/L仍显著降低后续风险(HR=0.33,95%CI 0.17~0.67,P=0.003),提示保护效应在随访后期仍然存在。
亚组分析显示,该保护作用在性别、年龄、肥胖、糖尿病病程及血糖控制等分层中均一致(交互P>0.05)。但在高风险人群中效应更强:DPN患者(HR=0.16,P=0.001;交互P=0.031)、高血压患者(HR=0.09,P<0.001;交互P=0.005)、心血管疾病患者(HR=0.11,P=0.002)、DKD患者(HR=0.07,P=0.002)及DR患者(HR=0.14,P=0.021)均表现出更强保护效应(图3)。

图3. 高△FCP(>126.8pmol/L)与泌汗相关小纤维神经功能恶化风险的亚组分析,垂直虚线标识HR = 1.0。HR通过Cox比例风险模型计算,调整协变量包括年龄、性别、BMI、糖尿病病程、吸烟状况、饮酒情况、HbA1c和高血压。
五、稳健性验证与中介分析
敏感性分析结果一致:无论采用25%或10%分位重新定义结局,或以ESCF下降≥75%/≥90%界定恶化,高ΔFCP均显示稳定保护作用(HR=0.42,P=0.002;HR=0.29,P=0.003),且Weibull模型结果与Cox模型一致(HR=0.356,P=0.003),提示结论稳健。中介分析显示,基线FCP仅解释约2%的效应,而约98%来自ΔFCP本身(HR=0.23,P=0.002),表明其保护作用基本独立于基线β细胞功能。
研究讨论
机制解释和临床意义
本研究的核心发现是:内源性C肽恢复与小纤维神经功能保护密切相关,且这种关系具有明确的阈值特征,并在高风险人群中更为显著。这一发现从临床角度支持了“β细胞保护”的重要性。从机制上看,小纤维神经对微循环和代谢环境变化更为敏感。C肽通过改善血管内皮功能、增加局部血流、降低氧化应激等作用,可能优先影响这些神经结构。而大纤维神经及肾脏损伤更多涉及结构性改变,可能需要更长期或不同机制的干预,因此在本研究较短随访中未观察到显著效果 。
本研究结果对临床实践及未来治疗策略具有重要启示:1)首先,支持2型糖尿病管理从单纯控糖转向更加重视β细胞功能的保护与恢复,将其纳入并发症预防的重要目标。尽管目前证据尚不足以将ΔFCP 126.8 pmol/L作为常规治疗靶值,但在特定人群(尤其已合并糖尿病并发症或心血管代谢合并症者)中,追求“有意义的C肽恢复”而非仅避免进一步下降,具有潜在临床价值。2)其次,联合应用Sudoscan等快速、无创工具动态监测泌汗相关小纤维功能及C肽变化,有助于识别对β细胞保护策略有反应的患者,并及时调整治疗方案。3)最后,本研究亦为未来干预研究提供依据,即需进一步验证通过改善β细胞功能的策略(如早期联合治疗、减重、代谢手术及新型β细胞靶向药物),在以C肽恢复为直接目标时,是否能够因果性地延缓或改变泌汗相关小纤维功能障碍的进展。
当然,研究也存在局限性,包括单中心回顾性设计、未测量刺激C肽以及未采用皮肤活检等结构性指标。但多种统计方法及敏感性分析结果一致,增强了结论的可靠性。
结语
综上,在该真实世界队列中,内源性C肽恢复与泌汗相关小纤维功能恶化风险显著降低相关,且超过一定阈值时保护作用更为明显,尤其在高风险人群中获益更大。该效应具有小纤维终点特异性,独立于基线C肽水平,并可持续至随访1年以后。结果支持将β细胞保护与恢复作为早期糖尿病神经病变的潜在干预方向,未来仍需前瞻性研究进一步验证其因果关系并明确临床目标。
参考文献:
1.Cai Q, Xie T, Gong H, Zhang W, Guo L, Pan Q. Endogenous Recovery of Fasting C-Peptide Decreases Progression of Sudomotor Small-Fibre Dysfunction in Adults With Diabetes: A Real-World Cohort Study. Diabetes Metab Res Rev. 2026 May;42(4):e70173. doi: 10.1002/dmrr.70173. PMID: 42047412; PMCID: PMC13123299. 2 comments








 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言