编者按:胰岛素的发现,堪称二十世纪医学史上重大的里程碑——它让糖尿病从无药可救的绝症,转变为可被长期管理的慢性疾病。过去一个世纪,伴随着对糖尿病认知的深化和生物制药技术的迭代,胰岛素经历了从动物粗提物,到精密模拟生理分泌的类似物,乃至迈向具备“智能响应”功能的创新制剂的历史性演进。本文将系统梳理胰岛素百年发展的关键节点,分析当前治疗路径,并前瞻未来方向,旨在为关注该领域的医患群体、产业界及公共卫生决策者,提供一份系统而前瞻的参考。
百年演进:从奇迹发现到科学基石
在胰岛素诞生前,人类对糖尿病的认知长期停滞于表象观察。古埃及已有关于多尿症状的记载,古希腊文献中亦可见类似描述,但这些观察均未能触及疾病的本质[1,2]。直至19世纪,德国学者Paul Langerhans在胰腺中发现独特细胞团簇(后称“胰岛”),首次为糖尿病研究锚定了解剖学靶点[3]。随后的动物实验进一步证实:胰腺分泌着维系血糖平衡的关键物质,而其缺乏直接导致糖尿病[4]。至此,科学探索的焦点凝聚于如何提取这一神秘物质。
1921年,班廷成功从狗胰腺中提取出具有生物活性的胰岛素物质[5]。其后,生物化学家James Collip对对提取物进行精制纯化,使其得以安全用于人体[6]。1922年,该胰岛素被应用于一名14岁的1型糖尿病患者Leonard Thompson,其危重的高血糖与酮症得到奇迹般逆转——这标志着现代糖尿病治疗纪元的正式开启。
2、超越治疗:胰岛素带来的多重科学革命
从动物胰腺提取物起步,胰岛素经历了百年演进,历经基因工程合成的人胰岛素,逐步发展出速效、长效、预混及超长效类似物,并进一步实现了每周一次给药的基础胰岛素周制剂,每一步都标志着药学技术与治疗理念的跃升。
胰岛素演进从根本上重塑了代谢领域。它不仅精准揭示了胰岛素绝对或相对缺乏是糖尿病病理生理的核心[7],还通过阐明其对糖、脂肪、蛋白质代谢的调节机制(图1),奠定了现代代谢研究的基石。
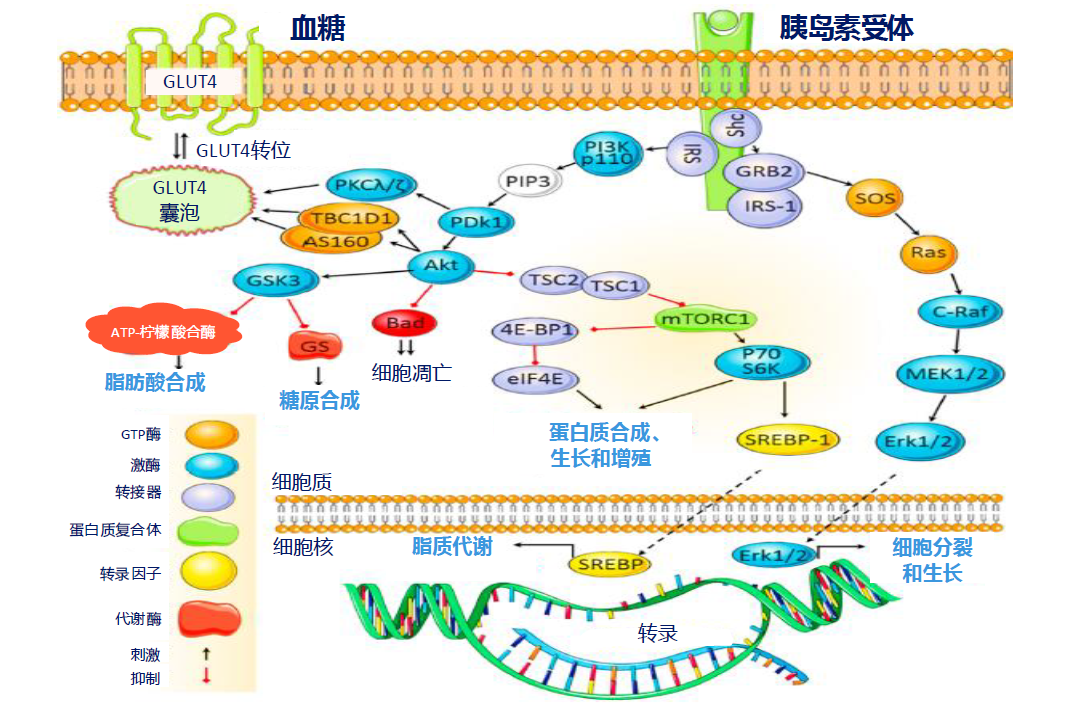
图1. 胰岛素与糖、蛋白、脂肪代谢
同时,一系列大型临床研究对胰岛素治疗的探索,促进了糖尿病管理理念的持续发展(图2)。例如,DCCT/EDIC研究证实,早期强化胰岛素治疗可带来长期获益[8]。UKPDS研究证实了新诊断2型糖尿病(T2DM)患者早期强化治疗可带来长期并发症获益[9]。这些研究开创了以长期硬终点为导向的循证实践范式,引领现代医学进入以高质量证据为决策核心的循证时代[10]。
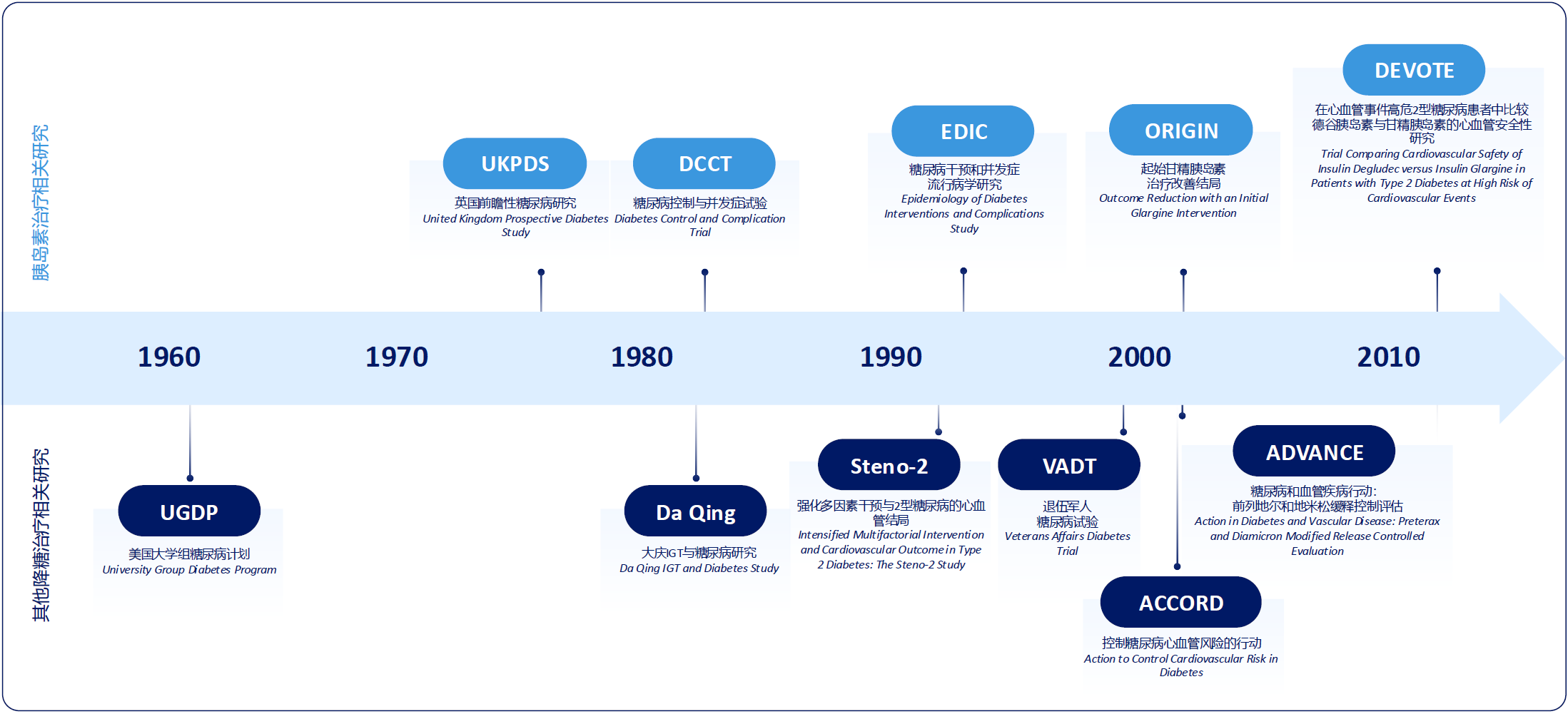
图2. 胰岛素治疗相关的循证研究
彭永德教授曾在学术会议上提到,现代胰岛素治疗的核心目标是精准模拟人体生理性胰岛素分泌模式。在生理状态下,胰岛素分泌呈现两种基本模式:基础分泌以持续、低速率的胰岛素释放,抑制肝脏葡萄糖输出,维持空腹血糖稳定;餐时脉冲分泌则在进食后迅速大量释放胰岛素,促进葡萄糖利用与储存,从而有效控制餐后血糖升高(图3)。

图3. 生理胰岛素分泌模式
为了模拟这一理想状态,胰岛素研发长期围绕“基础-餐时胰岛素”方案不断演进,形成了一套多维度、系统化的现代治疗策略。
1、基础胰岛素的持续革新
基础胰岛素的发展史,是一部向更持久、更平稳、更贴近生理方向演进的技术革新史。早期使用的中效胰岛素(如NPH)存在明显的药效峰值,易引发夜间低血糖风险。随着分子修饰技术的突破,第一代长效类似物(如地特胰岛素)实现了无峰值的平稳释放,显著降低了低血糖发生率。新一代超长效类似物(如德谷胰岛素)通过结构优化与制剂创新,进一步将作用时间延长至30~42小时,为血糖控制提供了更平稳、更持久的解决方案[13]。
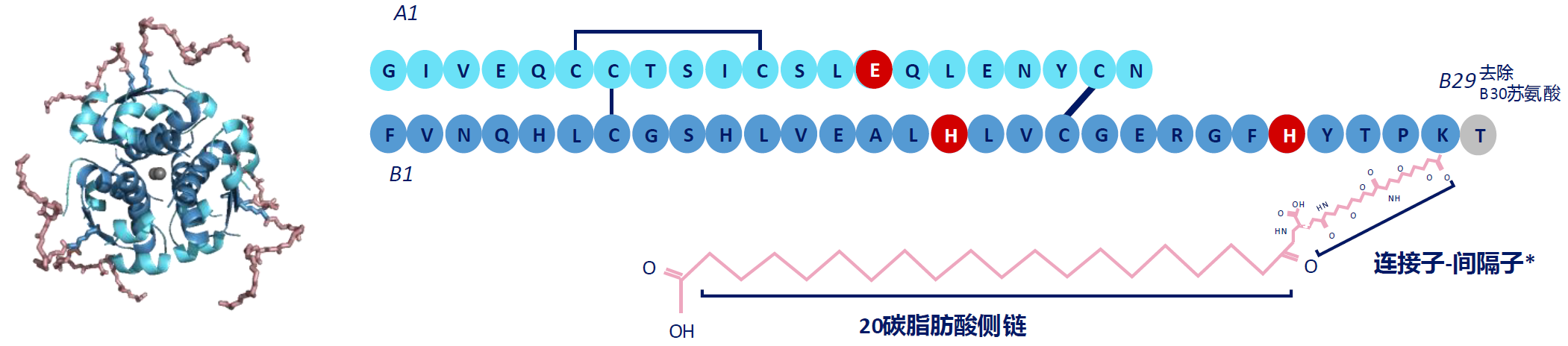
最具里程碑意义的突破是基础胰岛素周制剂——依柯胰岛素的问世。其通过脂肪酸酰化技术显著延长半衰期达196小时,实现了每周一次给药的革命性跨越(图4)。这一突破将患者全年的基础胰岛素注射次数从365次减少至约52次,不仅极大减轻治疗负担、提高依从性,也为糖尿病长期管理提供了更人性化、更贴近生理节律的治疗选择[14,15]。
2、餐时胰岛素的快速匹配
餐时胰岛素的进化方向是不断缩短起效时间,以更好地匹配餐后快速上升的血糖水平。传统的短效人胰岛素需在餐前30分钟注射,而新一代速效胰岛素类似物,如门冬胰岛素,将起效时间缩短至10~15分钟,可实现餐前即刻甚至餐后立即注射。这不仅为患者提供了更灵活的生活方式,也有助于减少迟发性低血糖的发生风险。
3、复合制剂的简化策略
为在疗效与便捷性之间取得平衡,预混胰岛素和双胰岛素类似物应运而生。这类制剂通过两种方式简化治疗方案:一是将基础与餐时胰岛素按固定比例预先混合(如预混门冬胰岛素30);二是利用创新技术使基础与餐时成分在注射后独立发挥各自作用(如德谷门冬双胰岛素)。这两种设计均在减少每日注射次数的同时,实现对空腹及餐后血糖的双重控制,特别适用于仍保留部分胰岛素分泌功能的T2DM患者。
4、联合治疗的协同强化
针对T2DM复杂的病理生理机制,胰岛素联合其他作用机制的药物已成为核心优化策略[16]。例如,胰岛素和胰高糖素样肽-1受体激动剂(GLP-1RA)的联合应用:胰岛素直接补充内源性胰岛素分泌不足,降低空腹血糖;而GLP-1RA则以葡萄糖浓度依赖性方式促进胰岛素分泌、抑制胰高血糖素释放、延缓胃排空,从而在控制餐后血糖、减轻体重及心血管保护方面发挥协同作用[17]。
5、技术赋能的个体化管理
现代监测与管理技术提高了胰岛素治疗的精细化管理。持续葡萄糖监测(CGM)通过提供实时、全面的葡萄糖图谱,推动治疗从经验推断转向数据驱动。胰岛素泵与CGM联动的混合闭环系统,能够根据血糖读数自动调节基础胰岛素输注率,已初步实现“人工胰腺”功能[18]。同时,数字化管理平台与应用程序通过整合胰岛素剂量、血糖、饮食、运动等多维数据,构建起支持远程指导、医患协同与自我管理的智能生态系统[19],进一步推动糖尿病管理的现代化与智能化发展。
综上所述,现代胰岛素治疗已超越早期简单的替代补充理念,发展成为一套集生理模拟精准化、制剂方案个性化、治疗机制协同化、管理手段智能化于一体的高度整合模式。这一演进不仅显著提升血糖控制的安全性、有效性及患者依从性,更从根本上改善糖尿病患者的生活质量与远期预后,同时为迈向更理想、更智慧的糖尿病管理新时代奠定了坚实基础。
尽管已取得显著成就,当前胰岛素治疗仍面临几项关键挑战:进一步降低低血糖风险、提升患者生活质量、更精准地模拟生理性胰岛素分泌模式以及提高治疗可及性与经济性。目前的研究与开发正围绕这些核心问题持续推进,旨在为糖尿病患者带来更安全、更便捷、更符合生理且更具成本效益的治疗方案。
1、联合治疗:从协同增效到病理根源干预
目前,胰岛素周制剂与GLP-1RA周制剂的联合制剂正处于研发阶段。此类联合制剂通过机制互补,协同调控血糖与体重(图5),有望实现“双周一次”或“每月一次”的超长效给药方案,从而显著简化治疗流程、减轻患者负担,并进一步提升治疗依从性。
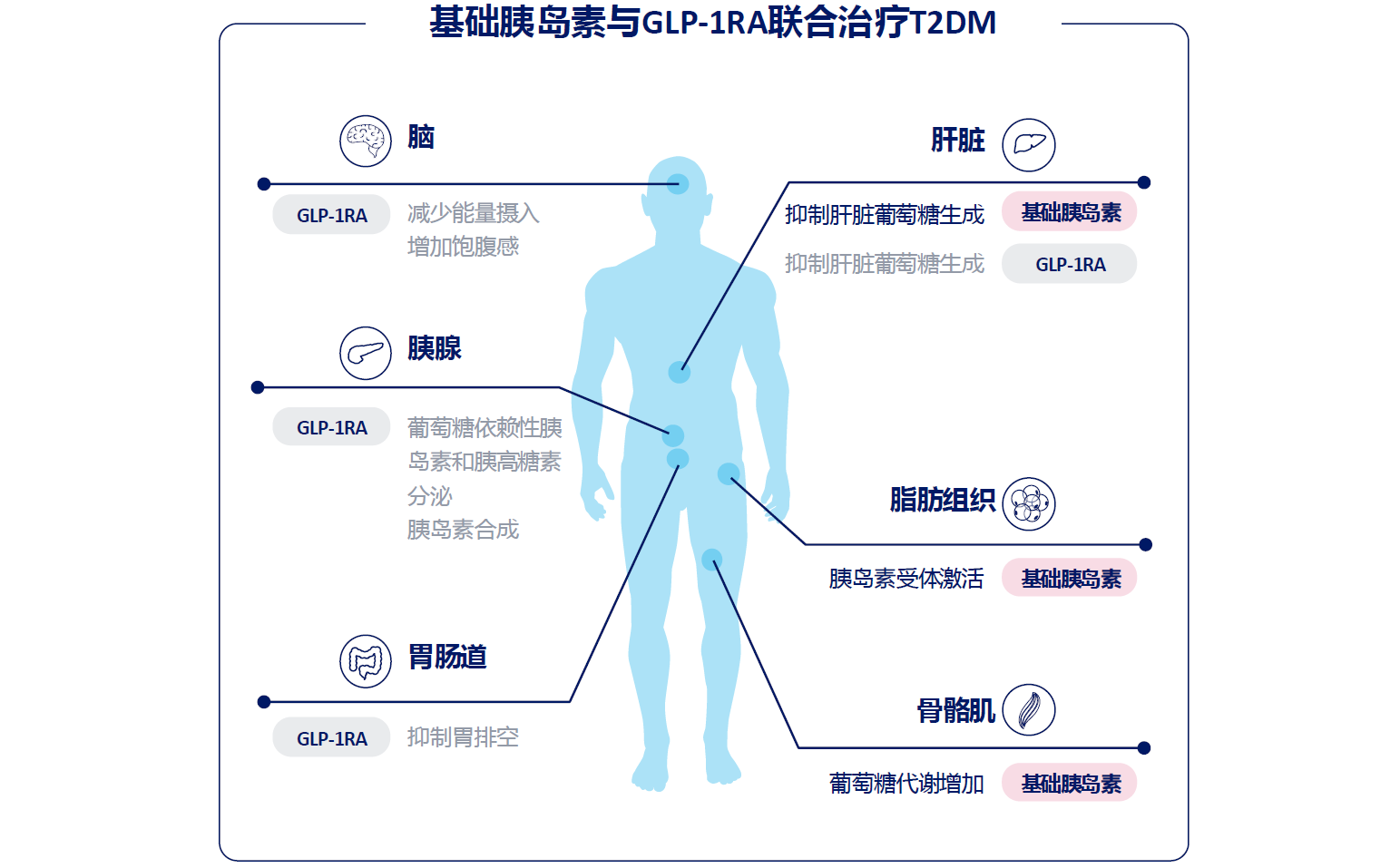
图5. 基础胰岛素与GLP-1RA的协同作用
更前沿的研究正探索以胰岛素为核心,联合作用于胰岛素抵抗、慢性炎症、代谢相关脂肪性肝病、β细胞功能保护及凋亡抑制等多重病理生理环节的创新治疗方案。此类多靶点、多维度的联合策略,旨在从疾病根源进行干预,不仅追求血糖稳定控制,更致力于实现机体长期代谢稳态的重建,从而为T2DM功能性逆转提供潜在可能[20]。
2、更便捷的给药:口服胰岛素
口服胰岛素因其无创便捷、可模拟生理性门静脉输注途径等优势,长期以来被视为糖尿病药物治疗的理想选择,但其发展面临多重生物学障碍:胃内酸性环境易导致胰岛素变性失活,肠道中丰富的蛋白酶可快速降解其肽链结构,而肠上皮紧密连接及胰岛素分子本身的亲水性也严重限制了其跨膜吸收,导致口服生物利用度普遍低于1%[21]。
为克服这些屏障,研究已取得一系列进展:通过脂质体、纳米粒等包埋技术及肠溶包衣策略保护胰岛素免受胃肠道环境破坏;利用渗透促进剂和细胞穿透肽增强其在肠道黏膜的透过性;并开发肠道微针胶囊、仿生载体系统等新型递送技术以提升靶向吸收效率[22]。
尽管目前尚无口服胰岛素产品成功实现大规模商业化应用,但随着制剂工程与纳米递送技术的持续进步,这一更具生理贴合性、用药更便利的治疗方案正逐步从科学理想迈向临床现实。
3、更智能的胰岛素:葡萄糖敏感性胰岛素
葡萄糖敏感性胰岛素的核心机制是在胰岛素分子结构中引入可感应葡萄糖浓度的“分子开关”。例如,候选分子NNC2215在血糖升高时,其分子构象发生改变,增强与胰岛素受体的结合能力,从而促进降糖作用;当血糖降低时,分子开关“关闭”,减弱其生物活性,进而显著降低低血糖风险[23]。
这类智能胰岛素分子能够更贴近生理性胰岛素分泌的动态调节模式,有望实现更安全、更自主的血糖管理,代表了胰岛素疗法向仿生智能化方向演进的重要趋势。
4、更整合的系统:数字化与闭环生态系统
未来的糖尿病管理将是一个高度整合的数字化生态系统。这不仅仅是设备的连接,更是数据、算法和服务的深度融合[24]。高级混合闭环及全闭环系统将搭载更智能的算法,实现餐食、运动等日常代谢扰动的自动识别与响应,推动血糖调节走向全自动化。人工智能与大数据技术将应用于血糖趋势预测、个性化胰岛素剂量调整与生活方式指导,并可提前预警高低血糖风险。基于云平台的虚拟照护与远程医疗系统,能够实现患者实时数据与医疗团队的无缝共享,打破地理限制,支持远程监测、即时干预与个体化指导,从而系统性提升糖尿病管理的效率、质量与可及性。
创新·超越·未来:胰岛素的百年征程
胰岛素的百年历程,是一部从绝望中诞生希望、在探索中实现超越、于创新中定义未来的医学史诗。它从一个挽救生命的简单提取物,成长为驱动蛋白质科学和生物技术革命的引擎,持续推动糖尿病管理理念的每一次突破。
今天,周制剂重塑了治疗便捷性的标准,CGM与智能算法正将管理推向精准化。展望未来,葡萄糖敏感性胰岛素、口服制剂和智能化闭环系统,将共同开启一个更安全、更自主、更智能的糖尿病管理新时代。
站在新百年的起点,胰岛素的故事仍在继续——它以持续创新的生命力,为数亿患者照亮通往更健康、更自主生活的道路,生动诠释着医学守护人类健康的永恒使命。
参考文献
1. Mohajan, Devajit (2023): Historical View of Diabetics Mellitus: From Ancient Egyptian Polyuria to Discovery of Insulin. Published in: Studies in Social Science & Humanities , Vol. 2, No. 7 (12 August 2023): pp. 26-34.
2. Kurtzhals P, Gough S. Diabet Med. 2021; 38(12): e14623.
3. Langerhans P. Beiträge zur mikroskopischen Anatomie der Bauchspeicheldrüse. Inaugural-Dissertation, Berlin, 1869.
4. von Mering J, Minkowski O. Diabetes mellitus nach Pankreasexstirpation. Arch Exp Pathol Pharmakol. 1890; 26: 371-387.
5. Banting FG, Best CH. The internal secretion of the pancreas. J Lab Clin Med. 1922; 7: 251-266.
6. Banting FG, Best CH, Collip JB, et al. Pancreatic extracts in the treatment of diabetes mellitus. Can Med Assoc J 1922;12:141-146.
7. Sanger F. The arrangement of amino acids in proteins. Adv Protein Chem 1952;7:1-67.
8. The Diabetes Control and Complications Trial (DCCT) Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med 1993;329:977-986.
9. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet 1998;352:837-853.
10. Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications (DCCT/EDIC) Research Group. Intensive diabetes treatment and cardiovascular outcomes in type 1 diabetes: the DCCT/EDIC study 30-year follow-up. Lancet Diabetes Endocrinol 2016;4:561-569.
11. Goeddel DV, Kleid DG, Bolivar F, et al. Expression in Escherichia coli of chemically synthesized genes for human insulin. Proc Natl Acad Sci U S A 1979;76:106-110.
12. Chance RE, Frank BH. Research, development, production, and safety of biosynthetic human insulin. Diabetes Care 1993;16(Suppl 3):133-142.
13. Heise T, Nosek L, Bøttcher SG, et al. Ultra-long-acting insulin degludec has a flat and stable glucose-lowering effect. Diabetes Obes Metab 2012;14:944-950.
14. Zinman B, Philis-Tsimikas A, Cariou B, et al. Insulin degludec versus insulin glargine in insulin-naive patients with type 2 diabetes: a 1-year, randomized, treat-to-target trial (BEGIN Once Long). Diabetes Care 2012;35:2464-2471.
15. Heise T, Chien J, Beals JM, et al. Pharmacokinetic and pharmacodynamic properties of insulin icodec compared with insulin glargine U100 and degludec in people with type 2 diabetes. Diabetes Care 2021;44:1017-1024.
16. DeFronzo RA, Buse JB, Kim T, et al. Once-weekly dulaglutide versus once-daily liraglutide in metformin-treated patients with type 2 diabetes (AWARD-6): a randomised, open-label, phase 3, non-inferiority trial. Lancet 2015;385:2057-2066.
17. Gough SCL, Bode B, Woo V, et al. Efficacy and safety of a fixed-ratio combination of insulin degludec and liraglutide (IDegLira) compared with its components given alone: results of a phase 3, open-label, randomised, 26-week, treat-to-target trial in insulin-naive patients with type 2 diabetes. Lancet Diabetes Endocrinol 2014;2:885-893.
18. Battelino T, Danne T, Bergenstal RM, et al. Clinical targets for continuous glucose monitoring data interpretation: recommendations from the international consensus on time in range. Diabetes Care 2019;42:1593-1603.
19. Brown SA, Kovatchev BP, Raghinaru D, et al. Six-month randomized, multicenter trial of closed-loop control in type 1 diabetes. N Engl J Med 2019;381:1707-1717.
20. Bailey CJ, Tahrani AA, Barnett AH. Future glucose-lowering drugs for type 2 diabetes. Lancet Diabetes Endocrinol 2016;4:350-359.
21. Heinemann L, Jacques Y. Oral insulin and buccal insulin: a critical reappraisal. J Diabetes Sci Technol 2009;3:568-584.
22. Veiseh O, Tang BC, Whitehead KA, et al. Managing diabetes with nanomedicine: challenges and opportunities. Nat Rev Drug Discov 2015;14:45-57.
23. Chuang VT, Kragh-Hansen U, Otagiri M. Pharmaceutical strategies utilizing recombinant human serum albumin. Pharm Res 2002;19:569-577.
24. Bergenstal RM, Garg S, Weinzimer SA, et al. Safety of a hybrid closed-loop insulin delivery system in patients with type 1 diabetes. JAMA 2016;316:1407-1408. 2 comments
百年演进:从奇迹发现到科学基石
1、漫长探索:从模糊认知到靶点锁定
在胰岛素诞生前,人类对糖尿病的认知长期停滞于表象观察。古埃及已有关于多尿症状的记载,古希腊文献中亦可见类似描述,但这些观察均未能触及疾病的本质[1,2]。直至19世纪,德国学者Paul Langerhans在胰腺中发现独特细胞团簇(后称“胰岛”),首次为糖尿病研究锚定了解剖学靶点[3]。随后的动物实验进一步证实:胰腺分泌着维系血糖平衡的关键物质,而其缺乏直接导致糖尿病[4]。至此,科学探索的焦点凝聚于如何提取这一神秘物质。
1921年,班廷成功从狗胰腺中提取出具有生物活性的胰岛素物质[5]。其后,生物化学家James Collip对对提取物进行精制纯化,使其得以安全用于人体[6]。1922年,该胰岛素被应用于一名14岁的1型糖尿病患者Leonard Thompson,其危重的高血糖与酮症得到奇迹般逆转——这标志着现代糖尿病治疗纪元的正式开启。
2、超越治疗:胰岛素带来的多重科学革命
从动物胰腺提取物起步,胰岛素经历了百年演进,历经基因工程合成的人胰岛素,逐步发展出速效、长效、预混及超长效类似物,并进一步实现了每周一次给药的基础胰岛素周制剂,每一步都标志着药学技术与治疗理念的跃升。
胰岛素演进从根本上重塑了代谢领域。它不仅精准揭示了胰岛素绝对或相对缺乏是糖尿病病理生理的核心[7],还通过阐明其对糖、脂肪、蛋白质代谢的调节机制(图1),奠定了现代代谢研究的基石。

图1. 胰岛素与糖、蛋白、脂肪代谢
同时,一系列大型临床研究对胰岛素治疗的探索,促进了糖尿病管理理念的持续发展(图2)。例如,DCCT/EDIC研究证实,早期强化胰岛素治疗可带来长期获益[8]。UKPDS研究证实了新诊断2型糖尿病(T2DM)患者早期强化治疗可带来长期并发症获益[9]。这些研究开创了以长期硬终点为导向的循证实践范式,引领现代医学进入以高质量证据为决策核心的循证时代[10]。

图2. 胰岛素治疗相关的循证研究
胰岛素研究对现代科学的贡献不仅限于代谢领域,更延伸至蛋白质科学、生物技术、化学技术等众多科学领域。其中,在蛋白质科学领域,胰岛素是全球首个人工合成的蛋白质。其氨基酸序列的测定和三维结构的解析为蛋白质折叠与功能研究奠定了基础。同时,胰岛素生物合成途径的阐明及其高灵敏、特异性测量方法的建立,推动了蛋白质研究的整体方法论进步[11]。在生物技术领域,胰岛素首次将重组DNA技术应用于大规模生产,其后进一步使用酵母系统进行生产,建立了安全、可扩展的工业化生产体系。这一技术不仅开创了生物制药的新纪元,也为后续各类重组蛋白药物(如生长激素、干扰素、抗体类药物)的研发与生产铺平了道路[12]。
彭永德教授曾在学术会议上提到,现代胰岛素治疗的核心目标是精准模拟人体生理性胰岛素分泌模式。在生理状态下,胰岛素分泌呈现两种基本模式:基础分泌以持续、低速率的胰岛素释放,抑制肝脏葡萄糖输出,维持空腹血糖稳定;餐时脉冲分泌则在进食后迅速大量释放胰岛素,促进葡萄糖利用与储存,从而有效控制餐后血糖升高(图3)。

图3. 生理胰岛素分泌模式
为了模拟这一理想状态,胰岛素研发长期围绕“基础-餐时胰岛素”方案不断演进,形成了一套多维度、系统化的现代治疗策略。
1、基础胰岛素的持续革新
基础胰岛素的发展史,是一部向更持久、更平稳、更贴近生理方向演进的技术革新史。早期使用的中效胰岛素(如NPH)存在明显的药效峰值,易引发夜间低血糖风险。随着分子修饰技术的突破,第一代长效类似物(如地特胰岛素)实现了无峰值的平稳释放,显著降低了低血糖发生率。新一代超长效类似物(如德谷胰岛素)通过结构优化与制剂创新,进一步将作用时间延长至30~42小时,为血糖控制提供了更平稳、更持久的解决方案[13]。
最具里程碑意义的突破是基础胰岛素周制剂——依柯胰岛素的问世。其通过脂肪酸酰化技术显著延长半衰期达196小时,实现了每周一次给药的革命性跨越(图4)。这一突破将患者全年的基础胰岛素注射次数从365次减少至约52次,不仅极大减轻治疗负担、提高依从性,也为糖尿病长期管理提供了更人性化、更贴近生理节律的治疗选择[14,15]。
2、餐时胰岛素的快速匹配
餐时胰岛素的进化方向是不断缩短起效时间,以更好地匹配餐后快速上升的血糖水平。传统的短效人胰岛素需在餐前30分钟注射,而新一代速效胰岛素类似物,如门冬胰岛素,将起效时间缩短至10~15分钟,可实现餐前即刻甚至餐后立即注射。这不仅为患者提供了更灵活的生活方式,也有助于减少迟发性低血糖的发生风险。
3、复合制剂的简化策略
为在疗效与便捷性之间取得平衡,预混胰岛素和双胰岛素类似物应运而生。这类制剂通过两种方式简化治疗方案:一是将基础与餐时胰岛素按固定比例预先混合(如预混门冬胰岛素30);二是利用创新技术使基础与餐时成分在注射后独立发挥各自作用(如德谷门冬双胰岛素)。这两种设计均在减少每日注射次数的同时,实现对空腹及餐后血糖的双重控制,特别适用于仍保留部分胰岛素分泌功能的T2DM患者。
4、联合治疗的协同强化
针对T2DM复杂的病理生理机制,胰岛素联合其他作用机制的药物已成为核心优化策略[16]。例如,胰岛素和胰高糖素样肽-1受体激动剂(GLP-1RA)的联合应用:胰岛素直接补充内源性胰岛素分泌不足,降低空腹血糖;而GLP-1RA则以葡萄糖浓度依赖性方式促进胰岛素分泌、抑制胰高血糖素释放、延缓胃排空,从而在控制餐后血糖、减轻体重及心血管保护方面发挥协同作用[17]。
5、技术赋能的个体化管理
现代监测与管理技术提高了胰岛素治疗的精细化管理。持续葡萄糖监测(CGM)通过提供实时、全面的葡萄糖图谱,推动治疗从经验推断转向数据驱动。胰岛素泵与CGM联动的混合闭环系统,能够根据血糖读数自动调节基础胰岛素输注率,已初步实现“人工胰腺”功能[18]。同时,数字化管理平台与应用程序通过整合胰岛素剂量、血糖、饮食、运动等多维数据,构建起支持远程指导、医患协同与自我管理的智能生态系统[19],进一步推动糖尿病管理的现代化与智能化发展。
综上所述,现代胰岛素治疗已超越早期简单的替代补充理念,发展成为一套集生理模拟精准化、制剂方案个性化、治疗机制协同化、管理手段智能化于一体的高度整合模式。这一演进不仅显著提升血糖控制的安全性、有效性及患者依从性,更从根本上改善糖尿病患者的生活质量与远期预后,同时为迈向更理想、更智慧的糖尿病管理新时代奠定了坚实基础。
未来展望:突破瓶颈,迈向智能与治愈新纪元
尽管已取得显著成就,当前胰岛素治疗仍面临几项关键挑战:进一步降低低血糖风险、提升患者生活质量、更精准地模拟生理性胰岛素分泌模式以及提高治疗可及性与经济性。目前的研究与开发正围绕这些核心问题持续推进,旨在为糖尿病患者带来更安全、更便捷、更符合生理且更具成本效益的治疗方案。
1、联合治疗:从协同增效到病理根源干预
目前,胰岛素周制剂与GLP-1RA周制剂的联合制剂正处于研发阶段。此类联合制剂通过机制互补,协同调控血糖与体重(图5),有望实现“双周一次”或“每月一次”的超长效给药方案,从而显著简化治疗流程、减轻患者负担,并进一步提升治疗依从性。

图5. 基础胰岛素与GLP-1RA的协同作用
更前沿的研究正探索以胰岛素为核心,联合作用于胰岛素抵抗、慢性炎症、代谢相关脂肪性肝病、β细胞功能保护及凋亡抑制等多重病理生理环节的创新治疗方案。此类多靶点、多维度的联合策略,旨在从疾病根源进行干预,不仅追求血糖稳定控制,更致力于实现机体长期代谢稳态的重建,从而为T2DM功能性逆转提供潜在可能[20]。
2、更便捷的给药:口服胰岛素
口服胰岛素因其无创便捷、可模拟生理性门静脉输注途径等优势,长期以来被视为糖尿病药物治疗的理想选择,但其发展面临多重生物学障碍:胃内酸性环境易导致胰岛素变性失活,肠道中丰富的蛋白酶可快速降解其肽链结构,而肠上皮紧密连接及胰岛素分子本身的亲水性也严重限制了其跨膜吸收,导致口服生物利用度普遍低于1%[21]。
为克服这些屏障,研究已取得一系列进展:通过脂质体、纳米粒等包埋技术及肠溶包衣策略保护胰岛素免受胃肠道环境破坏;利用渗透促进剂和细胞穿透肽增强其在肠道黏膜的透过性;并开发肠道微针胶囊、仿生载体系统等新型递送技术以提升靶向吸收效率[22]。
尽管目前尚无口服胰岛素产品成功实现大规模商业化应用,但随着制剂工程与纳米递送技术的持续进步,这一更具生理贴合性、用药更便利的治疗方案正逐步从科学理想迈向临床现实。
3、更智能的胰岛素:葡萄糖敏感性胰岛素
葡萄糖敏感性胰岛素的核心机制是在胰岛素分子结构中引入可感应葡萄糖浓度的“分子开关”。例如,候选分子NNC2215在血糖升高时,其分子构象发生改变,增强与胰岛素受体的结合能力,从而促进降糖作用;当血糖降低时,分子开关“关闭”,减弱其生物活性,进而显著降低低血糖风险[23]。
这类智能胰岛素分子能够更贴近生理性胰岛素分泌的动态调节模式,有望实现更安全、更自主的血糖管理,代表了胰岛素疗法向仿生智能化方向演进的重要趋势。
4、更整合的系统:数字化与闭环生态系统
未来的糖尿病管理将是一个高度整合的数字化生态系统。这不仅仅是设备的连接,更是数据、算法和服务的深度融合[24]。高级混合闭环及全闭环系统将搭载更智能的算法,实现餐食、运动等日常代谢扰动的自动识别与响应,推动血糖调节走向全自动化。人工智能与大数据技术将应用于血糖趋势预测、个性化胰岛素剂量调整与生活方式指导,并可提前预警高低血糖风险。基于云平台的虚拟照护与远程医疗系统,能够实现患者实时数据与医疗团队的无缝共享,打破地理限制,支持远程监测、即时干预与个体化指导,从而系统性提升糖尿病管理的效率、质量与可及性。
创新·超越·未来:胰岛素的百年征程
胰岛素的百年历程,是一部从绝望中诞生希望、在探索中实现超越、于创新中定义未来的医学史诗。它从一个挽救生命的简单提取物,成长为驱动蛋白质科学和生物技术革命的引擎,持续推动糖尿病管理理念的每一次突破。
今天,周制剂重塑了治疗便捷性的标准,CGM与智能算法正将管理推向精准化。展望未来,葡萄糖敏感性胰岛素、口服制剂和智能化闭环系统,将共同开启一个更安全、更自主、更智能的糖尿病管理新时代。
站在新百年的起点,胰岛素的故事仍在继续——它以持续创新的生命力,为数亿患者照亮通往更健康、更自主生活的道路,生动诠释着医学守护人类健康的永恒使命。
参考文献
1. Mohajan, Devajit (2023): Historical View of Diabetics Mellitus: From Ancient Egyptian Polyuria to Discovery of Insulin. Published in: Studies in Social Science & Humanities , Vol. 2, No. 7 (12 August 2023): pp. 26-34.
2. Kurtzhals P, Gough S. Diabet Med. 2021; 38(12): e14623.
3. Langerhans P. Beiträge zur mikroskopischen Anatomie der Bauchspeicheldrüse. Inaugural-Dissertation, Berlin, 1869.
4. von Mering J, Minkowski O. Diabetes mellitus nach Pankreasexstirpation. Arch Exp Pathol Pharmakol. 1890; 26: 371-387.
5. Banting FG, Best CH. The internal secretion of the pancreas. J Lab Clin Med. 1922; 7: 251-266.
6. Banting FG, Best CH, Collip JB, et al. Pancreatic extracts in the treatment of diabetes mellitus. Can Med Assoc J 1922;12:141-146.
7. Sanger F. The arrangement of amino acids in proteins. Adv Protein Chem 1952;7:1-67.
8. The Diabetes Control and Complications Trial (DCCT) Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med 1993;329:977-986.
9. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet 1998;352:837-853.
10. Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications (DCCT/EDIC) Research Group. Intensive diabetes treatment and cardiovascular outcomes in type 1 diabetes: the DCCT/EDIC study 30-year follow-up. Lancet Diabetes Endocrinol 2016;4:561-569.
11. Goeddel DV, Kleid DG, Bolivar F, et al. Expression in Escherichia coli of chemically synthesized genes for human insulin. Proc Natl Acad Sci U S A 1979;76:106-110.
12. Chance RE, Frank BH. Research, development, production, and safety of biosynthetic human insulin. Diabetes Care 1993;16(Suppl 3):133-142.
13. Heise T, Nosek L, Bøttcher SG, et al. Ultra-long-acting insulin degludec has a flat and stable glucose-lowering effect. Diabetes Obes Metab 2012;14:944-950.
14. Zinman B, Philis-Tsimikas A, Cariou B, et al. Insulin degludec versus insulin glargine in insulin-naive patients with type 2 diabetes: a 1-year, randomized, treat-to-target trial (BEGIN Once Long). Diabetes Care 2012;35:2464-2471.
15. Heise T, Chien J, Beals JM, et al. Pharmacokinetic and pharmacodynamic properties of insulin icodec compared with insulin glargine U100 and degludec in people with type 2 diabetes. Diabetes Care 2021;44:1017-1024.
16. DeFronzo RA, Buse JB, Kim T, et al. Once-weekly dulaglutide versus once-daily liraglutide in metformin-treated patients with type 2 diabetes (AWARD-6): a randomised, open-label, phase 3, non-inferiority trial. Lancet 2015;385:2057-2066.
17. Gough SCL, Bode B, Woo V, et al. Efficacy and safety of a fixed-ratio combination of insulin degludec and liraglutide (IDegLira) compared with its components given alone: results of a phase 3, open-label, randomised, 26-week, treat-to-target trial in insulin-naive patients with type 2 diabetes. Lancet Diabetes Endocrinol 2014;2:885-893.
18. Battelino T, Danne T, Bergenstal RM, et al. Clinical targets for continuous glucose monitoring data interpretation: recommendations from the international consensus on time in range. Diabetes Care 2019;42:1593-1603.
19. Brown SA, Kovatchev BP, Raghinaru D, et al. Six-month randomized, multicenter trial of closed-loop control in type 1 diabetes. N Engl J Med 2019;381:1707-1717.
20. Bailey CJ, Tahrani AA, Barnett AH. Future glucose-lowering drugs for type 2 diabetes. Lancet Diabetes Endocrinol 2016;4:350-359.
21. Heinemann L, Jacques Y. Oral insulin and buccal insulin: a critical reappraisal. J Diabetes Sci Technol 2009;3:568-584.
22. Veiseh O, Tang BC, Whitehead KA, et al. Managing diabetes with nanomedicine: challenges and opportunities. Nat Rev Drug Discov 2015;14:45-57.
23. Chuang VT, Kragh-Hansen U, Otagiri M. Pharmaceutical strategies utilizing recombinant human serum albumin. Pharm Res 2002;19:569-577.
24. Bergenstal RM, Garg S, Weinzimer SA, et al. Safety of a hybrid closed-loop insulin delivery system in patients with type 1 diabetes. JAMA 2016;316:1407-1408. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言