编者按:
在糖尿病管理日益强调精准化与个体化的今天,如何科学评估患者对日常饮食的真实血糖反应,成为临床与科研的关键议题。传统基于血糖指数(GI)的营养建议虽具参考价值,却难以解释个体间对相同食物的巨大反应差异。尤其在中国等以碳水为主食的地区,不同主食(如米饭、面条、馒头、燕麦)对餐后血糖的实际影响,以及进餐时间是否真正“重要”,仍缺乏高质量的真实世界证据。近期,一项发表在Int J Gen Med期刊上的新研究“Postprandial Glycemic Impact of Meal Timing and Staple Type in Outpatients with Dysglycemia: A Pilot Study Under a Streamlined and Real-World Framework”进行探索,现整理如下!
碳水化合物对餐后血糖影响最大。在亚洲,白米、小麦制品和燕麦是主要主食,尽管其血糖指数(GI)已有记载,但研究发现个体对相同食物的PPGR差异显著,且关于这些主食在真实生活场景下的相对影响,尤其是在IGT和T2DM人群中的研究仍存在空白。同时,关于用餐时间对PPGR影响的研究也较为缺乏。
为此,我们利用CGM在自由生活条件下,对血糖异常人群的PPGR进行研究,重点关注主食类型和用餐时间这两个关键变量,并初步探讨了人口学、生活方式等因素对个体差异的影响。
2、研究设计
本研究采用一种创新的一站式真实世界研究框架,旨在高效捕捉T2DM及IGT门诊患者的真实餐后血糖反应(PPGRs)。参与者仅需一次门诊就诊,即可完成饮食指导与CGM传感器(Guardian™ Sensor 3,美敦力)的佩戴,随后在家中按日常习惯完成标准化测试餐,并自行取下设备,无需复诊,从而最大限度减轻参与负担并提升数据生态效度。研究共纳入33名符合标准的参与者[年龄18~75岁,体重指数(BMI)18~35 kg/m2,糖化血红蛋白(HbA1c)<11%,用药稳定或未治疗],在为期一周的自由生活期间完成7次含50克碳水化合物的标准化饮食测试。
测试内容包括:在个体惯常用餐时间摄入葡萄糖溶液(早餐、午餐、晚餐),以及在午餐时段分别摄入蒸小麦面包、日式米饭、小麦面条和燕麦,以评估不同主食对PPGR的影响——此设计契合中国人群午餐碳水主食摄入最高的饮食模式。
所有参与者均签署书面知情同意,研究方案经北京协和医学院医院伦理委员会批准(JS-2450),并在ClinicalTrials.gov注册(NCT04562454),严格遵循《赫尔辛基宣言》。为确保数据质量,研究通过餐食照片、厨房秤称重及标准化烹饪指南减少自我报告偏差;CGM每5分钟记录一次间质葡萄糖值,基线血糖定义为餐前30分钟中位值,主要结局指标为餐后120分钟增量曲线下面积(iAUC120)。
数据分析采用线性混合效应模型(以受试者为随机截距),校正年龄、性别、BMI、HbA1c和基线血糖,比较不同用餐时间及主食类型对PPGR的影响,并进一步构建个体化敏感性指数(如精制主食敏感指数、燕麦敏感指数等),结合多重插补法处理缺失数据,辅以随机森林插补进行敏感性分析。所有统计分析基于R 4.5.1完成,显著性水平设为P<0.05。
3、研究结果
本研究共35人报名,2人因时间冲突退出,最终33人纳入分析。参与者普遍认为该研究框架简便、耐量性好,并愿意再次参与类似测试。共收集231条餐食记录(33人×7餐),其中200条(86.58%)保留用于分析,31条(13.42%)被排除,原因包括:未遵守方案(n=12)、基线血糖异常(n=4)、数据缺失(n=9)及iAUC120过低(<18 mmol/L·min,n=6)。
1.基线特征
因缺失两个及以上餐次血糖数据的参与者被排除,时间效应分析最终纳入全部33名参与者。
如图1所示,研究比较了早餐、午餐和晚餐后120分钟与180分钟的血糖反应曲线及iAUC分布。线性混合效应模型(以早餐为参照)显示:在120分钟内,用餐时间对iAUC120整体无显著影响(P=0.110);虽晚餐较早餐iAUC120降低(β=-59.49,95% CI:-114.68~-4.30,未调整P=0.039),但经多重比较校正后不显著(调整P=0.096);午餐与早餐差异亦不显著(调整P=0.352)。
其他PPGR指标(相对峰值、波动幅度、达峰时间、变异系数)均不受用餐时间影响(均P>0.05)。180分钟分析结果类似:iAUC180整体无显著时间效应(P=0.097),晚餐较早餐降低(β=-76.15,未调整P=0.032),但校正后不显著(调整P=0.080);午餐与早餐无差异(调整P=0.405),其余指标亦无显著时间效应。

图1. 早餐、午餐和晚餐摄入葡萄糖后的血糖反应曲线(120分钟:a;180分钟:b),以及相应iAUC120(c)和iAUC180(d)的分布情况
3.主食类型对血糖反应的影响
排除主食类型(葡萄糖、蒸面包、米饭、面条、燕麦)中缺失三种及以上数据的参与者后,共30人纳入分析。
如图2所示,研究比较了午餐摄入五种碳水化合物后的血糖反应曲线及iAUC分布。以葡萄糖为参照的线性混合效应模型显示:在120分钟内,主食类型对iAUC120有显著整体影响(P<0.001),蒸面包、米饭、面条和燕麦均显著低于葡萄糖,其中面条降幅最大(β=-179.53,调整P<0.001),其次为蒸面包(β=-142.99)、燕麦(β=-129.88)和米饭(β=-100.58,调整P=0.002);面条iAUC120亦显著低于米饭(调整P=0.025)。
所有主食的相对峰值血糖和波动幅度均显著低于葡萄糖(均P<0.001),但主食间无差异;峰值时间和变异系数不受主食类型影响(均P>0.05)。180分钟分析结果类似:主食类型对iAUC180整体影响显著(P<0.001),蒸面包、面条和燕麦显著低于葡萄糖(面条β=-181.98,调整P<0.001),米饭虽未校正时较低(P=0.022),但校正后不显著(调整P=0.143);相对峰值和波动幅度同样均低于葡萄糖(P<0.001),主食间无差异,峰值时间与变异系数仍无显著影响。
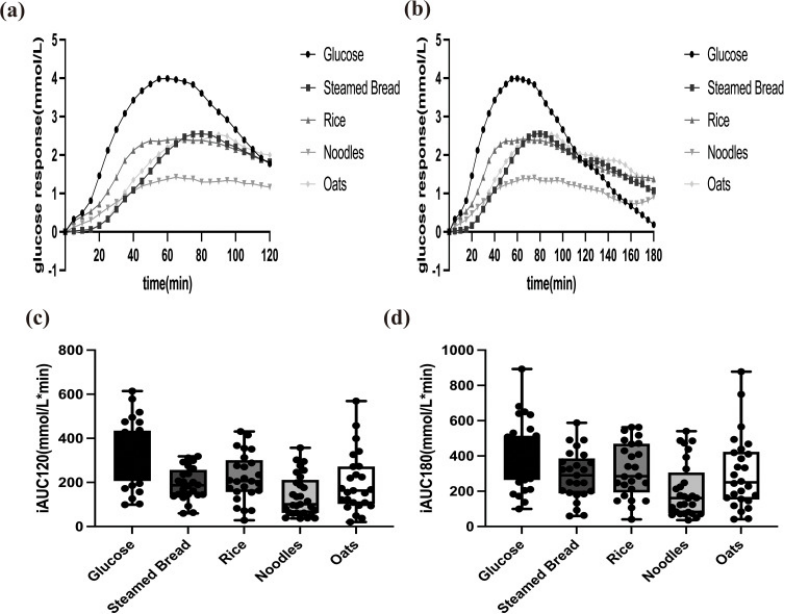
图2. 午餐摄入葡萄糖、蒸面包、米饭、面条和燕麦后的血糖反应曲线(120分钟:a;180分钟:b),以及对应的iAUC120(c)和iAUC180(d)分布情况
4.候选变量与四项个体化血糖反应指数(用餐时间变异指数、精制主食敏感指数、燕麦敏感指数和主食类型变异指数)的关联分析
在未调整和调整模型中,HOMA-IR与用餐时间变异指数呈显著正相关(调整后β=9.10,95% CI:3.01~15.20,P=0.005)。此外,相比中国南方出生者,华北出生者精制主食敏感指数显著更高(调整后 β=267.14,95% CI:59.18~475.09,P=0.014)。上述关联在敏感性分析中保持稳健;仅在敏感性分析中观察到睡眠/饮食规律与用餐时间变异指数的关联。其余变量(年龄、性别、BMI、HbA1c、用药、吸烟)均未与四项个体化指数中的任一指标显著相关(所有P>0.05)。
4、研究结论
总之,本研究证实了在门诊环境中高效获取真实PPGR数据的可行性。更重要的是,研究凸显个体反应的巨大异质性,强调营养干预应从“通用建议”转向“个体适配”——即从“何时吃最好”“哪种主食更好”,转向“对这个患者何时吃、吃什么最好”。未来需通过多中心、多样化队列验证此模型,并结合微生物组、代谢组等深入解析个体差异机制,推动精准营养在糖尿病管理中的落地。
参考文献
Wang S, et al. Int J Gen Med. 2026 Feb 26;19:591057. 2 comments
在糖尿病管理日益强调精准化与个体化的今天,如何科学评估患者对日常饮食的真实血糖反应,成为临床与科研的关键议题。传统基于血糖指数(GI)的营养建议虽具参考价值,却难以解释个体间对相同食物的巨大反应差异。尤其在中国等以碳水为主食的地区,不同主食(如米饭、面条、馒头、燕麦)对餐后血糖的实际影响,以及进餐时间是否真正“重要”,仍缺乏高质量的真实世界证据。近期,一项发表在Int J Gen Med期刊上的新研究“Postprandial Glycemic Impact of Meal Timing and Staple Type in Outpatients with Dysglycemia: A Pilot Study Under a Streamlined and Real-World Framework”进行探索,现整理如下!
1、研究背景
碳水化合物对餐后血糖影响最大。在亚洲,白米、小麦制品和燕麦是主要主食,尽管其血糖指数(GI)已有记载,但研究发现个体对相同食物的PPGR差异显著,且关于这些主食在真实生活场景下的相对影响,尤其是在IGT和T2DM人群中的研究仍存在空白。同时,关于用餐时间对PPGR影响的研究也较为缺乏。
为此,我们利用CGM在自由生活条件下,对血糖异常人群的PPGR进行研究,重点关注主食类型和用餐时间这两个关键变量,并初步探讨了人口学、生活方式等因素对个体差异的影响。
2、研究设计
本研究采用一种创新的一站式真实世界研究框架,旨在高效捕捉T2DM及IGT门诊患者的真实餐后血糖反应(PPGRs)。参与者仅需一次门诊就诊,即可完成饮食指导与CGM传感器(Guardian™ Sensor 3,美敦力)的佩戴,随后在家中按日常习惯完成标准化测试餐,并自行取下设备,无需复诊,从而最大限度减轻参与负担并提升数据生态效度。研究共纳入33名符合标准的参与者[年龄18~75岁,体重指数(BMI)18~35 kg/m2,糖化血红蛋白(HbA1c)<11%,用药稳定或未治疗],在为期一周的自由生活期间完成7次含50克碳水化合物的标准化饮食测试。
测试内容包括:在个体惯常用餐时间摄入葡萄糖溶液(早餐、午餐、晚餐),以及在午餐时段分别摄入蒸小麦面包、日式米饭、小麦面条和燕麦,以评估不同主食对PPGR的影响——此设计契合中国人群午餐碳水主食摄入最高的饮食模式。
所有参与者均签署书面知情同意,研究方案经北京协和医学院医院伦理委员会批准(JS-2450),并在ClinicalTrials.gov注册(NCT04562454),严格遵循《赫尔辛基宣言》。为确保数据质量,研究通过餐食照片、厨房秤称重及标准化烹饪指南减少自我报告偏差;CGM每5分钟记录一次间质葡萄糖值,基线血糖定义为餐前30分钟中位值,主要结局指标为餐后120分钟增量曲线下面积(iAUC120)。
数据分析采用线性混合效应模型(以受试者为随机截距),校正年龄、性别、BMI、HbA1c和基线血糖,比较不同用餐时间及主食类型对PPGR的影响,并进一步构建个体化敏感性指数(如精制主食敏感指数、燕麦敏感指数等),结合多重插补法处理缺失数据,辅以随机森林插补进行敏感性分析。所有统计分析基于R 4.5.1完成,显著性水平设为P<0.05。
3、研究结果
本研究共35人报名,2人因时间冲突退出,最终33人纳入分析。参与者普遍认为该研究框架简便、耐量性好,并愿意再次参与类似测试。共收集231条餐食记录(33人×7餐),其中200条(86.58%)保留用于分析,31条(13.42%)被排除,原因包括:未遵守方案(n=12)、基线血糖异常(n=4)、数据缺失(n=9)及iAUC120过低(<18 mmol/L·min,n=6)。
1.基线特征
应试者平均年龄43.21±10.47岁,女性占48.48%(16/33);84.85%(28人)为T2DM,15.15%(5人)为IGT;中位病程3.00(1.00~5.00)年,HbA1c中位数6.20%(5.57~6.78%);平均BMI 27.21±4.42 kg/m2,42.42%(14人)为肥胖;78.79%(26人)使用降糖药,其余仅行生活方式干预。男性吸烟率(47.06% vs. 6.25%)、精制谷物摄入率(94.12% vs. 62.50%)、血脂异常率(88.24% vs. 50.00%)及血清肌酐水平(79.80±16.56 vs. 56.77±9.23 μmol/L)均显著高于女性(P<0.05),而年龄、病程、HbA1c和用药情况在性别间无显著差异(P>0.05)。
因缺失两个及以上餐次血糖数据的参与者被排除,时间效应分析最终纳入全部33名参与者。
如图1所示,研究比较了早餐、午餐和晚餐后120分钟与180分钟的血糖反应曲线及iAUC分布。线性混合效应模型(以早餐为参照)显示:在120分钟内,用餐时间对iAUC120整体无显著影响(P=0.110);虽晚餐较早餐iAUC120降低(β=-59.49,95% CI:-114.68~-4.30,未调整P=0.039),但经多重比较校正后不显著(调整P=0.096);午餐与早餐差异亦不显著(调整P=0.352)。
其他PPGR指标(相对峰值、波动幅度、达峰时间、变异系数)均不受用餐时间影响(均P>0.05)。180分钟分析结果类似:iAUC180整体无显著时间效应(P=0.097),晚餐较早餐降低(β=-76.15,未调整P=0.032),但校正后不显著(调整P=0.080);午餐与早餐无差异(调整P=0.405),其余指标亦无显著时间效应。

图1. 早餐、午餐和晚餐摄入葡萄糖后的血糖反应曲线(120分钟:a;180分钟:b),以及相应iAUC120(c)和iAUC180(d)的分布情况
3.主食类型对血糖反应的影响
排除主食类型(葡萄糖、蒸面包、米饭、面条、燕麦)中缺失三种及以上数据的参与者后,共30人纳入分析。
如图2所示,研究比较了午餐摄入五种碳水化合物后的血糖反应曲线及iAUC分布。以葡萄糖为参照的线性混合效应模型显示:在120分钟内,主食类型对iAUC120有显著整体影响(P<0.001),蒸面包、米饭、面条和燕麦均显著低于葡萄糖,其中面条降幅最大(β=-179.53,调整P<0.001),其次为蒸面包(β=-142.99)、燕麦(β=-129.88)和米饭(β=-100.58,调整P=0.002);面条iAUC120亦显著低于米饭(调整P=0.025)。
所有主食的相对峰值血糖和波动幅度均显著低于葡萄糖(均P<0.001),但主食间无差异;峰值时间和变异系数不受主食类型影响(均P>0.05)。180分钟分析结果类似:主食类型对iAUC180整体影响显著(P<0.001),蒸面包、面条和燕麦显著低于葡萄糖(面条β=-181.98,调整P<0.001),米饭虽未校正时较低(P=0.022),但校正后不显著(调整P=0.143);相对峰值和波动幅度同样均低于葡萄糖(P<0.001),主食间无差异,峰值时间与变异系数仍无显著影响。

图2. 午餐摄入葡萄糖、蒸面包、米饭、面条和燕麦后的血糖反应曲线(120分钟:a;180分钟:b),以及对应的iAUC120(c)和iAUC180(d)分布情况
4.候选变量与四项个体化血糖反应指数(用餐时间变异指数、精制主食敏感指数、燕麦敏感指数和主食类型变异指数)的关联分析
在未调整和调整模型中,HOMA-IR与用餐时间变异指数呈显著正相关(调整后β=9.10,95% CI:3.01~15.20,P=0.005)。此外,相比中国南方出生者,华北出生者精制主食敏感指数显著更高(调整后 β=267.14,95% CI:59.18~475.09,P=0.014)。上述关联在敏感性分析中保持稳健;仅在敏感性分析中观察到睡眠/饮食规律与用餐时间变异指数的关联。其余变量(年龄、性别、BMI、HbA1c、用药、吸烟)均未与四项个体化指数中的任一指标显著相关(所有P>0.05)。
4、研究结论
总之,本研究证实了在门诊环境中高效获取真实PPGR数据的可行性。更重要的是,研究凸显个体反应的巨大异质性,强调营养干预应从“通用建议”转向“个体适配”——即从“何时吃最好”“哪种主食更好”,转向“对这个患者何时吃、吃什么最好”。未来需通过多中心、多样化队列验证此模型,并结合微生物组、代谢组等深入解析个体差异机制,推动精准营养在糖尿病管理中的落地。
参考文献
Wang S, et al. Int J Gen Med. 2026 Feb 26;19:591057. 2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言