编者按
在国际糖尿病联盟(IDF)2025年更新发布的2型糖尿病(T2DM)管理指南中,经典降糖药二甲双胍仍被明确列为一线基础治疗药物。这一推荐立足于其问世百余年所累积的坚实循证证据,超过60年临床实践反复验证的有效性与安全性,不断被发掘的降糖外多重获益,以及全球范围内的良好可及性与药物经济学优势。在当今新型证据层出不穷、靶器官保护理念日益深入的背景下,二甲双胍何以持续占据一线基石地位?本期默讲堂,中山大学附属第三医院曾龙驿教授将全面解读该指南,深入剖析二甲双胍在T2DM管理中的重要价值。
专家简介

中山大学附属第三医院内分泌科首席专家
中山大学附属第三医院甲状腺多学科诊疗中心副主任
广东省糖尿病防治重点实验室名誉主任
医学博士,主任医师,教授,博士生导师
中华医学会糖尿病学分会流行病学与预防学组副组长
中国老年学和老年医学学会基层慢病防治管理分会常委
中国研究型医院学会糖尿病学专业委员会常委
广东省医学会糖尿病学分会顾问
广东省中医药学会内分泌专委会顾问
降糖方案解析:从一线单药到联合基石的循证支持
2025 IDF指南[1]再次明确二甲双胍在T2DM药物治疗中的核心地位,推荐其作为全球T2DM患者的一线单药治疗及联合治疗的基石(图1)。这一推荐主要基于以下充分循证依据:
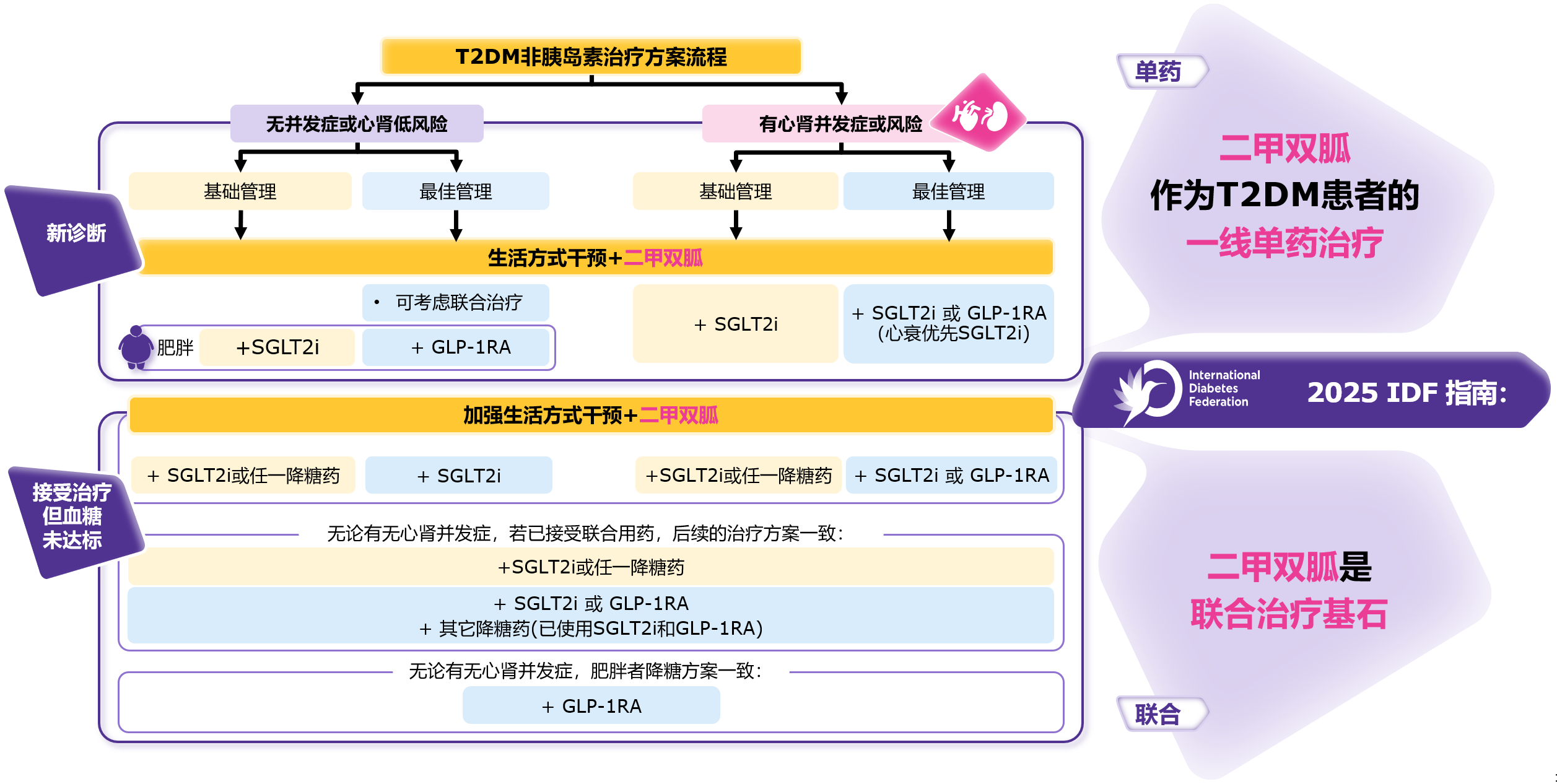
图1. 2025 IDF指南:T2DM非胰岛素治疗方案的具体建议
单药治疗中,二甲双胍呈剂量依赖性强效降糖,2000 mg/d最佳剂量下可降低HbA1c达2.0%[2]。其长期安全性良好,不增加低血糖风险,最常见不良反应为胃肠道反应且多为轻中度、短暂性[3]。二甲双胍具有明确长期心血管获益:UKPDS 91研究42年随访数据显示,新诊断T2DM患者早期接受二甲双胍强化治疗,显著降低心肌梗死风险31%和全因死亡风险20%[4]。二甲双胍在全球不同收入国家中可获得性高(64.7%~100%)[5],且作为一线方案的成本效益显著优于SGLT2i或GLP-1RA(图2)[6,7]。
血糖控制不达标时需启动联合治疗,二甲双胍作为基础药物可与其他降糖药物联合,实现机制互补,协同降糖。荟萃分析表明,在二甲双胍基础上联用SGLT2i、GLP-1RA或DPP-4i均可进一步改善血糖控制,提高HbA1c达标率[8];与单用胰岛素相比,联用二甲双胍不仅增强降糖效果,还能减少体重增加和胰岛素用量(图3)[9]。
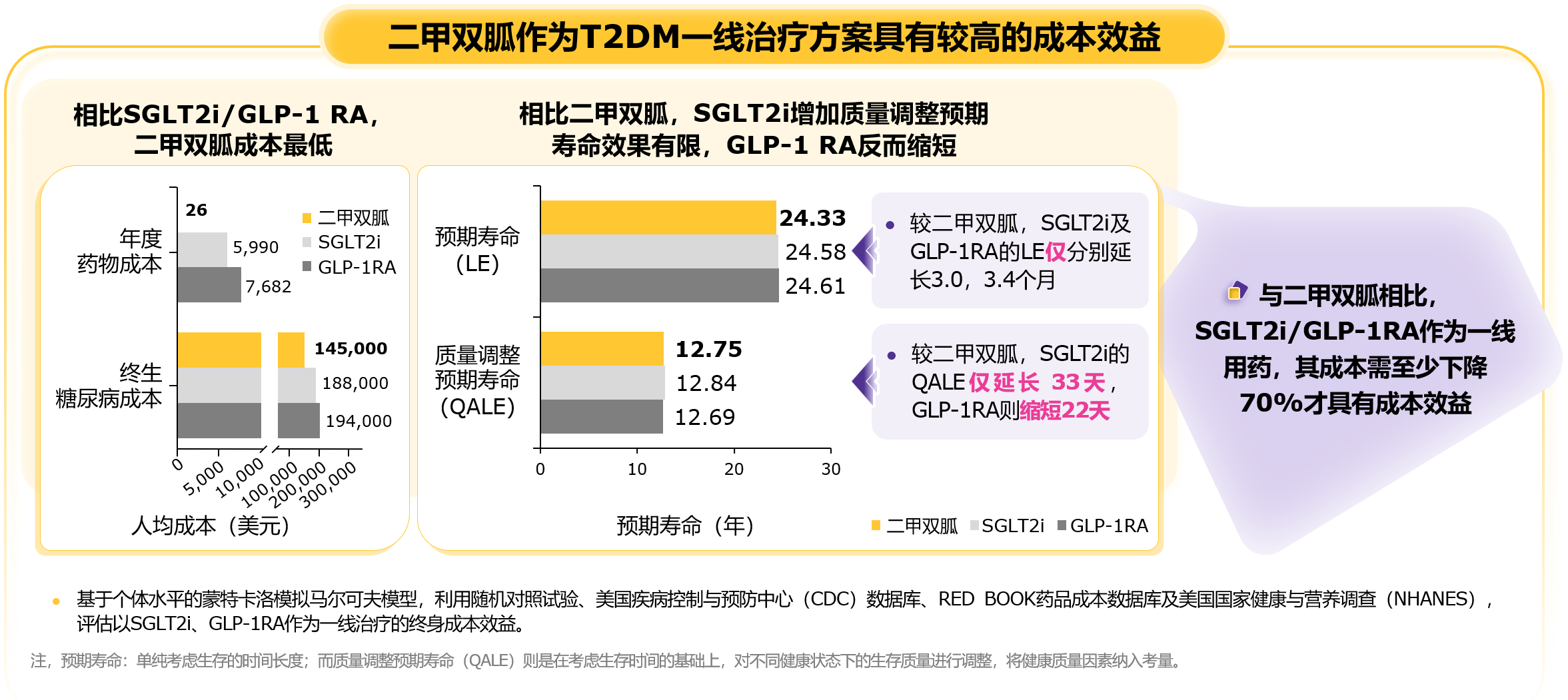
图2. 相比SGLT2i/GLP-1RA,二甲双胍作为一线治疗具有更高的成本效益
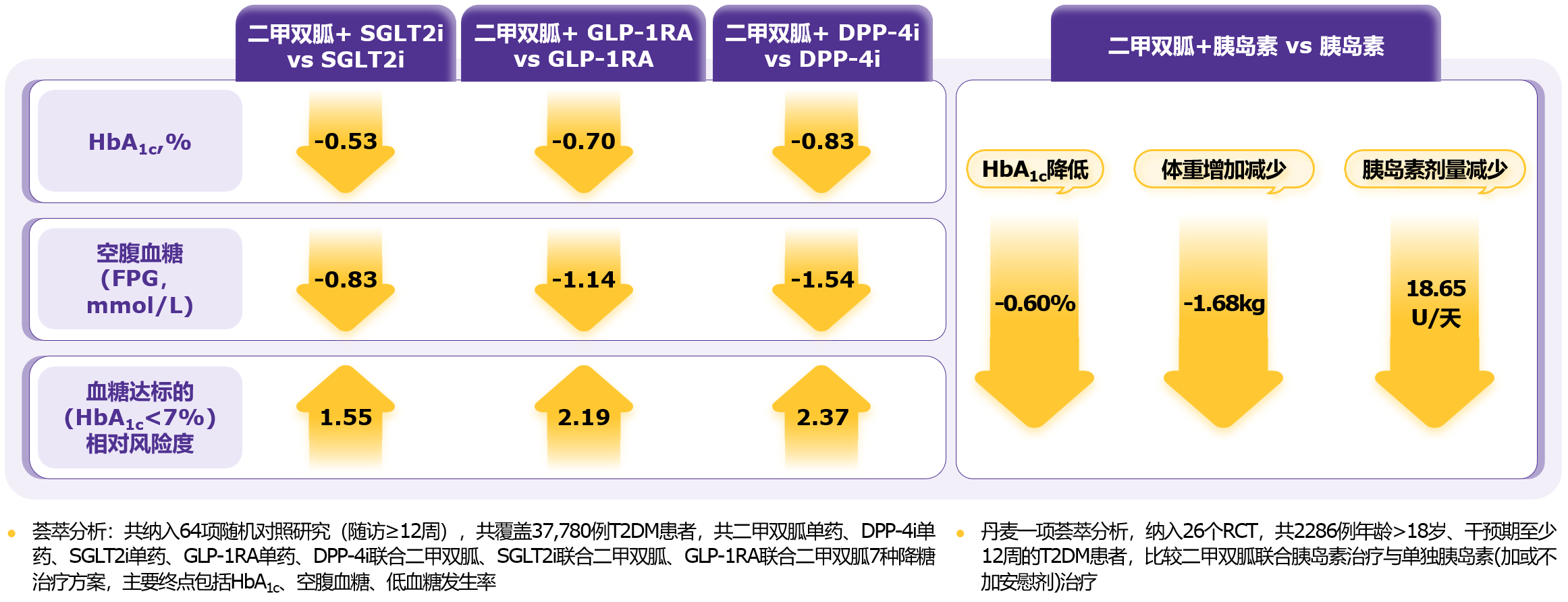
图3. 以二甲双胍为基础的联合治疗可进一步改善血糖控制,与胰岛素联用可减少体重增加,降低胰岛素剂量
2025 IDF指南[1]同时指出,目前支持SGLT2i或GLP-1RA作为一线单药治疗的证据仍不充分。相关心血管结局试验(CVOT)中,超过70%受试者基线使用了二甲双胍[10-25]。分析发现,SGLT2i/GLP-1RA降低合并心血管疾病(CVD)患者主要心血管不良事件(MACE)风险,但在仅有心血管危险因素或未合并ASCVD患者中未观察到MACE获益[26,27]。CVOT或肾脏结局试验证实SGLT2i或GLP-1RA降低合并CVD患者的MACE风险,但基线使用二甲双胍者较未使用者的主要结局风险进一步降低约30%[1]。因此,评估这两类新药的心血管获益时,无法完全排除二甲双胍的保护作用。
预防策略解析:从筛查策略到干预措施
糖尿病前期已成为全球重大公共卫生挑战,与糖尿病高患病率及不良结局密切相关。大庆研究发现,若不干预,6年及20年内糖尿病前期进展为糖尿病的比例分别高达65.8%与92.8%[28]。糖尿病前期人群发生微血管与大血管并发症的风险较血糖正常者高出2~4倍[29]。2025 IDF指南提出,1 h口服葡萄糖耐量试验(OGTT)可作为糖尿病及糖尿病前期筛查的新方法。从发病机制看,空腹血糖受损(IFG)人群主要表现为肝脏胰岛素抵抗,糖耐量受损(IGT)人群以外周胰岛素抵抗及胰岛素分泌缺陷为主,而IFG+IGT人群同时存在上述异常[30]。二甲双胍通过激活AMPK通路改善胰岛素抵抗,从而直击糖尿病前期的核心发病机制。
2025 IDF指南[1]推荐二甲双胍作为T2DM预防干预手段之一,除上述机制原因,也与其积累的多项研究证据有关。Cochrane系统评价显示,与安慰剂或单纯生活方式干预相比,二甲双胍可降低T2DM发生风险达50%[31];美国糖尿病预防计划(DPP)[32]与中国糖尿病预防计划(CDPP)[33]也分别证实,生活方式干预基础上联合二甲双胍能使糖尿病发病风险下降31%和17%(图4)。研究还发现,经强化生活方式干预者,体重平均每减少1 kg,糖尿病风险降低16%[34]。2025 IDF指南[1]也提示,即使减重1~2 kg也有助于降低糖尿病风险。DPP研究显示,二甲双胍可带来约2.5 kg的体重减轻,并在10年随访期间保持稳定[35]。MET-REMODEL研究则提示,在合并冠心病、胰岛素抵抗和/或糖尿病前期的非糖尿病人群中,二甲双胍可显著降低左室质量指数和左室质量,减少皮下脂肪、体重和血压[36]。
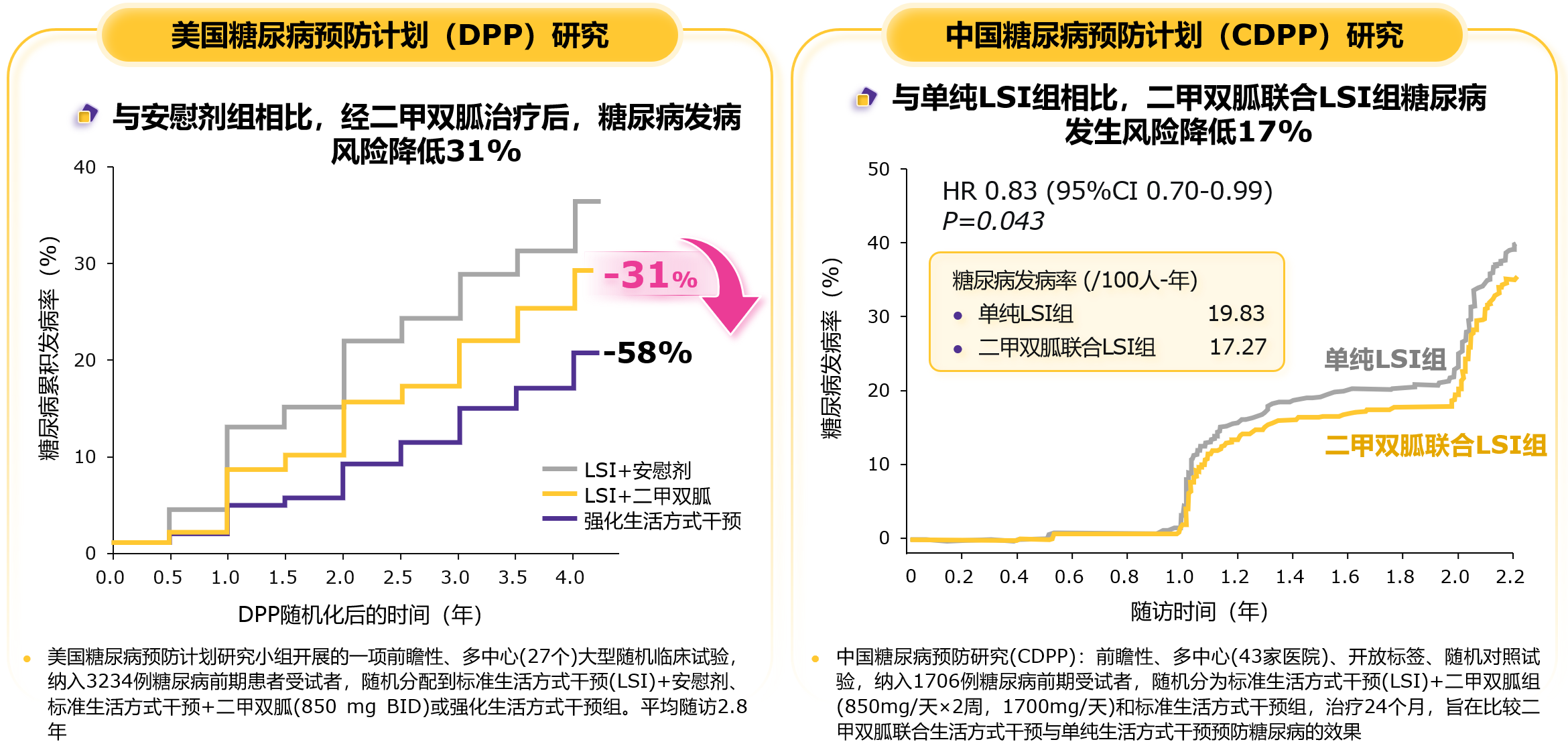
图4. 国内外大型临床试验证明二甲双胍显著降低糖尿病发生风险
靶器官保护策略解析:多支柱管理模式赋能并发症/合并症管理
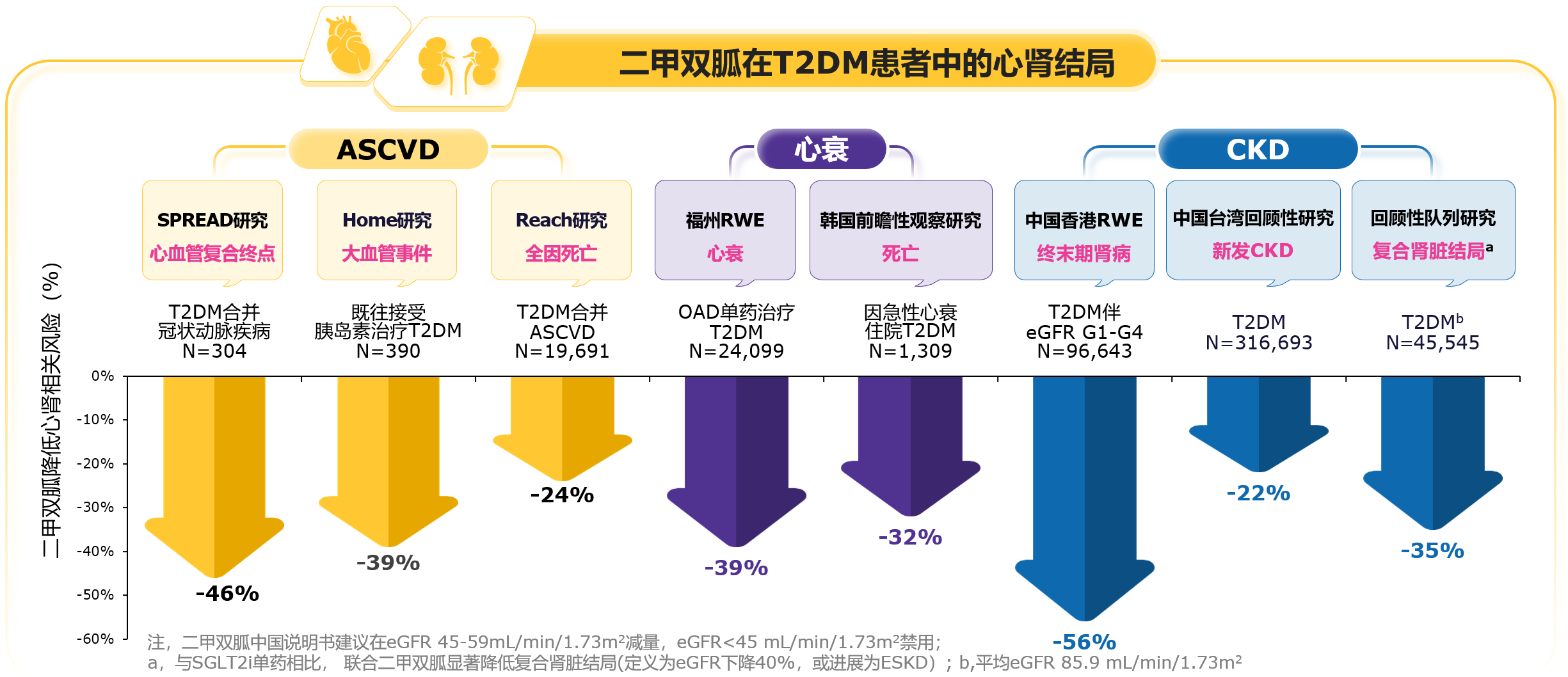
高血糖作为核心驱动力,肥胖及相关风险因素协同加剧其对多系统靶器官损伤。因此,2025 IDF指南指出,以危险因素控制为核心的多支柱综合管理成为防治并发症的基石,包括生活方式干预、早期强化血糖控制及多风险因素干预等[1]。在此框架下,二甲双胍展现出超越降糖的广泛获益。大量循证证据证实,其能为T2DM患者带来明确心肾保护作用,包括显著降低动脉粥样硬化性心血管疾病(ASCVD)、心力衰竭发生风险及全因死亡率,延缓CKD进展并减少终末期肾病风险(图5)[37-44]。此外,二甲双胍兼具降压、调脂等风险因素管理作用[45,46],其多效性契合糖尿病并发症多支柱管理原则。在代谢相关脂肪性肝病(MASLD)方面,二甲双胍可改善合并该病的T2DM患者的肝功能与代谢指标[47,48]。研究也提示,在糖尿病视网膜病变(DR)防治中,二甲双胍可降低其发生与进展风险,并可能增强抗VEGF治疗的疗效[49-53]。在体重管理方面,二甲双胍可使超重或肥胖T2DM患者体重轻度下降1.5~2.9 kg[54],与GIP/GLP-1RA联用时可增加实现减重≥15%的可能性[55]。
凭借其确切的疗效、良好的安全性及广泛的额外获益,二甲双胍在国内外指南中均居于核心地位。《国家基层糖尿病防治管理指南(2025)》[56]也明确推荐,二甲双胍应作为T2DM药物治疗的一线首选并贯穿全程,是联合治疗中不可或缺的基础药物。总之,二甲双胍全面覆盖糖尿病事件链全程管理,是实现糖尿病综合管理目标的重要基石。
总结
在T2DM管理中,二甲双胍凭借其全球可获得性、疗效确切、安全性良好、低血糖风险低、成本效益显著、明确的长期心血管获益及多个靶器官保护作用,被2025 IDF指南推荐作为一线单药治疗及联合治疗的基础,并推荐其用于糖尿病预防。我国《国家基层糖尿病防治管理指南(2025)》也明确,二甲双胍是T2DM治疗的一线首选和全程联合治疗的基石,若无禁忌且耐受,应长期保留于治疗方案中。在目前糖尿病治疗药物日益丰富的背景下,血糖管理常需联合用药,而二甲双胍在这一过程中仍具有不可替代的重要地位。
注:二甲双胍在中国尚未获批治疗糖尿病前期、MASLD、DR及降低体重的适应症,本文仅供医疗卫生人士学术交流。
参考文献
1. Ceriello A, et al. Diabetes Res Clin Pract. 2025; 222 Suppl 1: 112152.
2. Garber AJ, et al. Am J Med. 1997; 103(6): 491-497.
3. Kalyani RR, et al. JAMA. 2025; 334(11): 984-1002.
4. Adler AI, et al. Lancet. 2024; 404(10448): 145-155.
5. Chow CK, et al. Lancet Diabetes Endocrinol. 2018; 6(10): 798-808.
6. Solini A, Tricò D. Diabetes Obes Metab. 2024; 26 Suppl 3: 20-30.
7. Choi JG, et al. Ann Intern Med. 2022; 175(10): 1392-1400.
8. Jia S, et al. Acta Diabetol. 2021; 58(1): 5-18.
9. Hemmingsen B, et al. BMJ. 2012; 344: e1771.
10. Zinman B, et al. N Engl J Med. 2015; 373(22): 2117-2128. EMPA-REG OUTCOME
11. Neal B, et al. N Engl J Med. 2017; 377(7): 644-657. CANVAS
12. Wiviott SD, et al. N Engl J Med. 2019; 380(4): 347-357. DECLARE–TIMI 58
13. Cannon CP, et al. N Engl J Med. 2020; 383(15): 1425-1435. VERTIS CV
14. Bhatt DL, et al. N Engl J Med. 2021; 384(2): 129-139. SCORED
15. Pfeffer MA, et al. N Engl J Med. 2015; 373(23): 2247-2257. ELIXA
16. Marso SP, et al. N Engl J Med. 2016; 375(4): 311-322. LEADER
17. Marso SP, et al. N Engl J Med. 2016; 375(19): 1834-1844. SUSTAIN-6
18. Holman RR, et al. N Engl J Med. 2017; 377(13): 1228-1239. EXSCEL
19. Gerstein HC, et al. Diabetes Obes Metab. 2018; 20(1): 42-49. REWIND
20. Hernandez AF, et al. Lancet. 2018; 392(10157): 1519-1529. Harmony Outcomes
21. Husain M, et al. N Engl J Med. 2019; 381(9): 841-851. PIONEER 6
22. Gerstein HC, et al. N Engl J Med. 2021; 385(10): 896-907. AMPLITUDE-O
23. Ruff CT, et al. Nat Med. 2022; 28(1): 89-95. FREEDOM-CVO
24. McGuire DK, et al. Diabetes Obes Metab. 2023; 25(7): 1932-1941. SOUL
25. Nicholls SJ, et al. Am Heart J. 2024; 267: 1-11. SURPASS-CVOT
26. McGuire DK, et al. JAMA Cardiol. 2021; 6(2): 148-158.
27. Sattar N, et al. Lancet Diabetes Endocrinol. 2021; 9(10): 653-662.
28. Li G, et al. Lancet. 2008; 371(9626): 1783-1789.
29. Cai X, et al. BMJ. 2020; 370: m2297.
30. Campbell MD, et al. Nat Rev Endocrinol. 2020; 16(7): 395-400.
31. Madsen KS, et al. Cochrane Database Syst Rev. 2019; 12(12): CD008558.
32. Knowler WC, et al. N Engl J Med. 2002; 346(6): 393-403.
33. Zhang L, et al. Lancet Diabetes Endocrinol. 2023; 11(8): 567-577.
34. Hamman RF, et al. Diabetes Care. 2006; 29(9): 2102-2107.
35. Diabetes Prevention Program Research Group, et al. Lancet. 2009; 374(9702): 1677-1686.
36. Mohan M, et al. Eur Heart J. 2019; 40(41): 3409-3417.
37. Hong J, et al. Diabetes Care. 2013; 36(5): 1304-1311.
38. Kooy A, et al. Arch Intern Med. 2009; 169(6): 616-625.
39. Roussel R, et al. Arch Intern Med. 2010; 170(21): 1892-1899.
40. He S, et al. J Diabetes Res. 2021; 2021: 5534387.
41. Chun KH, et al. Diabetes Metab. 2024; 50(1): 101504.
42. Yang A, et al. Pharmaceuticals (Basel). 2022; 15(9): 1140.
43. Lin YL, et al. Pharmaceuticals (Basel). 2025; 18(1): 95.
44. Agur T, et al. Cardiovasc Diabetol. 2025; 24(1): 97.
45. Sin HY, et al. Arch Pharm Res. 2011; 34(1): 99-107.
46. Gillani SW, et al. J Pharm Bioallied Sci. 2021; 13(1): 76-82.
47. Feng WH, et al. J Diabetes Investig. 2019; 10(2): 399-407.
48. Liu W, et al. Biomedicines. 2025; 13(6): 1315.
49. Maleškić S, et al. Acta Med Acad. 2017; 46(2): 116-123.
50. Li Y, Ryu C, et al. J Diabetes Res. 2018; 2018: 2801450.
51. Fan YP, et al. J Diabetes Res. 2020; 2020: 9161039.
52. Uwimana A, et al. Medicine (Baltimore). 2022; 101(42): e31266.
53. Shao Y, et al. Acta Diabetol. 2022; 59(4): 553-559.
54. Ji L, et al. PLoS One. 2013; 8(2): e57222.
55. Małecki MT, et al. Diabetes Care. 2023; 46(12): 2292-2299.
56. 基本公共卫生服务项目基层糖尿病防治管理办公室, 中华医学会糖尿病学分会. 中华内科杂志. 2025; 64(12): 1169-1186. 2 comments
在国际糖尿病联盟(IDF)2025年更新发布的2型糖尿病(T2DM)管理指南中,经典降糖药二甲双胍仍被明确列为一线基础治疗药物。这一推荐立足于其问世百余年所累积的坚实循证证据,超过60年临床实践反复验证的有效性与安全性,不断被发掘的降糖外多重获益,以及全球范围内的良好可及性与药物经济学优势。在当今新型证据层出不穷、靶器官保护理念日益深入的背景下,二甲双胍何以持续占据一线基石地位?本期默讲堂,中山大学附属第三医院曾龙驿教授将全面解读该指南,深入剖析二甲双胍在T2DM管理中的重要价值。
专家简介

中山大学附属第三医院内分泌科首席专家
中山大学附属第三医院甲状腺多学科诊疗中心副主任
广东省糖尿病防治重点实验室名誉主任
医学博士,主任医师,教授,博士生导师
中华医学会糖尿病学分会流行病学与预防学组副组长
中国老年学和老年医学学会基层慢病防治管理分会常委
中国研究型医院学会糖尿病学专业委员会常委
广东省医学会糖尿病学分会顾问
广东省中医药学会内分泌专委会顾问
降糖方案解析:从一线单药到联合基石的循证支持
2025 IDF指南[1]再次明确二甲双胍在T2DM药物治疗中的核心地位,推荐其作为全球T2DM患者的一线单药治疗及联合治疗的基石(图1)。这一推荐主要基于以下充分循证依据:

图1. 2025 IDF指南:T2DM非胰岛素治疗方案的具体建议
单药治疗中,二甲双胍呈剂量依赖性强效降糖,2000 mg/d最佳剂量下可降低HbA1c达2.0%[2]。其长期安全性良好,不增加低血糖风险,最常见不良反应为胃肠道反应且多为轻中度、短暂性[3]。二甲双胍具有明确长期心血管获益:UKPDS 91研究42年随访数据显示,新诊断T2DM患者早期接受二甲双胍强化治疗,显著降低心肌梗死风险31%和全因死亡风险20%[4]。二甲双胍在全球不同收入国家中可获得性高(64.7%~100%)[5],且作为一线方案的成本效益显著优于SGLT2i或GLP-1RA(图2)[6,7]。
血糖控制不达标时需启动联合治疗,二甲双胍作为基础药物可与其他降糖药物联合,实现机制互补,协同降糖。荟萃分析表明,在二甲双胍基础上联用SGLT2i、GLP-1RA或DPP-4i均可进一步改善血糖控制,提高HbA1c达标率[8];与单用胰岛素相比,联用二甲双胍不仅增强降糖效果,还能减少体重增加和胰岛素用量(图3)[9]。

图2. 相比SGLT2i/GLP-1RA,二甲双胍作为一线治疗具有更高的成本效益

图3. 以二甲双胍为基础的联合治疗可进一步改善血糖控制,与胰岛素联用可减少体重增加,降低胰岛素剂量
2025 IDF指南[1]同时指出,目前支持SGLT2i或GLP-1RA作为一线单药治疗的证据仍不充分。相关心血管结局试验(CVOT)中,超过70%受试者基线使用了二甲双胍[10-25]。分析发现,SGLT2i/GLP-1RA降低合并心血管疾病(CVD)患者主要心血管不良事件(MACE)风险,但在仅有心血管危险因素或未合并ASCVD患者中未观察到MACE获益[26,27]。CVOT或肾脏结局试验证实SGLT2i或GLP-1RA降低合并CVD患者的MACE风险,但基线使用二甲双胍者较未使用者的主要结局风险进一步降低约30%[1]。因此,评估这两类新药的心血管获益时,无法完全排除二甲双胍的保护作用。
预防策略解析:从筛查策略到干预措施
糖尿病前期已成为全球重大公共卫生挑战,与糖尿病高患病率及不良结局密切相关。大庆研究发现,若不干预,6年及20年内糖尿病前期进展为糖尿病的比例分别高达65.8%与92.8%[28]。糖尿病前期人群发生微血管与大血管并发症的风险较血糖正常者高出2~4倍[29]。2025 IDF指南提出,1 h口服葡萄糖耐量试验(OGTT)可作为糖尿病及糖尿病前期筛查的新方法。从发病机制看,空腹血糖受损(IFG)人群主要表现为肝脏胰岛素抵抗,糖耐量受损(IGT)人群以外周胰岛素抵抗及胰岛素分泌缺陷为主,而IFG+IGT人群同时存在上述异常[30]。二甲双胍通过激活AMPK通路改善胰岛素抵抗,从而直击糖尿病前期的核心发病机制。
2025 IDF指南[1]推荐二甲双胍作为T2DM预防干预手段之一,除上述机制原因,也与其积累的多项研究证据有关。Cochrane系统评价显示,与安慰剂或单纯生活方式干预相比,二甲双胍可降低T2DM发生风险达50%[31];美国糖尿病预防计划(DPP)[32]与中国糖尿病预防计划(CDPP)[33]也分别证实,生活方式干预基础上联合二甲双胍能使糖尿病发病风险下降31%和17%(图4)。研究还发现,经强化生活方式干预者,体重平均每减少1 kg,糖尿病风险降低16%[34]。2025 IDF指南[1]也提示,即使减重1~2 kg也有助于降低糖尿病风险。DPP研究显示,二甲双胍可带来约2.5 kg的体重减轻,并在10年随访期间保持稳定[35]。MET-REMODEL研究则提示,在合并冠心病、胰岛素抵抗和/或糖尿病前期的非糖尿病人群中,二甲双胍可显著降低左室质量指数和左室质量,减少皮下脂肪、体重和血压[36]。

图4. 国内外大型临床试验证明二甲双胍显著降低糖尿病发生风险
靶器官保护策略解析:多支柱管理模式赋能并发症/合并症管理
高血糖作为核心驱动力,肥胖及相关风险因素协同加剧其对多系统靶器官损伤。因此,2025 IDF指南指出,以危险因素控制为核心的多支柱综合管理成为防治并发症的基石,包括生活方式干预、早期强化血糖控制及多风险因素干预等[1]。在此框架下,二甲双胍展现出超越降糖的广泛获益。大量循证证据证实,其能为T2DM患者带来明确心肾保护作用,包括显著降低动脉粥样硬化性心血管疾病(ASCVD)、心力衰竭发生风险及全因死亡率,延缓CKD进展并减少终末期肾病风险(图5)[37-44]。此外,二甲双胍兼具降压、调脂等风险因素管理作用[45,46],其多效性契合糖尿病并发症多支柱管理原则。在代谢相关脂肪性肝病(MASLD)方面,二甲双胍可改善合并该病的T2DM患者的肝功能与代谢指标[47,48]。研究也提示,在糖尿病视网膜病变(DR)防治中,二甲双胍可降低其发生与进展风险,并可能增强抗VEGF治疗的疗效[49-53]。在体重管理方面,二甲双胍可使超重或肥胖T2DM患者体重轻度下降1.5~2.9 kg[54],与GIP/GLP-1RA联用时可增加实现减重≥15%的可能性[55]。
凭借其确切的疗效、良好的安全性及广泛的额外获益,二甲双胍在国内外指南中均居于核心地位。《国家基层糖尿病防治管理指南(2025)》[56]也明确推荐,二甲双胍应作为T2DM药物治疗的一线首选并贯穿全程,是联合治疗中不可或缺的基础药物。总之,二甲双胍全面覆盖糖尿病事件链全程管理,是实现糖尿病综合管理目标的重要基石。
总结
在T2DM管理中,二甲双胍凭借其全球可获得性、疗效确切、安全性良好、低血糖风险低、成本效益显著、明确的长期心血管获益及多个靶器官保护作用,被2025 IDF指南推荐作为一线单药治疗及联合治疗的基础,并推荐其用于糖尿病预防。我国《国家基层糖尿病防治管理指南(2025)》也明确,二甲双胍是T2DM治疗的一线首选和全程联合治疗的基石,若无禁忌且耐受,应长期保留于治疗方案中。在目前糖尿病治疗药物日益丰富的背景下,血糖管理常需联合用药,而二甲双胍在这一过程中仍具有不可替代的重要地位。
注:二甲双胍在中国尚未获批治疗糖尿病前期、MASLD、DR及降低体重的适应症,本文仅供医疗卫生人士学术交流。
参考文献
1. Ceriello A, et al. Diabetes Res Clin Pract. 2025; 222 Suppl 1: 112152.
2. Garber AJ, et al. Am J Med. 1997; 103(6): 491-497.
3. Kalyani RR, et al. JAMA. 2025; 334(11): 984-1002.
4. Adler AI, et al. Lancet. 2024; 404(10448): 145-155.
5. Chow CK, et al. Lancet Diabetes Endocrinol. 2018; 6(10): 798-808.
6. Solini A, Tricò D. Diabetes Obes Metab. 2024; 26 Suppl 3: 20-30.
7. Choi JG, et al. Ann Intern Med. 2022; 175(10): 1392-1400.
8. Jia S, et al. Acta Diabetol. 2021; 58(1): 5-18.
9. Hemmingsen B, et al. BMJ. 2012; 344: e1771.
10. Zinman B, et al. N Engl J Med. 2015; 373(22): 2117-2128. EMPA-REG OUTCOME
11. Neal B, et al. N Engl J Med. 2017; 377(7): 644-657. CANVAS
12. Wiviott SD, et al. N Engl J Med. 2019; 380(4): 347-357. DECLARE–TIMI 58
13. Cannon CP, et al. N Engl J Med. 2020; 383(15): 1425-1435. VERTIS CV
14. Bhatt DL, et al. N Engl J Med. 2021; 384(2): 129-139. SCORED
15. Pfeffer MA, et al. N Engl J Med. 2015; 373(23): 2247-2257. ELIXA
16. Marso SP, et al. N Engl J Med. 2016; 375(4): 311-322. LEADER
17. Marso SP, et al. N Engl J Med. 2016; 375(19): 1834-1844. SUSTAIN-6
18. Holman RR, et al. N Engl J Med. 2017; 377(13): 1228-1239. EXSCEL
19. Gerstein HC, et al. Diabetes Obes Metab. 2018; 20(1): 42-49. REWIND
20. Hernandez AF, et al. Lancet. 2018; 392(10157): 1519-1529. Harmony Outcomes
21. Husain M, et al. N Engl J Med. 2019; 381(9): 841-851. PIONEER 6
22. Gerstein HC, et al. N Engl J Med. 2021; 385(10): 896-907. AMPLITUDE-O
23. Ruff CT, et al. Nat Med. 2022; 28(1): 89-95. FREEDOM-CVO
24. McGuire DK, et al. Diabetes Obes Metab. 2023; 25(7): 1932-1941. SOUL
25. Nicholls SJ, et al. Am Heart J. 2024; 267: 1-11. SURPASS-CVOT
26. McGuire DK, et al. JAMA Cardiol. 2021; 6(2): 148-158.
27. Sattar N, et al. Lancet Diabetes Endocrinol. 2021; 9(10): 653-662.
28. Li G, et al. Lancet. 2008; 371(9626): 1783-1789.
29. Cai X, et al. BMJ. 2020; 370: m2297.
30. Campbell MD, et al. Nat Rev Endocrinol. 2020; 16(7): 395-400.
31. Madsen KS, et al. Cochrane Database Syst Rev. 2019; 12(12): CD008558.
32. Knowler WC, et al. N Engl J Med. 2002; 346(6): 393-403.
33. Zhang L, et al. Lancet Diabetes Endocrinol. 2023; 11(8): 567-577.
34. Hamman RF, et al. Diabetes Care. 2006; 29(9): 2102-2107.
35. Diabetes Prevention Program Research Group, et al. Lancet. 2009; 374(9702): 1677-1686.
36. Mohan M, et al. Eur Heart J. 2019; 40(41): 3409-3417.
37. Hong J, et al. Diabetes Care. 2013; 36(5): 1304-1311.
38. Kooy A, et al. Arch Intern Med. 2009; 169(6): 616-625.
39. Roussel R, et al. Arch Intern Med. 2010; 170(21): 1892-1899.
40. He S, et al. J Diabetes Res. 2021; 2021: 5534387.
41. Chun KH, et al. Diabetes Metab. 2024; 50(1): 101504.
42. Yang A, et al. Pharmaceuticals (Basel). 2022; 15(9): 1140.
43. Lin YL, et al. Pharmaceuticals (Basel). 2025; 18(1): 95.
44. Agur T, et al. Cardiovasc Diabetol. 2025; 24(1): 97.
45. Sin HY, et al. Arch Pharm Res. 2011; 34(1): 99-107.
46. Gillani SW, et al. J Pharm Bioallied Sci. 2021; 13(1): 76-82.
47. Feng WH, et al. J Diabetes Investig. 2019; 10(2): 399-407.
48. Liu W, et al. Biomedicines. 2025; 13(6): 1315.
49. Maleškić S, et al. Acta Med Acad. 2017; 46(2): 116-123.
50. Li Y, Ryu C, et al. J Diabetes Res. 2018; 2018: 2801450.
51. Fan YP, et al. J Diabetes Res. 2020; 2020: 9161039.
52. Uwimana A, et al. Medicine (Baltimore). 2022; 101(42): e31266.
53. Shao Y, et al. Acta Diabetol. 2022; 59(4): 553-559.
54. Ji L, et al. PLoS One. 2013; 8(2): e57222.
55. Małecki MT, et al. Diabetes Care. 2023; 46(12): 2292-2299.
56. 基本公共卫生服务项目基层糖尿病防治管理办公室, 中华医学会糖尿病学分会. 中华内科杂志. 2025; 64(12): 1169-1186. 2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言