编者按
近期,52岁的T先生收到一份出乎意料的“诊断书”——T2DM。报告上的数字让他心头一紧:糖化血红蛋白(HbA1c)7.9%,空腹血糖(FPG)高达9.2 mmol/L。和许多新确诊的患者一样,面对未来漫长的控糖之路,他感到些许迷茫与担忧:该如何开始?治疗能否既有效又安全?
在诊室里,医生为他制定了一个清晰的起始方案:直接二甲双胍联合使用森格列汀。经过一段时间规范用药后,复诊结果显示,其血糖得到了有效且平稳的控制,治疗效果理想,也为后续长期管理奠定了良好基础。而这个看似简单的治疗决策背后,恰恰体现了当前对于新诊断T2DM管理的核心理念——早期联合治疗!
为深入剖析这一理念,《国际糖尿病》特邀武汉大学人民医院高凌教授,围绕新诊断T2DM患者的管理挑战、早期联合治疗的临床价值、治疗时机与人群选择,以及“森格列汀+二甲双胍”这对“控糖优选CP”的独特优势展开深度访谈,旨在为临床实践提供兼具前瞻性与实用性的管理参考。
《国际糖尿病》
在临床实践中,新诊断T2DM患者并不少见。请您谈谈这部分患者的血糖控制现状,以及在管理方面仍面临哪些主要挑战?

临床实践中,新诊断的T2DM患者数量较多,且呈现逐渐增多的趋势,在整体糖尿病人群中占比已超过一半[1]。然而,该人群早期血糖控制水平普遍不理想,HbA1c≥7.0%的比例高达63.2%;即使治疗1年后,仍有约31.5%的患者未达到血糖控制目标[2]。
糖尿病是一种终身性疾病,若在诊断后一年内HbA1c控制不佳,则未来发生微血管与大血管并发症及死亡的风险将显著增加[3]。因此,对于新诊断的T2DM患者,实施早期血糖强化管理至关重要且十分必要。
《国际糖尿病》
近年来,早期联合治疗逐渐成为临床共识。您如何看待这一策略的临床价值?尤其对于新诊断T2DM患者而言,早期联合治疗能带来哪些更好获益?

《中国糖尿病防治指南(2024版)》[4]指出,早期良好的血糖控制具有重要意义,早期联合是实现良好血糖控制的重要手段(A)。早期良好控糖不仅有助于保护β细胞功能,利于远期血糖控制,还可通过代谢记忆或遗留效应减少远期并发症,改善患者预后。
其中“代谢记忆”或“遗留效应”的证据来源于著名的UKPDS研究。该研究致力于探讨新诊断T2DM患者的治疗策略,在其随机对照研究后续10年的随访中,与常规治疗组相比,强化治疗组心血管等并发症发生率显著降低[5]。在随后10年及14年的观察性研究中,尽管两组均未进行强化治疗,但原强化治疗组的心血管事件(如心肌梗死)和全因死亡风险仍持续低于原常规治疗组[6]。这一结果表明,对于新诊断T2DM患者,早期良好血糖控制带来的心肌梗死和全因死亡风险降低及微血管获益几乎是终身的。
此外,针对新诊断 T2DM 患者的VERIFY 研究[7]显示,与传统单药起始的阶梯治疗相比,二肽基肽酶-4抑制剂(DPP-4i)联合二甲双胍的起始联合治疗减低HbA1c水平幅度更大,且5年随访期内显著降低血糖控制失败的风险达49%,同时不增加低血糖风险。
《国际糖尿病》

新诊断T2DM患者的治疗“黄金窗口”多集中于诊断后的1年内。在这一阶段,患者体内仍保留一定数量的β细胞功能。尽管在糖尿病发生过程中,β细胞功能受到抑制(表现为去分化),但多数并未转化为α细胞或发生不可逆的凋亡,其功能仍具有可逆性,被称为“休眠β细胞”。若在疾病早期通过有效干预,纠正促使β细胞去分化的病理因素,则可使其重新分化为成熟β细胞,恢复胰岛素分泌功能,从而在病因层面改善血糖控制[9]。
在临床特征方面,《成人2型糖尿病口服降糖药联合治疗专家共识(2025版)》[10]建议:当新诊断T2DM患者 HbA1c≥7.5% 时,推荐以二甲双胍为基础的起始联合治疗。其中,DPP-4i联合二甲双胍是一种循证充分的早期起始联合策略,在疗效、安全性及耐受性方面均表现良好,尤其适用于新诊断患者。特别是对于老年患者,该方案低血糖风险较低;而对于不能耐受高剂量二甲双胍的患者,采用中低剂量二甲双胍联合DPP-4i,有助于在保证降糖效果的同时,减少胃肠道不良反应,提高治疗依从性。
《国际糖尿病》
作为新型DPP-4i,森格列汀在疗效与安全性方面均表现出色。具体到森格列汀与二甲双胍这对“搭档”应用时,您认为其是否具备更突出的“组合优势”?

森格列汀是全新一代高选择性DPP-4i,在西格列汀的结构基础上进行优化研发,具有更高的靶点亲和力和更强的酶抑制能力[11]。药效学研究显示,森格列汀50 mg即可实现与西格列汀100 mg相当的DPP-4抑制效果,且抑制持续时间更长[12]。这不仅赋予其单药治疗的优势,也为联合治疗提供了坚实基础,使其在与二甲双胍联合应用时展现出更突出的“组合优势”,为患者带来更高效的血糖管理。
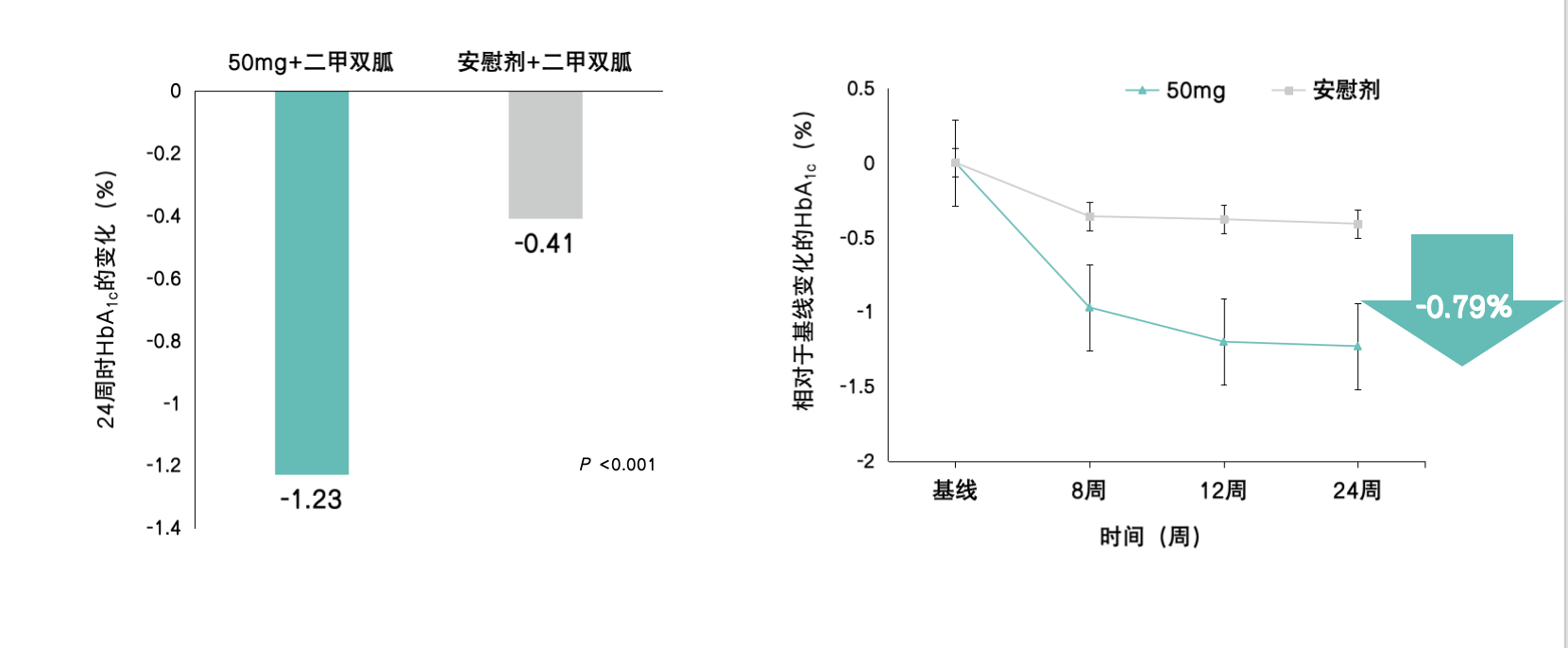
大幅降低HbA1c水平:森格列汀联合二甲双胍的III期临床研究[13]显示,该联合方案治疗24周,HbA1c降低达1.23%,相比安慰剂组降低0.79%,具有统计学差异及显著临床意义。从既往公布的多个同类药物联合二甲双胍治疗的III期数据来看,这一降糖幅度处于领先地位。
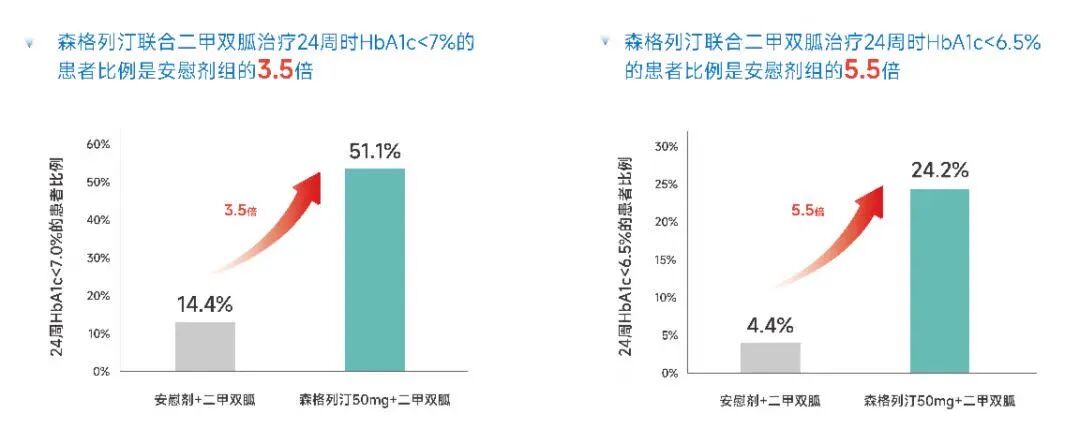
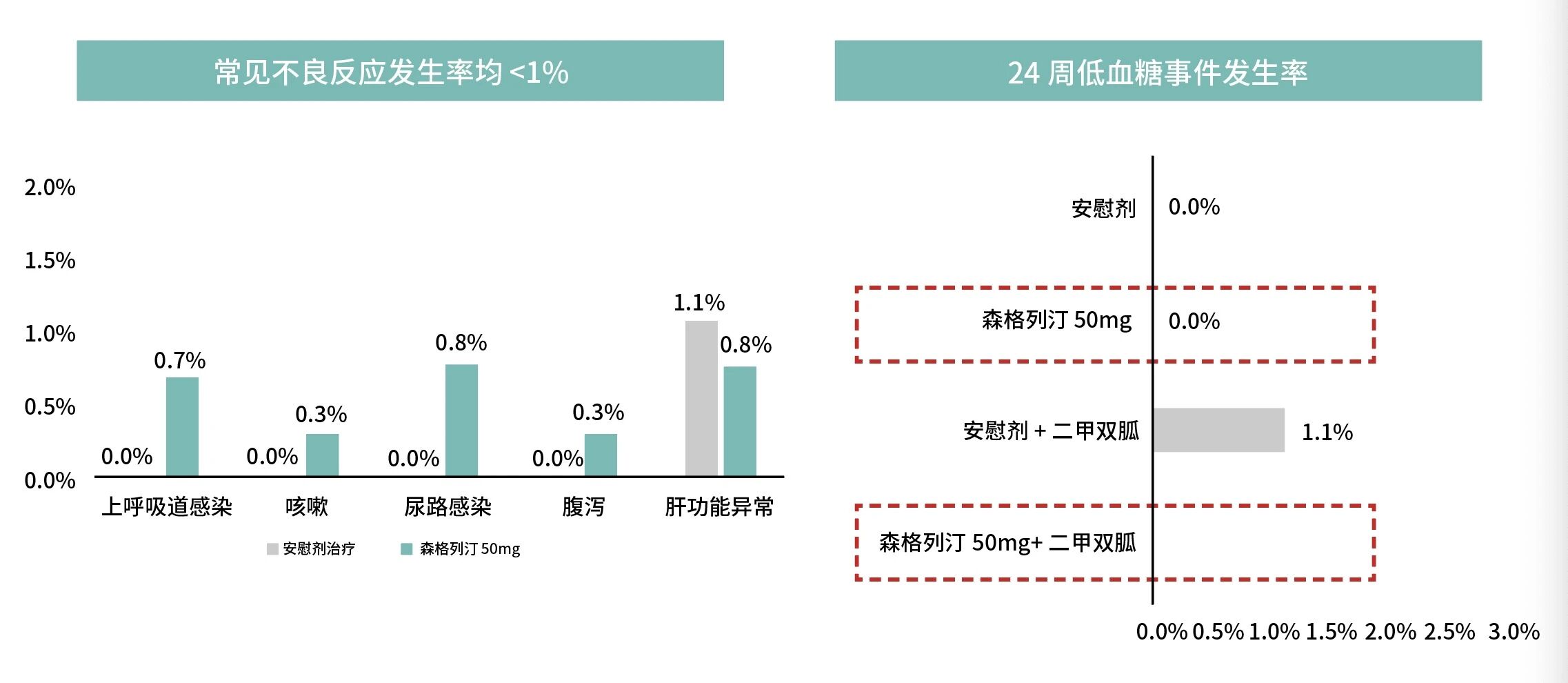
显著改善β细胞功能:III期临床研究[13]显示,森格列汀联合二甲双胍治疗第24周扣除安慰剂效应后,胰岛β细胞功能较基线分别提升16.2%(100 mg组)和14.1%(50 mg组),提示该联合方案有助于保护β细胞功能,并可能延缓疾病进展。

专家简介

武汉大学人民医院内分泌科主任,教授,二级主任医师,博士研究生导师
中华医学会糖尿病分会委员
中国医师协会内分泌代谢分会委员
武汉医学会内分泌分会主委
湖北省医学会内分泌分会副主委
湖北省医师协会内分泌代谢分会副主委
武汉大学学报医学版编委, 临床内科杂志编委
在世界级顶刊Lancet等世界一流期刊发表多篇第一作者或者通讯作者论文,他引单篇最高达300次以上
参考文献:
[1]Li Y, et al. BMJ. 2020; 369: m997.
[2]Cai X, et al. J Diabetes Investig . 2020; 11(1): 151-161.
[3]Laiteerapong N, et al. Diabetes Care. 2019; 42(3): 416-426.
[4]中华医学会糖尿病学分会 . 中国糖尿病防治指南(2024 版)[J]. 中华糖尿病杂志, 2025, 17(1):16-139. DOI: 10.3760/cma.j.cn115791-20241203-00705.
[5]Holman RR, Paul SK, Bethel MA, et al. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med. 2008 Oct 9;359(15):1577-89. doi: 10.1056/NEJMoa0806470. Epub 2008 Sep 10. PMID: 18784090.
[6]Adler AI, Coleman RL, Leal J, et al. Post-trial monitoring of a randomised controlled trial of intensive glycaemic control in type 2 diabetes extended from 10 years to 24 years (UKPDS 91). Lancet. 2024 Jul 13;404(10448):145-155. doi: 10.1016/S0140-6736(24)00537-3. Epub 2024 May 18. PMID: 38772405.
[7]Matthews DR, Paldánius PM, Proot P, et al. Glycaemic durability of an early combination therapy with vildagliptin and metformin versus sequential metformin monotherapy in newly diagnosed type 2 diabetes (VERIFY): a 5-year, multicentre, randomised, double-blind trial. Lancet. 2019 Oct 26;394(10208):1519-1529. doi: 10.1016/S0140-6736(19)32131-2. Epub 2019 Sep 18. PMID: 31542292.
[8]刘滟琳,陈国芳,孙洪平,等.《生活方式干预治疗和缓解成人2型糖尿病和糖尿病前期的临床实践指南(2025)》:要点与解读[J].中华糖尿病杂志, 2025, 17(10):1233-1241.DOI:10.3760/cma.j.cn115791-20250714-00348.
[9]《缓解2型糖尿病中国专家共识》编写专家委员会. 中国全科医学. 2021;24(32):4037-4048.
[10]中国医师协会内分泌代谢科医师分会 . 成人 2 型糖尿病口服降糖药联合治疗专家共识
(2025版)[J]. 中华内科杂志, 2025, 64(8): 707-722. DOI: 10.3760/cma.j.cn112138-20250515-00279.
[11]Ji L, Lu J, Gao L, et al. Efficacy and safety of cetagliptin as monotherapy in patients with type 2 diabetes: A randomized, double-blind, placebo-controlled phase 3 trial. Diabetes Obes Metab. 2023 Dec;25(12):3671-3681. doi: 10.1111/dom.15261. Epub 2023 Sep 3. PMID: 37661308.
[12]Zhou C, Zhou S, Wang J, et al. Safety, tolerability, pharmacokinetics and pharmacokinetic-pharmacodynamic modeling of cetagliptin in patients with type 2 diabetes mellitus. Front Endocrinol (Lausanne),2024,15:1359407.
[13]Ji L, Lu J, Gao L, et al. A randomized, double-blind, placebo controlled, phase 3 trial to evaluate the efficacy and safety of cetagliptin added to ongoing metformin therapy in patients with uncontrolled type 2 diabetes with metformin monotherapy. Diabetes Obes Metab. 2023 Dec;25(12):3788-3797. doi: 10.1111/dom.15274. Epub 2023 Sep 19. PMID: 37724698. 2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言