
编者按
第84届美国糖尿病协会(ADA)年会于6月21日至24日在美国奥兰多召开,众多1型糖尿病(T1DM)领域的最新研究进展成为热议焦点;这些研究聚焦于早期筛查、干预和预测等,为T1DM诊疗格局更新带来了新的曙光。《国际糖尿病》特邀中南大学湘雅二医院周智广教授第一时间在ADA年会现场分享T1DM领域的最新研究成果,深入探讨中国T1DM的诊疗现状及患者需求,并展望T1DM未来诊疗方向。
《国际糖尿病》
今年ADA大会上,T1DM领域的多项创新研究成果引起了广泛关注。请您分享下早期筛查、干预和预测等领域的重磅前沿研究进展,这些研究对T1DM诊疗格局的更新有何影响?
周智广教授:本次ADA年会公布了多项T1DM诊疗相关研究进展,涵盖早期筛查、早期干预、疾病进展与预测等多个方面。这些研究进展不仅丰富了我们对T1DM早期筛查和干预的理解,也为临床医生提供了新的视角和工具,以更有效地制定个体化创新管理的策略。具体可分为国外筛查和干预的临床实践、免疫干预研究最新数据、筛查指标与模型相关研究进展、疾病进展预测等,其中的几项研究令我印象深刻(点击“阅读原文”下载详细研究):
从国外筛查和干预的临床实践来看,自2022年11月美国FDA批准了CD3单抗Teplizumab用于延缓T1DM发病以来,人们对T1DM筛查的兴趣与日俱增。ADA大会中公布了一项旨在识别T1D Exchange质量改进协作中心在自身抗体筛查和Teplizumab管理准备方面的现状研究[1]。这项研究纳入了55个中心,结果发现大多数中心未对T1DM筛查实践做出改变。而在调整筛查实践的中心中,多数制定了筛查T1DM一级亲属的具体流程。与成人中心相比,儿童中心更积极,同时也更有意愿使用Teplizumab(图1)。
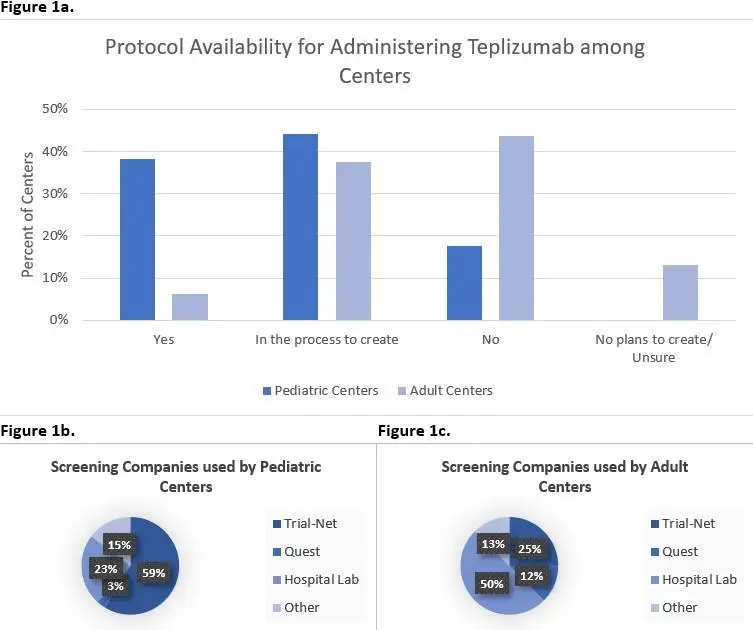
图1. 自身抗体筛查和Teplizumab的管理准备情况分析
在免疫干预研究领域,一项研究针对PROTECT符合方案集的8~17岁新诊断3期T1DM患者进行了分析[2],结果发现相比于对照组,Teplizumab治疗组的β细胞功能保护更好,同时胰岛素使用剂量更少(图2)。而另一项研究则评估了使用Teplizumab治疗期间的感染风险[3]。研究显示,使用Teplizumab患者的整体感染率与对照组并无显著差异,进一步支持CD3单抗Teplizumab是免疫调节而非免疫抑制。

图2. PROTECT符合方案集的8~17岁新诊断3期T1DM患者分析
在筛查指标与模型领域,有3项研究同样值得关注。第一项研究是用于筛查识别和预测高风险人群的持续葡萄糖监测(CGM)指标研究[4],这项同时也入选了ADA主席精选摘要。研究结果提示,CGM指标不仅有助于预测T1DM进展,还可对短期内发展为T1DM的风险级别进行分层,并协助筛选潜在的适合纳入预防试验的人群(图3)。第二项研究则通过T1DM遗传风险评分(简称GRS2,其结合了67个增加T1DM风险的HLA和非HLA单核苷酸多态性)分析预测患者对免疫治疗的反应[5];进一步分析TN10研究(n=44 Teplizumab,n=32 安慰剂)发现,随着GRS2增加,安慰剂组T1DM风险增加,而治疗组T1DM风险似乎减少,且GRS2≥13的人群具有更大治疗效益。总之,这项研究表明遗传风险评分有助于筛选T1DM预防治疗的可能获益人群。第三项研究[6]则以多项逻辑回归模型和二项模型组合为基础,开发出多基因风险评分(PRS)模型,可通过非侵入性方法进行早期差异性筛查,能够较好预测T1DM风险。
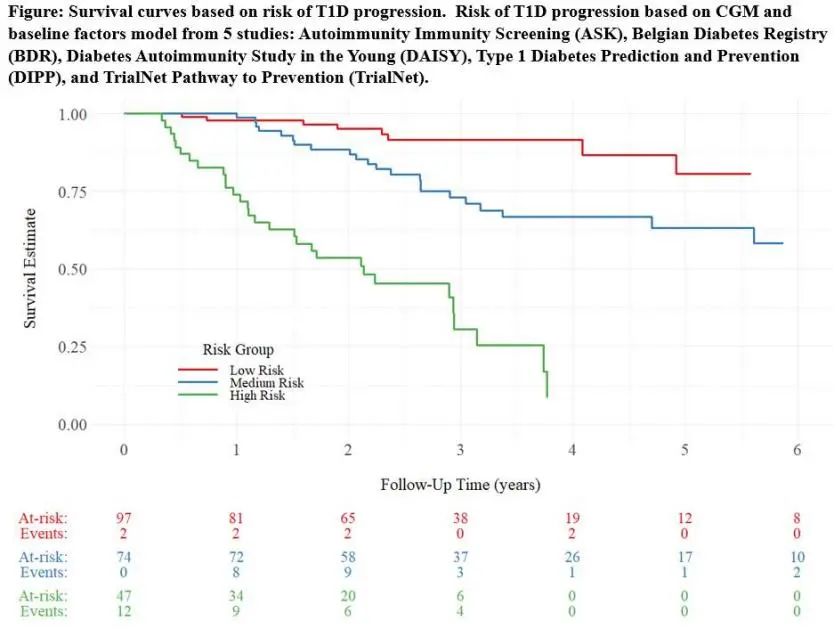
在T1DM疾病进展预测方面,一项旨在探讨葡萄糖拐点在自身抗体阳性T1DM进展中变异性的研究[7],结果表明,诊断前年龄较大和较肥胖的个体具有较早的AUC血糖拐点(图4)。另一项研究则分析了筛查时存在代谢异质性的个体在T1DM进展中的表现[8],研究通过空腹血糖和空腹C肽乘积(fgxfp)的中位数进行分层,发现fgxfp较高组的基线C肽显著更高,表现为葡萄糖C肽反应曲线(GCRC)的形态更宽且位置更偏右;在发展为T1DM的过程中(从基线到诊断),fgxfp较高组GCRC向左上方移动,而另一组则主要向上移动(图5)。


图5. 筛查时存在代谢异质性的个体在T1DM进展中的表现
从ADA公布的这些研究数据可以看到,目前在T1DM的早期筛查、预测、早期干预等方面已经取得了令人瞩目的成果和重要进展,为T1DM诊疗策略提供了重要参考价值。
《国际糖尿病》
然而我国T1DM的诊疗现状却并不容乐观,请您结合临床经验分享下我国的T1DM诊疗现状和痛点?立足当下,中国当前还有哪些未被满足的医疗需求?
周智广教授:目前T1DM全球患病率呈现持续上升趋势。2022年全球T1DM患病总人数达875万,其中中国超过44万,排名全球前列[9];预计到2040年,全球患病率增长60%~107%,患者数将达1350万~1740万[10]。而中国人口基数大、患病人数多、发病率增长快,<15岁人群发病率在过去的20年里增长了近4倍[11];此外,中国成人隐匿性自身免疫糖尿病(LADA)患者人数约1000万,居世界首位[11]。在此背景下,面对T1DM病因的复杂性及疾病进程的异质性,诊断和防治工作无疑面临着重重挑战。目前而言,T1DM诊疗领域仍有多方面痛点和未被满足的需求:
首先,诊断延迟、诊断时合并糖尿病酮症酸中毒(DKA)比例高。研究发现,欧美等高收入国家新诊断T1DM患儿的DKA发生率平均约30%[12],而中国这一比例更高。由中南大学湘雅二医院牵头的一项覆盖中国7个行政区域,涵盖所有年龄段的T1DM患者的CD1S研究结果显示[13],中国新诊断T1DM患者合并DKA发生比例很高,10岁以下DKA起病的比例超过50%,而诊断延迟是DKA高发的重要原因。
其次,漏诊和误诊率高。研究发现超过4成的T1DM患者被遗漏[14],且30岁以上T1DM患者的误诊比例高达50%,而漏诊已成为导致患者死亡的重要原因[15,16]。
再者,现有的治疗手段有限。T1DM现有治疗以胰岛素为主,无法从根本上终止或纠正T1DM的主要病因——免疫调节机制紊乱[17];且有研究发现,胰岛素强化治疗可能不能改变T1DM的胰岛β细胞功能衰退进程[18]。此外,临床上胰岛素使用往往存在注射负担、依从性差、低血糖风险、体重增加、心理障碍等问题[19-21]。
最后,虽然胰岛素制剂及输送装置不断改进,但现有治疗策略下的血糖控制远不理想,患者急慢性并发症比例较高。CD1S研究发现[13],中国T1DM患者仅有12%的糖化血红蛋白(HbA1c)达标,患者常合并心血管危险因素,超过60%的患者至少合并一种慢性并发症,甚至在病程10年以上的患者中80%存在慢性合并症。
因此,我们更要奋起直追,无论是T1DM早期筛查,还是T1DM患者管理,亦或是治疗手段,都应不断地更新调整,追赶世界T1DM领域的发展水平。
《国际糖尿病》
您认为在临床实践中应该采取哪些创新策略来更有效地应对这些挑战?
周智广教授:为了解决上述诊疗的痛点,目前诊疗实践提倡防治关口前移,通过早筛早诊早干预的新型疾病管理模式来改善患者的预后。
早筛早诊方面,中国新版T1DM指南[11]增添了T1DM分期,首次提出了亚临床T1DM的概念。基于新的分期分类系统,使防治前移成为可能:早期筛查T1DM高风险人群、及时提供干预,为T1DM诊疗提供新的机会窗口。通过早筛早诊,可有效识别出症状前T1DM患者,显著降低DKA发生率,为医疗教育和评估提供更多时间,改善发病时临床表现。
不仅中国新版T1DM指南,包括最新的ADA指南、ISPAD指南等在内的多项国际指南共识均强调早期筛查的重要性[22,23],并推荐对T1DM高危人群进行筛查。在本次ADA大会上,专家们特别讨论了早筛策略,并建议积极开展高危人群筛查工作。由JDRF牵头的多个国际权威协会组织共同制定的抗体阳性3期前T1DM的筛查监测共识,也最新发表于Diabetes Care和Diabetologia。
早期干预方面,新型免疫疗法已成为研究热点和重点;新型靶点的发现为T1DM指明新方向,目前相关药物包括靶向T细胞、B细胞、调节性T细胞和β细胞保存的药物等,其中最为耀眼的是CD3单抗Teplizumab。
前文已经提及,Teplizumab是2022年11月首个被美国FDA批准用于延缓T1DM发病的免疫治疗药物,研究证实其可延缓3期T1DM发病近3年,且安全性和耐受性良好[24]。PROTECT研究进一步地拓展了新诊断3期T1DM患者的治疗视野,研究结果显示Teplizumab可显著延缓新诊断T1DM患者的胰岛β细胞功能下降[25]。基于研究数据,2024年ADA指南建议[22],对于年龄≥8岁的2期T1DM患者,应考虑给予Teplizumab的治疗,以延缓症状性的T1DM,即3期T1DM的发生。
《国际糖尿病》
确实如您所说,早期筛查与干预对于T1DM而言非常重要。那么结合中国临床实践,请您谈谈目前国内的筛查现状如何?未来应如何发展具有中国特色的筛查策略?
周智广教授:我国T1DM高危人群筛查也已开展并取得一定成效,但尚未达到欧美等发达国家水平,因而我们应更积极启动高危人群的筛查工作。T1DM高危人群包括T1DM患者的一级亲属和携带HLA易感基因的普通人群[26,27]。研究证实,相对于普通人群,T1DM一级亲属的发病风险增加10倍以上[26,27]。同时,需要注意,中国LADA患者人数居于世界首位,而LADA遗传特征也与T1DM类似[11]。因此,考虑到人群差异和成本效益,未来的中国人群筛查策略可能与国外有所不同:推荐首选T1DM一级亲属进行筛查;结合中国T1DM特点,建议可考虑包含LADA和经典T1DM先证者的一级亲属。
目前主要的筛查手段包括自身抗体、易感基因和代谢指标的联合检测等,其中胰岛自身抗体最为有效、应用最为广泛。JDRF国际共识强调[28],通过胰岛自身抗体筛查可及时发现无症状T1DM患者,对有效控制疾病进展具有重要意义。2024 ADA指南及中国T1DM新版指南[11,22]均推荐对高危人群进行4种抗体筛查,包括胰岛素自身抗体(IAA)、谷氨酸脱羧酶自身抗体(GADA)、蛋白酪氨酸磷酸酶自身抗体(IA-2A)以及锌转运体8自身抗体(ZnT8A)。而对于抗体筛查阳性个体,推荐进行进一步血糖指标检测:根据血糖是否异常分为1期T1DM(个体存在≥2个胰岛自身抗体但血糖正常)和2期T1DM(个体存在≥2个胰岛自身抗体且血糖异常,但尚未出现临床症状),且应进一步加强监测与随访。
目前,国内在T1DM的抗体筛查经验、筛查策略与标准方向等尚存在不足,未来需要通过充分实践、探索T1DM高危筛查策略,不断积累和总结经验,采用中心化手段严格控制抗体检测质量,推动筛查监测流程标准化,这是实现早筛早诊策略的关键。此外,应积极引进包括CD3单抗Teplizumab在内的新型药物,使中国T1DM患者享受到世界T1DM领域的先进研究成果,并从中获益。

专家简介
周智广 教授
一级主任医师,博导,湘雅名医国家代谢性疾病临床医学研究中心主任内科学(内分泌与代谢病)国家重点学科带头人,教育部创新团队带头人糖尿病免疫学教育部重点实验室主任中国医师协会内分泌代谢科医师分会名誉会长国家心血管病专家委员会心血管代谢医学专业委员会主任委员湖南省医学会副会长、湖南省医学会内分泌学专业委员会主任委员《中国医师杂志》主编,《中华糖尿病杂志》、《中国动脉硬化杂志》、《Frontiers in Immunology》等杂志副主编,《Diabetes Metabolism Research and Reviews》、《Diabetes Research and Clinical Practice》等5本英文杂志编委。先后承担国家973、863、科技支撑计划、国家重点研发计划及国家自然科学基金重点国际合作项目等国内外糖尿病项目50余项,专注糖尿病免疫诊治和免疫发病机制研究。牵头制定了首部《中国1型糖尿病诊治指南》和《LADA诊疗共识》,发表SCI论文380余篇。培养毕业博士、硕士共186名。获得国家科技进步奖3项及省部级科技奖10项。2001年入选教育部“跨世纪人才”培养计划,1993年起享受国务院政府特殊津贴。参考文献:(上下滑动查看更多)
1. C.Demeterco-berggren, et al. ADA 2024. Abstract 1293-P2. K.C.Herold, et al. ADA 2024. Abstract 70-OR3. S.E.GitelmanADA, et al. 2024. Abstract 728-P4. P.Calhoun, et al. ADA 2024. Abstract 74-OR5. M.J.Redondo, et al. ADA 2024. Abstract 68-OR6. L. Mendizabal, et al. ADA 2024. Abstract 2002-LB7. H.M.Ismail, et al. ADA 2024. Abstract 330-OR8. E.K.Sims, et al. ADA 2024. Abstract 1460-P9. International Diabetes Federation Diabetes Atlas . 2022– Type 1 diabetes numbers in children and adults.10. Guo SJ, et al. Lancet Diabetes Endocrinol. 2022 Oct;10(10):688-689.11. 中国医师协会内分泌代谢科医师分会. 中华医学杂志. 2021;101(38): 3077-91.12. Cherubini V, et al. Diabetologia. 2020 Aug;63(8):1530-1541.13. Deng C, et al. Diabetes Metab Res Rev. 2024 Mar;40(3):e379614. The Lancet Regional Health-Europe. Lancet Reg Health Eur. 2023;29:100661.15. Muñoz C, et al. Clin Diabetes. 2019 Jul;37(3):276-281.16. Guo SJ,et al. Lancet Diabetes Endocrinol. 2022 Oct;10(10):688-689.17. 罗说明,周智广. 中国医师杂志. 2023; 25(3)321-324.18. McVean J, et al. JAMA. 2023 Mar 28;329(12):980-989.19. Insel RA, er al.Diabetes Care 2015;381964–1974.20. Chua,et al .Asian J Pharm Clin Res, 12(12) 2019:176-182.21. Wisting L, et al. BMJ Open Diabetes Res Care. 2016 Jun 23;4(1):e000203.22. Diabetes Care 2024;47(Supplement 1)S1–S32823. Besser REJ, et al. Pediatr Diabetes. 2022;23(8):1175-1187.24. Sims EK, et al. Sci Transl Med. 2021 March 03; 13(583)25. Ramos EL, et al. N Engl J Med. 2023;389(23):2151-2161.26. Maahs DM, et al. Endocrinol Metab Clin North Am. 2010 Sep;39(3):481-97.27. Parkkola A, et al. Diabetes Care. 2013 Feb;36(2):348-54.28. Insel RA, et al. Diabetes Care. 2015;38(10):1964-1974快讯视频•精彩来袭
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。4M编号:MAT-CN-2413527 批准日期:2024年6月 V.1.0 2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言