在代谢科学领域,白色脂肪组织(White Adipose Tissue,WAT)的认知正在发生根本性重塑。过去它被视为一种被动的能量储存库,如今已被公认为集代谢、内分泌和免疫功能于一体的高度动态器官。
2026年5月发表于Diabetologia的重磅综述,基于欧洲糖尿病研究协会(EASD)2025年Camillo Golgi奖得主、瑞典卡罗林斯卡学院Mikael Rydén教授的主题讲座整理,由教授本人梳理撰写。这篇综述明确揭示:脂肪细胞的更新、异质性以及与免疫系统的“对话”,是决定人体维持代谢健康还是走向2型糖尿病的关键。
长期以来,白色脂肪在代谢研究中被边缘化,被认为只是被动储存能量的“惰性组织”,重要性远不及肝脏、骨骼肌、胰腺等器官。早期肥胖相关疾病研究,也多将矛头指向经典靶组织的胰岛素异常,忽视了WAT的作用。
近几十年,这一传统认知被彻底颠覆:WAT具有高度动态性、内分泌活性和免疫复杂性,是代谢调节的核心。它能通过调控脂质储存、脂肪细胞更新和细胞间通讯,缓冲能量波动,保护其他器官免受脂质过载的损伤。
具体来讲,健康的白色脂肪是“代谢缓冲器”,而功能异常的白色脂肪会变成“代谢负担”。当脂肪细胞储存能力超载、脂质周转受损时,会引发组织缺氧、纤维化和慢性低度炎症,进而诱发胰岛素抵抗、心血管疾病等一系列代谢问题。
更值得关注的是,肥胖程度相似的人,代谢风险可能天差地别——“代谢健康型肥胖(MHO)”的存在,充分说明脂肪的“质量”(功能状态)比“数量”(储存量)更重要。同时,脂肪分布也会影响代谢结局:内脏脂肪相较皮下脂肪,更易引发血脂异常、肝脏胰岛素抵抗,这与其直接汇入门静脉循环的解剖特征密切相关。
二、肥胖难逆转的真相:脂质周转与“调定点”在作祟
肥胖研究的核心问题之一:为何肥胖一旦形成便难以逆转?这背后并非单纯源于“意志力不足”或简单的热量摄入与消耗失衡,而是WAT的两大核心特性在主导——脂质周转和肥胖“调定点”。
01、脂质周转:决定体重走向的关键动力学
脂质周转,是指脂肪细胞内脂质储存与动员的动态循环,受严格调控且存在显著个体差异。
能量平衡仅调控短期体重波动,而脂质周转决定微小、不易察觉的能量盈余能否长期累积囤积;
脂质周转障碍时,脂肪更易滞留储存,难以动员分解,即便没有暴饮暴食,体重也会渐进性升高;
该机制并非否定经典“能量平衡”理论,而是补充了肥胖的深层生物学机制——微小能量失衡如何被机体留存、并随时间持续放大。
02、脂肪细胞更新特点:只增不减,不可逆
借助14C定年技术,研究证实:成年人脂肪细胞终生处于持续更新状态,平均寿命约为10年,脂肪总量依靠细胞新生与死亡的平衡维持。
肥胖人群脂肪细胞生成速率显著升高,导致细胞总数永久性增加
减重仅能缩小脂肪细胞体积,无法减少脂肪细胞数量数,形成“多而小”的持续性增生状态;
细胞数量只增不减,形成长期肥胖结构基础,反复减重损害心血管代谢健康。
03、肥胖调定点与脂肪记忆
肥胖“调定点”:由脂肪细胞数量和脂质周转能力共同塑造。一旦建立,机体就会倾向于脂质滞留囤积,让减重难以维持。热量限制减重后,脂肪细胞体积缩小,同时呈现激素(瘦素降低)与转录层面的“高脂质亲和力”,形成强大的生理性体重反弹驱动力,这也是单纯生活方式干预长期成功率低的核心原因。
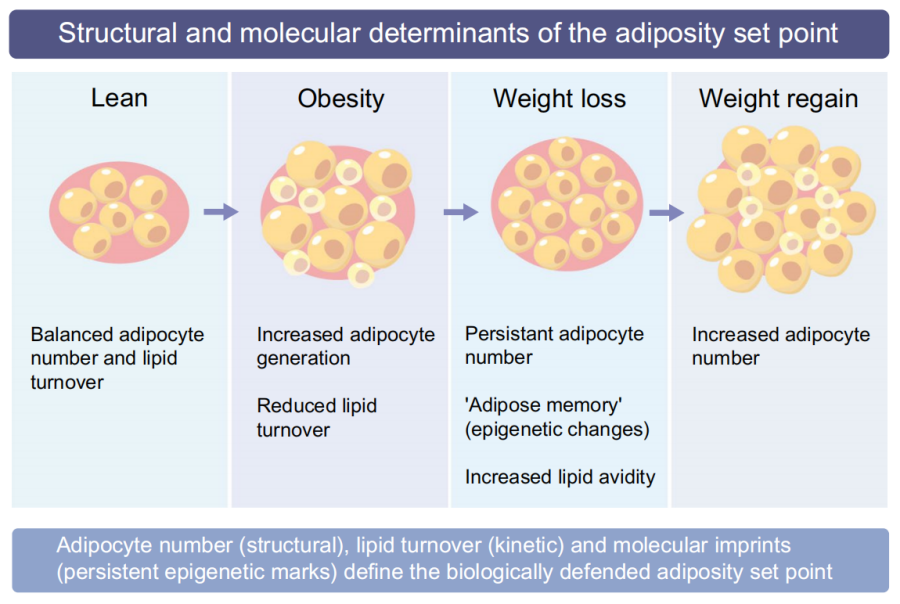
图1. 肥胖调定点的结构与分子决定因素
脂肪记忆:既往营养状态会留下持久的转录和表观遗传改变,限制脂肪细胞对减重、药物干预的响应能力。
二者关联:相互作用、彼此强化,结构特征稳固分子记忆,共同锁住肥胖表型。
表1. 肥胖调定点与脂肪记忆的区别及关联

与代谢疾病的关联:前瞻性研究表明,脂质周转障碍先于代谢疾病发生,可提前预测发病风险。甘油三酯周转变慢、脂解能力下降的个体,更易体重增加、出现糖耐量异常或2型糖尿病。这表明脂肪细胞脂质动员障碍不仅是代谢疾病的标志物,而且很可能是长期体重增加和代谢恶化的促成因素。
三、炎症假说更新:脂肪细胞才是“始作俑者”
长期以来,“炎症驱动脂肪功能异常”是主流观点——认为浸润的白细胞是脂肪组织炎症和胰岛素抵抗的主要原因。但临床实践发现,单纯靶向免疫细胞或炎症因子的抗炎治疗,代谢获益十分有限。
最新的“脂肪细胞优先”理论提出了不同的观点:功能异常的脂肪细胞才是炎症的起始信号。脂肪细胞肥大(Hypertrophy)是促炎信号的触发器——当脂肪细胞肥大时,会承受机械应力和缺氧,进而产生趋化因子(如MCP1/CCL2)招募免疫细胞。此时,炎症不是脂肪功能异常的“原因”,而是“结果”。
多项机制研究进一步佐证:应激状态下的脂肪细胞可分泌CCL2调控免疫细胞募集;脂肪细胞谷氨酰胺代谢改变、肌酸依赖的CCL2表达上调,都将细胞能量代谢与组织炎症紧密关联。
临床治疗启示:若炎症主要由脂肪细胞应激驱动,那么单纯抑制免疫系统效果有限。改善脂肪细胞的脂质周转能力、修复代谢功能,才能从根源上缓解慢性炎症。
四、空间转录组学揭秘:脂肪细胞功能各有“分工”
过去,脂肪细胞被视作“千人一面”的高度均一细胞群体,功能差异仅由细胞大小决定。但这无法解释:为何肥胖程度相近的人群,胰岛素敏感性、炎症水平、干预应答会截然不同。
空间转录组学技术的应用,揭开了脂肪细胞异质性的面纱:人类白色脂肪组织中,至少存在三种主要脂肪细胞状态——AdipoPLIN、AdipoLEP、AdipoSAA,三者各有“分工”且可随代谢环境动态转换:
AdipoPLIN:富集脂质周转相关通路,是脂质代谢调控的核心亚型;
AdipoLEP:主要负责感知脂肪组织质量变化;
AdipoSAA:呈现更强的炎症特征,且与脂肪库分布相关。
三种亚型的空间分布差异,直接影响脂肪组织的功能和个体代谢风险——即使BMI相同,胰岛素应答型脂肪细胞的比例不同,代谢健康状况也会天差地别。同时,不同脂肪细胞亚型占主导的个体,对干预的应答也不同。例如,AdipoPLIN富集的个体,更适合预防脂肪组织不良重塑的干预;而AdipoSAA富集的个体,更易从恢复脂肪细胞代谢灵活性的治疗中获益。
五、内脏脂肪的特殊角色:代谢与免疫的“交叉路口”
WAT分布于人体多个解剖部位,不同脂肪库在发育起源、血管化、神经支配和代谢影响上差异显著。传统皮下/内脏脂肪二分法已无法反映内脏脂肪库内部的高度异质性。
近期针对人类WAT的转录组与空间解析研究显示:皮下、大网膜、肠系膜、腹膜外等不同脂肪库,细胞组成与细胞间通讯模式差异显著,直接决定局部免疫微环境及全身代谢结局。
其中,紧邻结肠的腹膜外WAT尤为特殊,其富含表达血清淀粉样蛋白A(SAA)基因的AdipoSAA 细胞群——这类细胞在皮下脂肪中罕见,却在腹膜外脂肪中占比很高,且呈现先天免疫调节的转录特征,而非经典的脂质储存功能。
这一发现挑战了以往主流观点:脂肪组织免疫激活并非主要由浸润白细胞驱动,特定脂肪库中的脂肪细胞本身是局部免疫反应的调控者。
更有趣的是,腹膜外脂肪紧邻肠道,肠道微生物衍生信号(如脂多糖)可直接诱导AdipoSAA表达激活。这表明,AdipoSAA可能作为“哨兵”,连接肠道稳态与全身炎症,将肠道屏障信号转化为脂肪细胞驱动的免疫激活——这也解释了为何肠道健康与代谢疾病密切相关。
六、治疗思路启发与未来展望
综上,WAT早已不是单纯的“惰性储能罐”,而是结构动态、细胞异质、兼具代谢与免疫调控的核心脏器。对它的深入研究,不仅重塑了我们对肥胖、糖尿病的认知,也为代谢疾病个体化精准治疗提供了坚实的机制依据。未来,靶向脂肪细胞本身,或许有望实现代谢疾病的长效防控。
未来重点研究与转化方向:
治疗理念转型:未来的治疗策略不应仅仅关注体重数字下降,而应致力于恢复脂肪细胞的功能(质量),例如正常化脂质周转、重置脂肪细胞状态,从单纯以减重为中心,转向以脂肪组织修复为核心;
个体化精准医疗:通过分析个体的脂肪细胞组成(如AdipoPLIN/AdipoSAA的比例),未来可能预测患者对特定药物(如GLP-1受体激动剂)的反应,从而实现分型施治;
开放科学资源共建:科研团队已搭建脂肪组织知识门户(adiposetissue.org)与哺乳动物脂肪组织知识门户(MATKP;matkp.org)两大开放共享平台,整合多队列、多组学数据,助力推动领域协同研究,加速基础成果向临床转化。 2 comments
2026年5月发表于Diabetologia的重磅综述,基于欧洲糖尿病研究协会(EASD)2025年Camillo Golgi奖得主、瑞典卡罗林斯卡学院Mikael Rydén教授的主题讲座整理,由教授本人梳理撰写。这篇综述明确揭示:脂肪细胞的更新、异质性以及与免疫系统的“对话”,是决定人体维持代谢健康还是走向2型糖尿病的关键。

长期以来,白色脂肪在代谢研究中被边缘化,被认为只是被动储存能量的“惰性组织”,重要性远不及肝脏、骨骼肌、胰腺等器官。早期肥胖相关疾病研究,也多将矛头指向经典靶组织的胰岛素异常,忽视了WAT的作用。
近几十年,这一传统认知被彻底颠覆:WAT具有高度动态性、内分泌活性和免疫复杂性,是代谢调节的核心。它能通过调控脂质储存、脂肪细胞更新和细胞间通讯,缓冲能量波动,保护其他器官免受脂质过载的损伤。
具体来讲,健康的白色脂肪是“代谢缓冲器”,而功能异常的白色脂肪会变成“代谢负担”。当脂肪细胞储存能力超载、脂质周转受损时,会引发组织缺氧、纤维化和慢性低度炎症,进而诱发胰岛素抵抗、心血管疾病等一系列代谢问题。
更值得关注的是,肥胖程度相似的人,代谢风险可能天差地别——“代谢健康型肥胖(MHO)”的存在,充分说明脂肪的“质量”(功能状态)比“数量”(储存量)更重要。同时,脂肪分布也会影响代谢结局:内脏脂肪相较皮下脂肪,更易引发血脂异常、肝脏胰岛素抵抗,这与其直接汇入门静脉循环的解剖特征密切相关。
二、肥胖难逆转的真相:脂质周转与“调定点”在作祟
肥胖研究的核心问题之一:为何肥胖一旦形成便难以逆转?这背后并非单纯源于“意志力不足”或简单的热量摄入与消耗失衡,而是WAT的两大核心特性在主导——脂质周转和肥胖“调定点”。
01、脂质周转:决定体重走向的关键动力学
脂质周转,是指脂肪细胞内脂质储存与动员的动态循环,受严格调控且存在显著个体差异。
能量平衡仅调控短期体重波动,而脂质周转决定微小、不易察觉的能量盈余能否长期累积囤积;
脂质周转障碍时,脂肪更易滞留储存,难以动员分解,即便没有暴饮暴食,体重也会渐进性升高;
该机制并非否定经典“能量平衡”理论,而是补充了肥胖的深层生物学机制——微小能量失衡如何被机体留存、并随时间持续放大。
02、脂肪细胞更新特点:只增不减,不可逆
借助14C定年技术,研究证实:成年人脂肪细胞终生处于持续更新状态,平均寿命约为10年,脂肪总量依靠细胞新生与死亡的平衡维持。
肥胖人群脂肪细胞生成速率显著升高,导致细胞总数永久性增加
减重仅能缩小脂肪细胞体积,无法减少脂肪细胞数量数,形成“多而小”的持续性增生状态;
细胞数量只增不减,形成长期肥胖结构基础,反复减重损害心血管代谢健康。
03、肥胖调定点与脂肪记忆
肥胖“调定点”:由脂肪细胞数量和脂质周转能力共同塑造。一旦建立,机体就会倾向于脂质滞留囤积,让减重难以维持。热量限制减重后,脂肪细胞体积缩小,同时呈现激素(瘦素降低)与转录层面的“高脂质亲和力”,形成强大的生理性体重反弹驱动力,这也是单纯生活方式干预长期成功率低的核心原因。

图1. 肥胖调定点的结构与分子决定因素
脂肪记忆:既往营养状态会留下持久的转录和表观遗传改变,限制脂肪细胞对减重、药物干预的响应能力。
二者关联:相互作用、彼此强化,结构特征稳固分子记忆,共同锁住肥胖表型。
表1. 肥胖调定点与脂肪记忆的区别及关联

与代谢疾病的关联:前瞻性研究表明,脂质周转障碍先于代谢疾病发生,可提前预测发病风险。甘油三酯周转变慢、脂解能力下降的个体,更易体重增加、出现糖耐量异常或2型糖尿病。这表明脂肪细胞脂质动员障碍不仅是代谢疾病的标志物,而且很可能是长期体重增加和代谢恶化的促成因素。
三、炎症假说更新:脂肪细胞才是“始作俑者”
长期以来,“炎症驱动脂肪功能异常”是主流观点——认为浸润的白细胞是脂肪组织炎症和胰岛素抵抗的主要原因。但临床实践发现,单纯靶向免疫细胞或炎症因子的抗炎治疗,代谢获益十分有限。
最新的“脂肪细胞优先”理论提出了不同的观点:功能异常的脂肪细胞才是炎症的起始信号。脂肪细胞肥大(Hypertrophy)是促炎信号的触发器——当脂肪细胞肥大时,会承受机械应力和缺氧,进而产生趋化因子(如MCP1/CCL2)招募免疫细胞。此时,炎症不是脂肪功能异常的“原因”,而是“结果”。
多项机制研究进一步佐证:应激状态下的脂肪细胞可分泌CCL2调控免疫细胞募集;脂肪细胞谷氨酰胺代谢改变、肌酸依赖的CCL2表达上调,都将细胞能量代谢与组织炎症紧密关联。
临床治疗启示:若炎症主要由脂肪细胞应激驱动,那么单纯抑制免疫系统效果有限。改善脂肪细胞的脂质周转能力、修复代谢功能,才能从根源上缓解慢性炎症。
四、空间转录组学揭秘:脂肪细胞功能各有“分工”
过去,脂肪细胞被视作“千人一面”的高度均一细胞群体,功能差异仅由细胞大小决定。但这无法解释:为何肥胖程度相近的人群,胰岛素敏感性、炎症水平、干预应答会截然不同。
空间转录组学技术的应用,揭开了脂肪细胞异质性的面纱:人类白色脂肪组织中,至少存在三种主要脂肪细胞状态——AdipoPLIN、AdipoLEP、AdipoSAA,三者各有“分工”且可随代谢环境动态转换:
AdipoPLIN:富集脂质周转相关通路,是脂质代谢调控的核心亚型;
AdipoLEP:主要负责感知脂肪组织质量变化;
AdipoSAA:呈现更强的炎症特征,且与脂肪库分布相关。
三种亚型的空间分布差异,直接影响脂肪组织的功能和个体代谢风险——即使BMI相同,胰岛素应答型脂肪细胞的比例不同,代谢健康状况也会天差地别。同时,不同脂肪细胞亚型占主导的个体,对干预的应答也不同。例如,AdipoPLIN富集的个体,更适合预防脂肪组织不良重塑的干预;而AdipoSAA富集的个体,更易从恢复脂肪细胞代谢灵活性的治疗中获益。
五、内脏脂肪的特殊角色:代谢与免疫的“交叉路口”
WAT分布于人体多个解剖部位,不同脂肪库在发育起源、血管化、神经支配和代谢影响上差异显著。传统皮下/内脏脂肪二分法已无法反映内脏脂肪库内部的高度异质性。
近期针对人类WAT的转录组与空间解析研究显示:皮下、大网膜、肠系膜、腹膜外等不同脂肪库,细胞组成与细胞间通讯模式差异显著,直接决定局部免疫微环境及全身代谢结局。
其中,紧邻结肠的腹膜外WAT尤为特殊,其富含表达血清淀粉样蛋白A(SAA)基因的AdipoSAA 细胞群——这类细胞在皮下脂肪中罕见,却在腹膜外脂肪中占比很高,且呈现先天免疫调节的转录特征,而非经典的脂质储存功能。
这一发现挑战了以往主流观点:脂肪组织免疫激活并非主要由浸润白细胞驱动,特定脂肪库中的脂肪细胞本身是局部免疫反应的调控者。
更有趣的是,腹膜外脂肪紧邻肠道,肠道微生物衍生信号(如脂多糖)可直接诱导AdipoSAA表达激活。这表明,AdipoSAA可能作为“哨兵”,连接肠道稳态与全身炎症,将肠道屏障信号转化为脂肪细胞驱动的免疫激活——这也解释了为何肠道健康与代谢疾病密切相关。
六、治疗思路启发与未来展望
综上,WAT早已不是单纯的“惰性储能罐”,而是结构动态、细胞异质、兼具代谢与免疫调控的核心脏器。对它的深入研究,不仅重塑了我们对肥胖、糖尿病的认知,也为代谢疾病个体化精准治疗提供了坚实的机制依据。未来,靶向脂肪细胞本身,或许有望实现代谢疾病的长效防控。
未来重点研究与转化方向:
治疗理念转型:未来的治疗策略不应仅仅关注体重数字下降,而应致力于恢复脂肪细胞的功能(质量),例如正常化脂质周转、重置脂肪细胞状态,从单纯以减重为中心,转向以脂肪组织修复为核心;
个体化精准医疗:通过分析个体的脂肪细胞组成(如AdipoPLIN/AdipoSAA的比例),未来可能预测患者对特定药物(如GLP-1受体激动剂)的反应,从而实现分型施治;
开放科学资源共建:科研团队已搭建脂肪组织知识门户(adiposetissue.org)与哺乳动物脂肪组织知识门户(MATKP;matkp.org)两大开放共享平台,整合多队列、多组学数据,助力推动领域协同研究,加速基础成果向临床转化。 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言