近期,改善全球肾脏病预后组织(KDIGO)发布了《KDIGO 2026年糖尿病合并慢性肾脏病(CKD)临床实践指南(公开评审稿)》(以下简称“指南草案”)[1]。此次更新基于2022版指南,主要涉及第1章、第2章和第4章,内容包括糖尿病合并CKD的定义、预防、筛查、分期及心血管风险评估,血糖监测与目标值,以及药物治疗策略。
这些更新反映了近年来的最新进展以及循证证据。在治疗理念上,指南草案首次系统性强调预防为先,而不仅仅是对已确诊CKD的管理;在血糖监测方面,广泛推荐持续葡萄糖监测(CGM)并首次为使用者设定具体目标值;药物治疗是本次更新的重点,提出了全新的管理框架,其中对具有明确心肾保护证据的胰高糖素样肽-1受体激动剂(GLP-1RA,如司美格鲁肽)的推荐等级提升至最高的1A级。这些重要变化与临床实践密切相关,本文重点介绍指南草案中关于糖尿病合并CKD药物治疗的内容更新,以期为临床实践提供参考。

一、 指南草案更新速览:全面优化药物管理,GLP-1RA升级为1A级强力推荐
指南草案推荐采用生活方式干预与药物治疗相结合的策略来治疗糖尿病合并CKD患者,以降低肾病进展风险和心血管疾病风险。更新的管理框架体现了“个体化、加速、不断优化”的综合管理原则:以患者为中心,在生活方式和基础药物[肾素-血管紧张素系统抑制剂(RASi)、钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)、他汀类药物]之上,快速启动并优化联合治疗方案[GLP-1RA、非甾体类盐皮质激素受体拮抗剂(nsMRA)](图1)[1]。
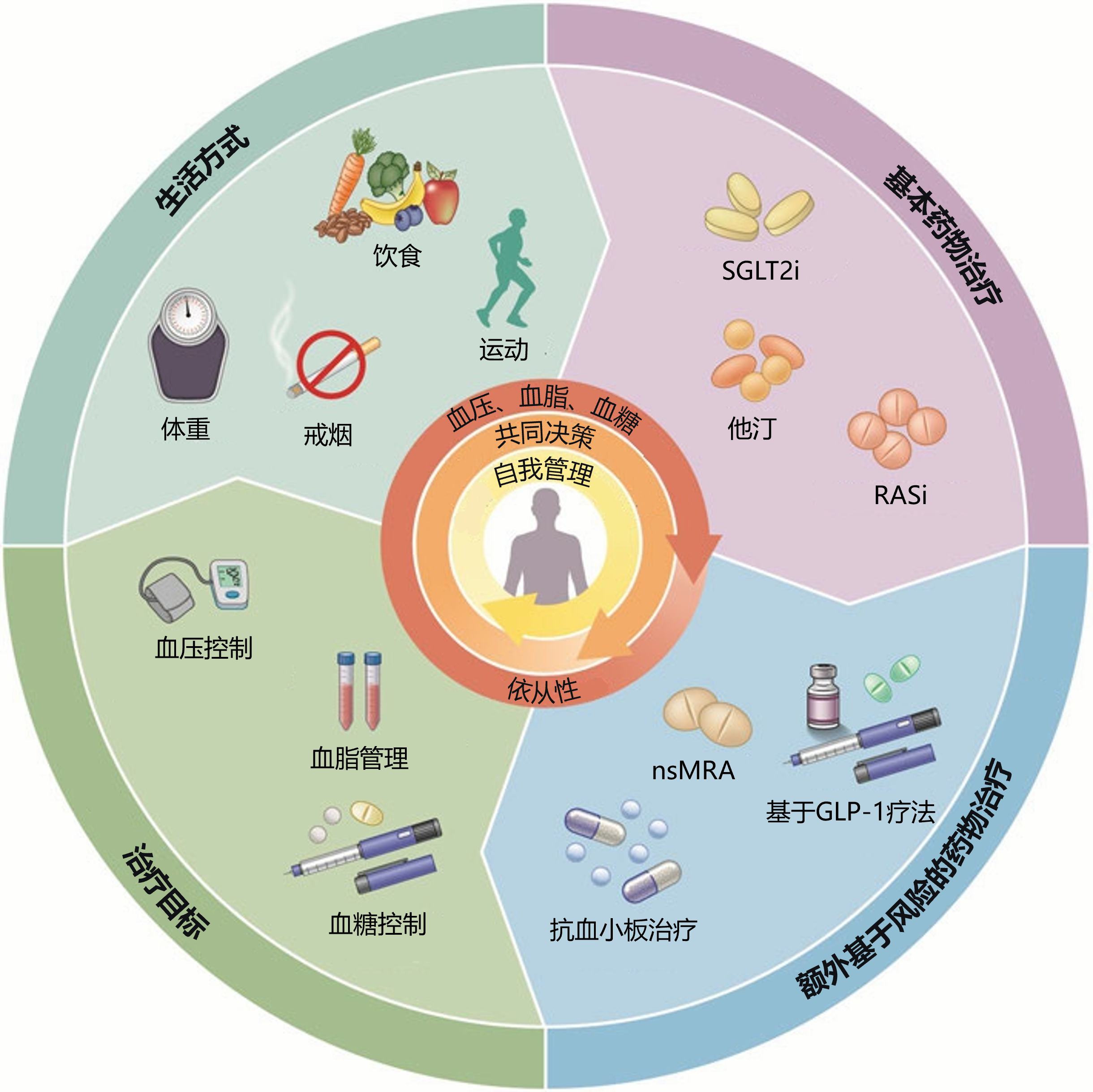
图1. 改善糖尿病合并CKD患者预后的综合管理策略
1、RASi:维持1B级推荐
推荐4.2.1:对于合并高血压且存在白蛋白尿的糖尿病合并CKD患者,应启动血管紧张素转换酶抑制剂(ACEI)或血管紧张素Ⅱ受体拮抗剂(ARB)治疗,并滴定至最大耐受剂量(1B)。
在开始使用或增加RASi剂量后的2~4周内,应监测血压、估算肾小球滤过率(eGFR)及血清钾水平的变化。ACEI与ARB不应联合使用[1]。
2、SGLT2i:维持1A级推荐
推荐4.3.1:对于eGFR≥20 ml/min/1.73m2的2型糖尿病(T2DM)合并CKD患者,建议使用SGLT2i(1A)。
一旦开始使用SGLT2i,即使eGFR降至20 ml/min/1.73m2以下,也应建议继续使用,除非出现不耐受或需要启动肾脏替代治疗。在长期禁食、重大手术或危重症期间,若酮症或低血容量风险增加,应合理暂停SGLT2i使用[1]。
3、GLP-1RA:升级为1A级推荐
推荐4.5.1:对于心肾高风险或血糖控制不达标的T2DM合并CKD患者,建议使用具有明确心血管或肾脏获益的GLP-1RA(1A)。
适用人群:指南草案明确推荐GLP-1RA用于已确诊动脉粥样硬化性心血管疾病(ASCVD)或尿白蛋白肌酐比值(UACR)≥100 mg/g的患者,以及需要强化血糖控制(HbA1c或CGM不达标)或合并肥胖需要减重的患者[1]。
同时,指南草案强调低剂量起始、逐步滴定以减轻胃肠道不良反应的策略。对于接受透析治疗的肾衰竭患者,亦可启动或继续GLP-1RA治疗。值得注意的是,不是所有GLP-1RA都有心肾获益,指南草案建议优先考虑具有明确心血管及肾脏保护作用的GLP-1类药物,如司美格鲁肽0.5 mg/1 mg注射液[1]。
支持将GLP-1RA升级为1A级推荐的循证证据来自11项心血管结局研究(CVOT)和1项肾脏结局研究(KOT)。这些研究评估了GLP-1RA在T2DM合并CKD患者中的心血管和肾脏获益,其中最强有力的肾脏获益证据来自FLOW研究。指南草案特别指出,与其他CVOT仅纳入较小样本的CKD人群不同,FLOW研究专门针对合并CKD的T2DM患者,是GLP-1RA类药物中首个且目前唯一*的KOT。其结果证实,司美格鲁肽1.0 mg可为T2DM合并CKD患者带来改善肾脏和心血管结局以及提高生存率的全面获益[1,2]。也正是基于该研究的纳入人群标准,指南草案将UACR≥100 mg/g作为使用GLP-1RA的重要指征之一[1,2]。
*截至2026年5月
4、nsMRA:升级为1A级推荐
推荐4.4.1:对于eGFR≥25 ml/min/1.73m2、血钾浓度正常且存在白蛋白尿(UACR≥30 mg/g)的T2DM合并CKD患者,在已使用最大耐受剂量RASi的基础上,建议加用有心肾获益证据的nsMRA(1A)。
对于已使用RASi但仍有白蛋白尿且血钾正常的患者,SGLT2i与nsMRA可同时启动。应用nsMRA后应定期监测血清钾水平[1]。
5、二甲双胍:1B级推荐
推荐4.6.1:对于eGFR≥30 ml/min/1.73m2、在应用SGLT2i和GLP-1RA治疗后血糖仍未达标或无法使用上述药物的T2DM合并CKD患者,建议使用二甲双胍(1B)。
该推荐明确将二甲双胍的地位置于SGLT2i和GLP-1RA之后。当eGFR处于30~44 ml/min/1.73m2时,建议二甲双胍剂量减半;当eGFR<60 ml/min/1.73m2时,应加强eGFR监测[1]。
综上,指南草案关于药物治疗提出了新的综合管理流程,并对各类药物的推荐等级、适用人群、使用规范等进行了系统梳理和更新。其中,GLP-1RA提升至1A级最高推荐等级是本次更新的重要亮点之一,司美格鲁肽因拥有FLOW研究的重磅循证支持而受到关注。
二、 GLP-1RA的肾脏获益:从循证到机制,司美格鲁肽拥有完整证据链
在GLP-1RA类药物中,司美格鲁肽的肾脏保护作用尤为突出,是中国首个且目前唯一*获批CKD适应症的肠促胰素类药物。从循证证据积累、机制探索到适应症获批,司美格鲁肽在多项关键研究中提供了较为完整的证据链。
目前唯一*一个针对肠促胰素类药物的KOT——FLOW研究
GLP-1RA的肾脏获益最初在CVOT的次要终点或探索性分析中被发现,相关荟萃分析提供了进一步支持,确证肾脏获益则来自专门设计的KOT——FLOW研究。该研究取得里程碑式突破,结果证实,T2DM合并CKD患者在标准治疗基础上,应用司美格鲁肽1.0 mg可显著降低肾脏复合事件风险达24%,显著降低UACR达40%,并明显延缓肾功能下降;同时,显著降低主要心血管不良事件(MACE)风险18%,并降低全因死亡风险20%[2]。事后分析进一步证实,司美格鲁肽1.0 mg在不同基线特征与疾病状态的广泛T2DM合并CKD人群中具有高度一致的肾脏获益[3]。
开展首个探索GLP-1RA肾脏获益机制的Ⅲ期临床研究——REMODEL研究
目前认为,GLP-1RA通过直接和间接等多种途径实现肾脏获益。REMODEL研究是首项针对GLP-1RA肾脏作用机制开展的随机、对照Ⅲ期临床研究,结果显示,司美格鲁肽1.0 mg可通过减少肾内及肾周脂肪、改善肾小球血流动力学、控制肾脏纤维化进程、下调肾小球内皮细胞代谢应激及纤维化/炎症相关基因表达等作用,产生特异性肾脏保护获益[4]。指南草案引用了REMODEL研究,作为解释GLP-1RA肾脏获益机制的重要依据[1]。该研究的事后分析进一步揭示,司美格鲁肽的肾脏保护机制独立于SGLT2i,两者作用可能互补,为未来优化联合治疗提供了理论支持[5]。
目前唯一*一个获批CKD适应症的肠促胰素类药物
2025年,司美格鲁肽先后获得美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)批准,新增CKD适应症,用于降低T2DM合并CKD患者的eGFR持续下降、终末期肾病和心血管死亡的风险。由此,司美格鲁肽成为首个且目前唯一*具有CKD适应症的肠促胰素类药物。
*截至2026年5月
本部分涉及司美格鲁肽剂量为0.5 mg/1.0 mg
三、 结语
2026 KDIGO指南草案对糖尿病合并CKD的药物治疗进行了重大更新,GLP-1RA司美格鲁肽地位提升,获得1A级强力推荐,这是来自肾病权威指南的高度肯定。此外,在国内外糖尿病权威指南,包括2024 CDS《中国糖尿病防治指南》和2026 ADA《糖尿病医学诊疗标准》中,具有明确肾脏获益的GLP-1RA亦获得一致推荐,作为T2DM合并CKD的一线治疗药物[6,7]。随着GLP-1RA循证地位日益巩固,糖尿病肾病的治疗策略正经历重大变革,心肾保护治疗四大支柱(RASi、SGLT2i、nsMRA、GLP-1RA)的新格局正在形成。其中,司美格鲁肽凭借FLOW研究的重磅循证、REMODEL研究的机制支持以及CKD适应症的独特优势,在GLP-1RA肾脏获益领域构建了较为完整的证据链,为广泛T2DM合并CKD患者进一步改善心肾结局提供了新的治疗选择。
参考文献
1. KDIGO 2026 Clinical Practice Guideline for Diabetes and Chronic Kidney Disease (CKD). Chapter 1, Chapter 2, & Chapter 4 update. Public Review Draft, March 2026.
2. Perkovic V, et al. N Engl J Med. 2024; 391(2): 109-121.
3. Bellary S, et al. Effect of once-weekly semaglutide 1.0 mg on kidney outcomes by baseline characteristics: Exploratory data from the FLOW trial. Poster presented at: World Congress of Nephrology (WCN) 2026; March 28–31, 2026; Yokohama, Japan. Abstract WCN26-AB 4078, Poster P324.
4. Cherney DZI, et al. Nephrol Dial Transplant. 2025; 40(11): 2182-2192.
5. Cherney DZI, et al. Mechanistic kidney effects of semaglutide by baseline SGLT2i use in type 2 diabetes: a post-hoc analysis of the REMODEL trial. Oral presentation. World Congress of Nephrology 2026; Yokohama, Japan. March 28, 2026.
6. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
7. American Diabetes Association. Diabetes Care. 2026; 49(Suppl. 1): S1-S371. 2 comments
这些更新反映了近年来的最新进展以及循证证据。在治疗理念上,指南草案首次系统性强调预防为先,而不仅仅是对已确诊CKD的管理;在血糖监测方面,广泛推荐持续葡萄糖监测(CGM)并首次为使用者设定具体目标值;药物治疗是本次更新的重点,提出了全新的管理框架,其中对具有明确心肾保护证据的胰高糖素样肽-1受体激动剂(GLP-1RA,如司美格鲁肽)的推荐等级提升至最高的1A级。这些重要变化与临床实践密切相关,本文重点介绍指南草案中关于糖尿病合并CKD药物治疗的内容更新,以期为临床实践提供参考。

一、 指南草案更新速览:全面优化药物管理,GLP-1RA升级为1A级强力推荐
指南草案推荐采用生活方式干预与药物治疗相结合的策略来治疗糖尿病合并CKD患者,以降低肾病进展风险和心血管疾病风险。更新的管理框架体现了“个体化、加速、不断优化”的综合管理原则:以患者为中心,在生活方式和基础药物[肾素-血管紧张素系统抑制剂(RASi)、钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)、他汀类药物]之上,快速启动并优化联合治疗方案[GLP-1RA、非甾体类盐皮质激素受体拮抗剂(nsMRA)](图1)[1]。

图1. 改善糖尿病合并CKD患者预后的综合管理策略
1、RASi:维持1B级推荐
推荐4.2.1:对于合并高血压且存在白蛋白尿的糖尿病合并CKD患者,应启动血管紧张素转换酶抑制剂(ACEI)或血管紧张素Ⅱ受体拮抗剂(ARB)治疗,并滴定至最大耐受剂量(1B)。
在开始使用或增加RASi剂量后的2~4周内,应监测血压、估算肾小球滤过率(eGFR)及血清钾水平的变化。ACEI与ARB不应联合使用[1]。
2、SGLT2i:维持1A级推荐
推荐4.3.1:对于eGFR≥20 ml/min/1.73m2的2型糖尿病(T2DM)合并CKD患者,建议使用SGLT2i(1A)。
一旦开始使用SGLT2i,即使eGFR降至20 ml/min/1.73m2以下,也应建议继续使用,除非出现不耐受或需要启动肾脏替代治疗。在长期禁食、重大手术或危重症期间,若酮症或低血容量风险增加,应合理暂停SGLT2i使用[1]。
3、GLP-1RA:升级为1A级推荐
推荐4.5.1:对于心肾高风险或血糖控制不达标的T2DM合并CKD患者,建议使用具有明确心血管或肾脏获益的GLP-1RA(1A)。
适用人群:指南草案明确推荐GLP-1RA用于已确诊动脉粥样硬化性心血管疾病(ASCVD)或尿白蛋白肌酐比值(UACR)≥100 mg/g的患者,以及需要强化血糖控制(HbA1c或CGM不达标)或合并肥胖需要减重的患者[1]。
同时,指南草案强调低剂量起始、逐步滴定以减轻胃肠道不良反应的策略。对于接受透析治疗的肾衰竭患者,亦可启动或继续GLP-1RA治疗。值得注意的是,不是所有GLP-1RA都有心肾获益,指南草案建议优先考虑具有明确心血管及肾脏保护作用的GLP-1类药物,如司美格鲁肽0.5 mg/1 mg注射液[1]。
支持将GLP-1RA升级为1A级推荐的循证证据来自11项心血管结局研究(CVOT)和1项肾脏结局研究(KOT)。这些研究评估了GLP-1RA在T2DM合并CKD患者中的心血管和肾脏获益,其中最强有力的肾脏获益证据来自FLOW研究。指南草案特别指出,与其他CVOT仅纳入较小样本的CKD人群不同,FLOW研究专门针对合并CKD的T2DM患者,是GLP-1RA类药物中首个且目前唯一*的KOT。其结果证实,司美格鲁肽1.0 mg可为T2DM合并CKD患者带来改善肾脏和心血管结局以及提高生存率的全面获益[1,2]。也正是基于该研究的纳入人群标准,指南草案将UACR≥100 mg/g作为使用GLP-1RA的重要指征之一[1,2]。
*截至2026年5月
4、nsMRA:升级为1A级推荐
推荐4.4.1:对于eGFR≥25 ml/min/1.73m2、血钾浓度正常且存在白蛋白尿(UACR≥30 mg/g)的T2DM合并CKD患者,在已使用最大耐受剂量RASi的基础上,建议加用有心肾获益证据的nsMRA(1A)。
对于已使用RASi但仍有白蛋白尿且血钾正常的患者,SGLT2i与nsMRA可同时启动。应用nsMRA后应定期监测血清钾水平[1]。
5、二甲双胍:1B级推荐
推荐4.6.1:对于eGFR≥30 ml/min/1.73m2、在应用SGLT2i和GLP-1RA治疗后血糖仍未达标或无法使用上述药物的T2DM合并CKD患者,建议使用二甲双胍(1B)。
该推荐明确将二甲双胍的地位置于SGLT2i和GLP-1RA之后。当eGFR处于30~44 ml/min/1.73m2时,建议二甲双胍剂量减半;当eGFR<60 ml/min/1.73m2时,应加强eGFR监测[1]。
综上,指南草案关于药物治疗提出了新的综合管理流程,并对各类药物的推荐等级、适用人群、使用规范等进行了系统梳理和更新。其中,GLP-1RA提升至1A级最高推荐等级是本次更新的重要亮点之一,司美格鲁肽因拥有FLOW研究的重磅循证支持而受到关注。
二、 GLP-1RA的肾脏获益:从循证到机制,司美格鲁肽拥有完整证据链
在GLP-1RA类药物中,司美格鲁肽的肾脏保护作用尤为突出,是中国首个且目前唯一*获批CKD适应症的肠促胰素类药物。从循证证据积累、机制探索到适应症获批,司美格鲁肽在多项关键研究中提供了较为完整的证据链。
目前唯一*一个针对肠促胰素类药物的KOT——FLOW研究
GLP-1RA的肾脏获益最初在CVOT的次要终点或探索性分析中被发现,相关荟萃分析提供了进一步支持,确证肾脏获益则来自专门设计的KOT——FLOW研究。该研究取得里程碑式突破,结果证实,T2DM合并CKD患者在标准治疗基础上,应用司美格鲁肽1.0 mg可显著降低肾脏复合事件风险达24%,显著降低UACR达40%,并明显延缓肾功能下降;同时,显著降低主要心血管不良事件(MACE)风险18%,并降低全因死亡风险20%[2]。事后分析进一步证实,司美格鲁肽1.0 mg在不同基线特征与疾病状态的广泛T2DM合并CKD人群中具有高度一致的肾脏获益[3]。
开展首个探索GLP-1RA肾脏获益机制的Ⅲ期临床研究——REMODEL研究
目前认为,GLP-1RA通过直接和间接等多种途径实现肾脏获益。REMODEL研究是首项针对GLP-1RA肾脏作用机制开展的随机、对照Ⅲ期临床研究,结果显示,司美格鲁肽1.0 mg可通过减少肾内及肾周脂肪、改善肾小球血流动力学、控制肾脏纤维化进程、下调肾小球内皮细胞代谢应激及纤维化/炎症相关基因表达等作用,产生特异性肾脏保护获益[4]。指南草案引用了REMODEL研究,作为解释GLP-1RA肾脏获益机制的重要依据[1]。该研究的事后分析进一步揭示,司美格鲁肽的肾脏保护机制独立于SGLT2i,两者作用可能互补,为未来优化联合治疗提供了理论支持[5]。
目前唯一*一个获批CKD适应症的肠促胰素类药物
2025年,司美格鲁肽先后获得美国食品药品监督管理局(FDA)和中国国家药品监督管理局(NMPA)批准,新增CKD适应症,用于降低T2DM合并CKD患者的eGFR持续下降、终末期肾病和心血管死亡的风险。由此,司美格鲁肽成为首个且目前唯一*具有CKD适应症的肠促胰素类药物。
*截至2026年5月
本部分涉及司美格鲁肽剂量为0.5 mg/1.0 mg
三、 结语
2026 KDIGO指南草案对糖尿病合并CKD的药物治疗进行了重大更新,GLP-1RA司美格鲁肽地位提升,获得1A级强力推荐,这是来自肾病权威指南的高度肯定。此外,在国内外糖尿病权威指南,包括2024 CDS《中国糖尿病防治指南》和2026 ADA《糖尿病医学诊疗标准》中,具有明确肾脏获益的GLP-1RA亦获得一致推荐,作为T2DM合并CKD的一线治疗药物[6,7]。随着GLP-1RA循证地位日益巩固,糖尿病肾病的治疗策略正经历重大变革,心肾保护治疗四大支柱(RASi、SGLT2i、nsMRA、GLP-1RA)的新格局正在形成。其中,司美格鲁肽凭借FLOW研究的重磅循证、REMODEL研究的机制支持以及CKD适应症的独特优势,在GLP-1RA肾脏获益领域构建了较为完整的证据链,为广泛T2DM合并CKD患者进一步改善心肾结局提供了新的治疗选择。
参考文献
1. KDIGO 2026 Clinical Practice Guideline for Diabetes and Chronic Kidney Disease (CKD). Chapter 1, Chapter 2, & Chapter 4 update. Public Review Draft, March 2026.
2. Perkovic V, et al. N Engl J Med. 2024; 391(2): 109-121.
3. Bellary S, et al. Effect of once-weekly semaglutide 1.0 mg on kidney outcomes by baseline characteristics: Exploratory data from the FLOW trial. Poster presented at: World Congress of Nephrology (WCN) 2026; March 28–31, 2026; Yokohama, Japan. Abstract WCN26-AB 4078, Poster P324.
4. Cherney DZI, et al. Nephrol Dial Transplant. 2025; 40(11): 2182-2192.
5. Cherney DZI, et al. Mechanistic kidney effects of semaglutide by baseline SGLT2i use in type 2 diabetes: a post-hoc analysis of the REMODEL trial. Oral presentation. World Congress of Nephrology 2026; Yokohama, Japan. March 28, 2026.
6. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
7. American Diabetes Association. Diabetes Care. 2026; 49(Suppl. 1): S1-S371. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言