编者按:
胰岛素是控制2型糖尿病(T2DM)患者高血糖的重要手段,主要针对胰岛β细胞分泌胰岛素不足的病理生理缺陷来发挥作用。与传统治疗方案如基础胰岛素、预混胰岛素相比,德谷门冬双胰岛素可更好兼顾空腹与餐后血糖控制,减少血糖波动。然而,对于部分病程较长、合并症多、胰岛素抵抗严重的T2DM患者,仅胰岛素治疗难以全面覆盖T2DM核心发病机制,且存在低血糖风险、体重增加、方案复杂等挑战。优化降糖方案需要兼顾胰岛素缺乏和胰岛素抵抗两大病理机制,并在强化降糖同时简化治疗。
作为首个基础胰岛素/GLP-1RA固定比例复方制剂(FRC),德谷胰岛素利拉鲁肽凭借机制互补、增效减副以及简化治疗等多重优势,为德谷门冬双胰岛素转换治疗提供优化方案。本文中,北京中医药大学东方医院秦皇岛医院内分泌科郑新颖教授分享临床病例和诊治体会,山东大学齐鲁第二医院陈诗鸿教授进行精彩点评。
01、病例基本信息
患者女性,54岁,因“渴饮乏力反复发作12年”于2024年8月1日就诊。
现病史:
患者12年前无诱因出现渴饮乏力,就诊于我院经查确诊“T2DM”,先期应用二甲双胍、格列美脲等多种降糖药物。
2017年因血糖控制不佳,治疗方案调整为睡前皮下注射18U甘精胰岛素,并联合口服二甲双胍。
2020年5月因血糖失控入院,其间发现难治性高血压、低血钾考虑原发性醛固酮增多症(原醛症),但患者拒绝进一步筛查,故仅对症给予补钾降压治疗,调整降糖方案为门冬胰岛素30早晚各18U皮下注射联合阿卡波糖口服。
2022年7月门诊随诊发现空腹血糖(FPG)始终不达标,睡前加服二甲双胍缓释片无改善,遂调整门冬胰岛素30为德谷门冬双胰岛素早18U、晚16U餐前皮下注射,联合二甲双胍缓释片+阿卡波糖口服。
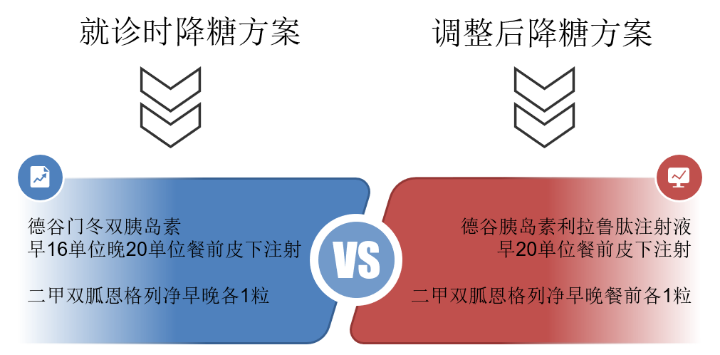
2024年3月肺CT检查发现偶然右侧肾上腺腺瘤,行手术治疗后血压、血钾恢复正常,围术期血糖波动在8~12 mmol/L。术后随诊因血糖不达标且尿蛋白阳性将二甲双胍调整为二甲双胍恩格列净早晚各1粒。此次就诊因术后康复过程中监测FPG波动于8~12 mmol/L,餐后血糖波动于9~15 mmol/L,寻求进一步改善血糖控制。就诊时降糖方案为德谷门冬双胰岛素早16U、晚20U餐前皮下注射,联合二甲双胍恩格列净早晚各1粒。
既往史:
高血压病史20余年,高血压难以控制、低钾血症病史4年,2024年3月行肾上腺腺瘤切除术后高血压、低血糖纠正。
家族史:
母亲、胞姐患糖尿病,均在40岁后发病。
体格检查:
血压135/88 mmHg,心率82 bpm。身高158 cm,体重63 kg,BMI 25.23 kg/m2。神清语利,甲状腺、心肺腹未见阳性体征,双下肢胫前轻度指凹性水肿,双下肢皮温正常,双足背动脉可触。
实验室检查:
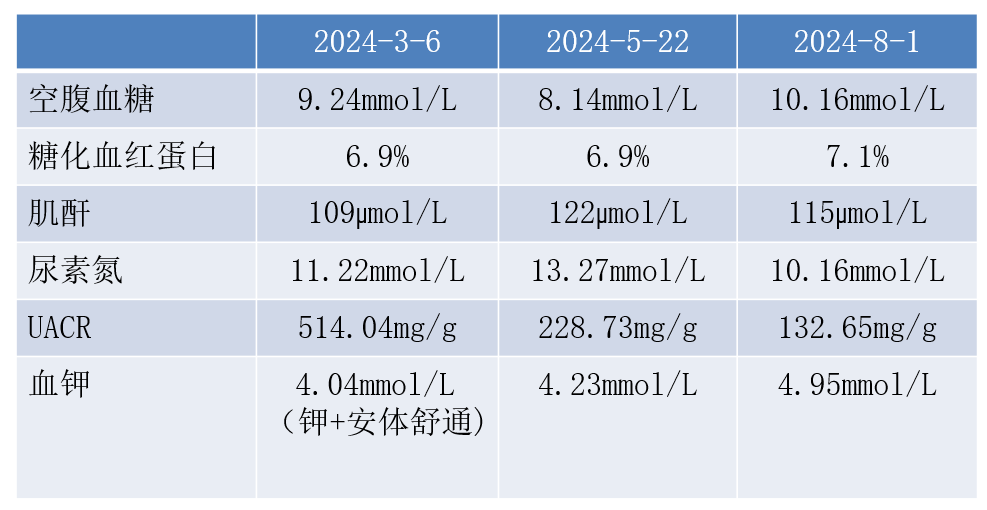
自2024年3月右侧肾上腺腺瘤术后的随诊结果如表1所示,可见FPG一直居高不下,糖化血红蛋白(HbA1c)无明显改善,尿蛋白明显下降。至本次就诊时FPG 10.16 mmol/L,HbA1c 7.1%;肌酐115 μmol/L,尿素氮10.16 mmol/L;尿白蛋白肌酐比值(UACR) 132.65 mg/g;血钾4.95 mmol/L。
表1. 实验室检查
1.T2DM
2.糖尿病肾病
3.超重
02、病例分析及治疗经过
该病例特点总结如下:
中年女性,糖尿病病史较长,已出现糖尿病肾病的并发症
血糖进行性恶化,长期接受胰岛素治疗,尝试过基础胰岛素+口服药(OAD)、预混胰岛素+OAD、双胰岛素+OAD,患者血糖始终未得到理想控制,尤其表现为空腹血糖不达标
曾合并右侧肾上腺腺瘤(原醛症),行手术治疗后高血压、低钾血症得以纠正,但其对糖代谢异常的影响可能持续存在
根据病例特点调整治疗方案:该患者胰岛功能较差,胰岛素分泌相对不足,但经长期胰岛素治疗仍未能将血糖控制在良好范围,且胰岛素剂量已经用到较高水平(每日36U)。结合其原醛症病史,胰岛素抵抗的情况不容忽视。为更加全面覆盖T2DM核心发病机制,以进一步改善血糖控制,遂将德谷门冬双胰岛素每日两次注射转换为德谷胰岛素利拉鲁肽20U早餐前皮下注射,保留OAD联合方案不变(二甲双胍恩格列净早晚各1粒)。
半年后(2025年2月)复查,FPG 5.27 mmol/l,UACR 110.66 mg/g。血糖维持良好控制,蛋白尿进一步减少。
03、专家点评

陈诗鸿教授
胰岛β细胞功能障碍和胰岛素抵抗是T2DM的两大核心病理生理机制。两者相互影响,涉及多个重要器官与组织,共同导致糖代谢紊乱。基础胰岛素和GLP-1RA机制互补,全面覆盖T2DM核心缺陷。德谷胰岛素利拉鲁肽作为基础胰岛素/GLP-1RA的首个FRC制剂,通过德谷胰岛素、利拉鲁肽双组分发挥协同作用,机制互补,覆盖T2DM多重病理生理机制(图1),在增强降糖疗效的同时减少不良反应[1],而且使用简便,每日一次注射,在预混胰岛素或双胰岛素转换治疗中具有多重优势。
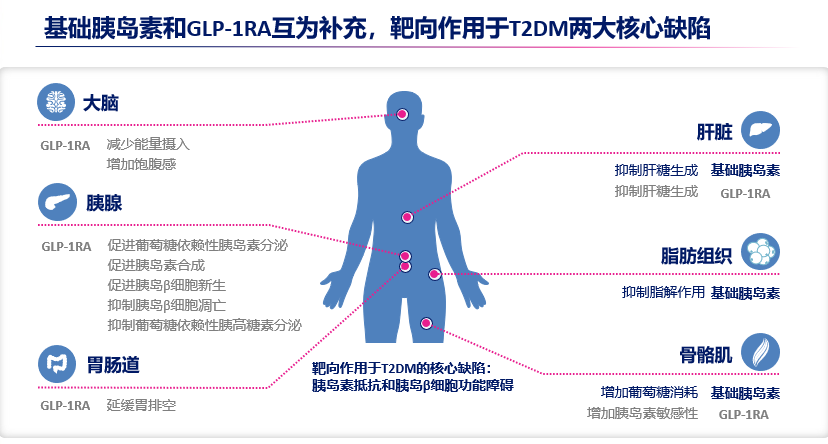
图1. 德谷胰岛素利拉鲁肽作用机制:两组分机制互补
强化降糖
DUAL系列研究证实,德谷胰岛素利拉鲁肽能够显著降低HbA1c(降幅达2.0%),全面改善空腹血糖和餐后血糖,HbA1c<7%达标率高达89.9% [2-12]。对于预混胰岛素转换人群,DUAL II Japan研究显示,预混胰岛素血糖控制不佳T2DM患者转换为德谷胰岛素利拉鲁肽治疗可进一步改善血糖控制(HbA1c降低1.58%),体重减轻(-1.5kg)且低血糖风险低[13]。
具体到该病例,历经基础胰岛素、预混胰岛素和双胰岛素治疗,但空腹血糖始终控制不佳,最终从双胰岛素转换为FRC,治疗后2周即实现了空腹和餐后血糖双达标,且大大节约胰岛素剂量,患者应用双胰岛素每日剂量达36U,德谷胰岛素利拉鲁肽转换剂量为20U,后续减至16U,即可维持血糖达标。
该病例一方面印证了FRC在研究中展现的强效降糖效果,另一方面也引发临床思考:对于胰岛素大剂量、长期治疗效果不佳的患者,一味增加剂量或并不利于降糖,反而可能加重胰岛素抵抗。由于该患者合并肾上腺腺瘤(原醛症),醛固酮水平增加可导致更严重的胰岛素抵抗,仅通过外源性补充胰岛素难以纠正胰岛素抵抗的问题,加用GLP-1RA可很好地弥补这一缺陷。德谷胰岛素与利拉鲁肽机制互补,协同增效,仅需较小的胰岛素剂量即可实现良好血糖控制,同时还能减少大剂量胰岛素带来的低血糖和体重增加风险。
简化治疗
FRC有助于简化治疗:①减少注射次数:德谷胰岛素利拉鲁肽每日1次任意时间注射,无需严格配合进餐,减少治疗负担。该患者从双胰岛素每日2次注射转换为FRC每日1次注射,进一步简化治疗,减少注射负担。②减少OAD种类:真实世界研究显示,启用德谷胰岛素利拉鲁肽后,大多数(82.8%)T2DM患者仅需联合1种OAD[14],即“一针一片”方案。该病例转换为FRC治疗后,保留原先的一种OAD不变,从“两针一片”简化为“一针一片”,更利于提高依从性。
综上,德谷胰岛素利拉鲁肽作为基础胰岛素/GLP-1RA联合制剂,凭借协同机制,可全面覆盖胰岛素缺乏和胰岛素抵抗两大核心机制,强效降糖同时简化治疗,帮助T2DM患者实现“强化且简化”双重获益。本病例中,患者由双胰岛素转换为德谷胰岛素利拉鲁肽治疗后,长期困扰的血糖控制欠佳问题得以迅速、显著改善,同时方案简化、治疗体验更好,患者信心大增。临床上,对于预混胰岛素或双胰岛素治疗血糖控制不佳的T2DM患者,不妨跳出传统胰岛素治疗思路,转换使用德谷胰岛素利拉鲁肽,或可取得化繁为简、事半功倍的效果。
点评专家简介

陈诗鸿 教授
山东大学齐鲁第二医院内分泌代谢科主任
疑难罕见病中心主任
二级教授,博士研究生导师,博士后合作导师
中华医学会内分泌学分会委员
中国医师协会内分泌代谢科医师分会委员
中国女医师协会医体专业委员会副主任委员
中国女医师协会糖尿病与内分泌专业委员会委员
山东省医学会骨质疏松与骨矿盐疾病分会主任委员
山东省老年医学学会内分泌专业委员会主任委员
山东省研究型医院学会内分泌学分会主任委员
山东省医学会内分泌学分会副主任委员
山东省医师协会内分泌科医师分会副主任委员
病例作者简介

郑新颖 教授
北京中医药大学东方医院秦皇岛医院
主任中医师、硕士研究生导师
北京中医药大学东方医院秦皇岛医院内分泌一科副主任
中国民族医药学会甲状腺病分会理事
河北省中医药学会骨质疏松专业委员会副主委
河北省中西医结合学会络病专业委员会常委
河北省名医学会慢病管理专业委员会常委
河北省药学会内分泌代谢药物专业委员会常委
河北省中西医结合学会糖尿病足专业委员会委员
参考文献
1.德谷胰岛素利拉鲁肽注射液临床应用专家指导建议. 中华糖尿病杂志. 2023; 15(3): 209-215.
2.Gough SC, et al. Diabetes Obes Metab. 2015; 17(10): 965-973. DUAL I ext
3.Buse JB, et al. Diabetes Care. 2014; 37(11): 2926-2933. DUAL II
4.Linjawi S, et al. Diabetes Ther. 2017; 8(1): 101-114. DUAL III
5.Rodbard HW, et al. Diabet Med. 2017; 34(2): 189-196. DUAL IV
6.Lingvay I, et al. JAMA. 2016; 315(9): 898-907. DUAL V
7.Harris SB, et al. Diabetes ObesMetab. 2017; 19(6): 858-865. DUAL VI
8.Billings LK, et al. Diabetes Care. 2018; 41(5): 1009-1016. DUAL VII
9.Aroda VR, et al. Lancet Diabetes Endocrinol. 2019; 7(8): 596-605. DUAL VIII
10.Philis-Tsimikas A, et al. Diabetes Obes Metab. 2019; 21(6): 1399-1408. DUAL IX
11.Wang W, et al. J Diabetes. 2022; 14(6): 401413. DUAL I China
12.Pei Y, et al. Diabetes Obes Metab. 2021; 23(12): 26872696. DUAL II China.
13.Watada H, et al. Diabetes Ther. 2020 Jan;11(1):331-339. DUAL II Japan.
14.Romano I, Serra R. Diabetes Ther. 2024; 15(1): 145-154. 2 comments
胰岛素是控制2型糖尿病(T2DM)患者高血糖的重要手段,主要针对胰岛β细胞分泌胰岛素不足的病理生理缺陷来发挥作用。与传统治疗方案如基础胰岛素、预混胰岛素相比,德谷门冬双胰岛素可更好兼顾空腹与餐后血糖控制,减少血糖波动。然而,对于部分病程较长、合并症多、胰岛素抵抗严重的T2DM患者,仅胰岛素治疗难以全面覆盖T2DM核心发病机制,且存在低血糖风险、体重增加、方案复杂等挑战。优化降糖方案需要兼顾胰岛素缺乏和胰岛素抵抗两大病理机制,并在强化降糖同时简化治疗。
作为首个基础胰岛素/GLP-1RA固定比例复方制剂(FRC),德谷胰岛素利拉鲁肽凭借机制互补、增效减副以及简化治疗等多重优势,为德谷门冬双胰岛素转换治疗提供优化方案。本文中,北京中医药大学东方医院秦皇岛医院内分泌科郑新颖教授分享临床病例和诊治体会,山东大学齐鲁第二医院陈诗鸿教授进行精彩点评。
01、病例基本信息
患者女性,54岁,因“渴饮乏力反复发作12年”于2024年8月1日就诊。
现病史:
患者12年前无诱因出现渴饮乏力,就诊于我院经查确诊“T2DM”,先期应用二甲双胍、格列美脲等多种降糖药物。
2017年因血糖控制不佳,治疗方案调整为睡前皮下注射18U甘精胰岛素,并联合口服二甲双胍。
2020年5月因血糖失控入院,其间发现难治性高血压、低血钾考虑原发性醛固酮增多症(原醛症),但患者拒绝进一步筛查,故仅对症给予补钾降压治疗,调整降糖方案为门冬胰岛素30早晚各18U皮下注射联合阿卡波糖口服。
2022年7月门诊随诊发现空腹血糖(FPG)始终不达标,睡前加服二甲双胍缓释片无改善,遂调整门冬胰岛素30为德谷门冬双胰岛素早18U、晚16U餐前皮下注射,联合二甲双胍缓释片+阿卡波糖口服。
2024年3月肺CT检查发现偶然右侧肾上腺腺瘤,行手术治疗后血压、血钾恢复正常,围术期血糖波动在8~12 mmol/L。术后随诊因血糖不达标且尿蛋白阳性将二甲双胍调整为二甲双胍恩格列净早晚各1粒。此次就诊因术后康复过程中监测FPG波动于8~12 mmol/L,餐后血糖波动于9~15 mmol/L,寻求进一步改善血糖控制。就诊时降糖方案为德谷门冬双胰岛素早16U、晚20U餐前皮下注射,联合二甲双胍恩格列净早晚各1粒。
既往史:
高血压病史20余年,高血压难以控制、低钾血症病史4年,2024年3月行肾上腺腺瘤切除术后高血压、低血糖纠正。
家族史:
母亲、胞姐患糖尿病,均在40岁后发病。
体格检查:
血压135/88 mmHg,心率82 bpm。身高158 cm,体重63 kg,BMI 25.23 kg/m2。神清语利,甲状腺、心肺腹未见阳性体征,双下肢胫前轻度指凹性水肿,双下肢皮温正常,双足背动脉可触。
实验室检查:
自2024年3月右侧肾上腺腺瘤术后的随诊结果如表1所示,可见FPG一直居高不下,糖化血红蛋白(HbA1c)无明显改善,尿蛋白明显下降。至本次就诊时FPG 10.16 mmol/L,HbA1c 7.1%;肌酐115 μmol/L,尿素氮10.16 mmol/L;尿白蛋白肌酐比值(UACR) 132.65 mg/g;血钾4.95 mmol/L。
表1. 实验室检查
1.T2DM
2.糖尿病肾病
3.超重
02、病例分析及治疗经过
该病例特点总结如下:
中年女性,糖尿病病史较长,已出现糖尿病肾病的并发症
血糖进行性恶化,长期接受胰岛素治疗,尝试过基础胰岛素+口服药(OAD)、预混胰岛素+OAD、双胰岛素+OAD,患者血糖始终未得到理想控制,尤其表现为空腹血糖不达标
曾合并右侧肾上腺腺瘤(原醛症),行手术治疗后高血压、低钾血症得以纠正,但其对糖代谢异常的影响可能持续存在
根据病例特点调整治疗方案:该患者胰岛功能较差,胰岛素分泌相对不足,但经长期胰岛素治疗仍未能将血糖控制在良好范围,且胰岛素剂量已经用到较高水平(每日36U)。结合其原醛症病史,胰岛素抵抗的情况不容忽视。为更加全面覆盖T2DM核心发病机制,以进一步改善血糖控制,遂将德谷门冬双胰岛素每日两次注射转换为德谷胰岛素利拉鲁肽20U早餐前皮下注射,保留OAD联合方案不变(二甲双胍恩格列净早晚各1粒)。
半年后(2025年2月)复查,FPG 5.27 mmol/l,UACR 110.66 mg/g。血糖维持良好控制,蛋白尿进一步减少。
03、专家点评

陈诗鸿教授
胰岛β细胞功能障碍和胰岛素抵抗是T2DM的两大核心病理生理机制。两者相互影响,涉及多个重要器官与组织,共同导致糖代谢紊乱。基础胰岛素和GLP-1RA机制互补,全面覆盖T2DM核心缺陷。德谷胰岛素利拉鲁肽作为基础胰岛素/GLP-1RA的首个FRC制剂,通过德谷胰岛素、利拉鲁肽双组分发挥协同作用,机制互补,覆盖T2DM多重病理生理机制(图1),在增强降糖疗效的同时减少不良反应[1],而且使用简便,每日一次注射,在预混胰岛素或双胰岛素转换治疗中具有多重优势。

图1. 德谷胰岛素利拉鲁肽作用机制:两组分机制互补
强化降糖
DUAL系列研究证实,德谷胰岛素利拉鲁肽能够显著降低HbA1c(降幅达2.0%),全面改善空腹血糖和餐后血糖,HbA1c<7%达标率高达89.9% [2-12]。对于预混胰岛素转换人群,DUAL II Japan研究显示,预混胰岛素血糖控制不佳T2DM患者转换为德谷胰岛素利拉鲁肽治疗可进一步改善血糖控制(HbA1c降低1.58%),体重减轻(-1.5kg)且低血糖风险低[13]。
具体到该病例,历经基础胰岛素、预混胰岛素和双胰岛素治疗,但空腹血糖始终控制不佳,最终从双胰岛素转换为FRC,治疗后2周即实现了空腹和餐后血糖双达标,且大大节约胰岛素剂量,患者应用双胰岛素每日剂量达36U,德谷胰岛素利拉鲁肽转换剂量为20U,后续减至16U,即可维持血糖达标。
该病例一方面印证了FRC在研究中展现的强效降糖效果,另一方面也引发临床思考:对于胰岛素大剂量、长期治疗效果不佳的患者,一味增加剂量或并不利于降糖,反而可能加重胰岛素抵抗。由于该患者合并肾上腺腺瘤(原醛症),醛固酮水平增加可导致更严重的胰岛素抵抗,仅通过外源性补充胰岛素难以纠正胰岛素抵抗的问题,加用GLP-1RA可很好地弥补这一缺陷。德谷胰岛素与利拉鲁肽机制互补,协同增效,仅需较小的胰岛素剂量即可实现良好血糖控制,同时还能减少大剂量胰岛素带来的低血糖和体重增加风险。
简化治疗
FRC有助于简化治疗:①减少注射次数:德谷胰岛素利拉鲁肽每日1次任意时间注射,无需严格配合进餐,减少治疗负担。该患者从双胰岛素每日2次注射转换为FRC每日1次注射,进一步简化治疗,减少注射负担。②减少OAD种类:真实世界研究显示,启用德谷胰岛素利拉鲁肽后,大多数(82.8%)T2DM患者仅需联合1种OAD[14],即“一针一片”方案。该病例转换为FRC治疗后,保留原先的一种OAD不变,从“两针一片”简化为“一针一片”,更利于提高依从性。
综上,德谷胰岛素利拉鲁肽作为基础胰岛素/GLP-1RA联合制剂,凭借协同机制,可全面覆盖胰岛素缺乏和胰岛素抵抗两大核心机制,强效降糖同时简化治疗,帮助T2DM患者实现“强化且简化”双重获益。本病例中,患者由双胰岛素转换为德谷胰岛素利拉鲁肽治疗后,长期困扰的血糖控制欠佳问题得以迅速、显著改善,同时方案简化、治疗体验更好,患者信心大增。临床上,对于预混胰岛素或双胰岛素治疗血糖控制不佳的T2DM患者,不妨跳出传统胰岛素治疗思路,转换使用德谷胰岛素利拉鲁肽,或可取得化繁为简、事半功倍的效果。
点评专家简介

陈诗鸿 教授
山东大学齐鲁第二医院内分泌代谢科主任
疑难罕见病中心主任
二级教授,博士研究生导师,博士后合作导师
中华医学会内分泌学分会委员
中国医师协会内分泌代谢科医师分会委员
中国女医师协会医体专业委员会副主任委员
中国女医师协会糖尿病与内分泌专业委员会委员
山东省医学会骨质疏松与骨矿盐疾病分会主任委员
山东省老年医学学会内分泌专业委员会主任委员
山东省研究型医院学会内分泌学分会主任委员
山东省医学会内分泌学分会副主任委员
山东省医师协会内分泌科医师分会副主任委员
病例作者简介

郑新颖 教授
北京中医药大学东方医院秦皇岛医院
主任中医师、硕士研究生导师
北京中医药大学东方医院秦皇岛医院内分泌一科副主任
中国民族医药学会甲状腺病分会理事
河北省中医药学会骨质疏松专业委员会副主委
河北省中西医结合学会络病专业委员会常委
河北省名医学会慢病管理专业委员会常委
河北省药学会内分泌代谢药物专业委员会常委
河北省中西医结合学会糖尿病足专业委员会委员
参考文献
1.德谷胰岛素利拉鲁肽注射液临床应用专家指导建议. 中华糖尿病杂志. 2023; 15(3): 209-215.
2.Gough SC, et al. Diabetes Obes Metab. 2015; 17(10): 965-973. DUAL I ext
3.Buse JB, et al. Diabetes Care. 2014; 37(11): 2926-2933. DUAL II
4.Linjawi S, et al. Diabetes Ther. 2017; 8(1): 101-114. DUAL III
5.Rodbard HW, et al. Diabet Med. 2017; 34(2): 189-196. DUAL IV
6.Lingvay I, et al. JAMA. 2016; 315(9): 898-907. DUAL V
7.Harris SB, et al. Diabetes ObesMetab. 2017; 19(6): 858-865. DUAL VI
8.Billings LK, et al. Diabetes Care. 2018; 41(5): 1009-1016. DUAL VII
9.Aroda VR, et al. Lancet Diabetes Endocrinol. 2019; 7(8): 596-605. DUAL VIII
10.Philis-Tsimikas A, et al. Diabetes Obes Metab. 2019; 21(6): 1399-1408. DUAL IX
11.Wang W, et al. J Diabetes. 2022; 14(6): 401413. DUAL I China
12.Pei Y, et al. Diabetes Obes Metab. 2021; 23(12): 26872696. DUAL II China.
13.Watada H, et al. Diabetes Ther. 2020 Jan;11(1):331-339. DUAL II Japan.
14.Romano I, Serra R. Diabetes Ther. 2024; 15(1): 145-154. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言