编者按
糖尿病视网膜病变(DR)是全球工作年龄人群致盲的主要原因之一。传统观点将其视为典型的微血管病变,但越来越多的研究清楚揭示:视网膜代谢损害并非被动伴随,而是推动神经-血管破坏的“源头病因”。在11月19~22日召开的中华医学会糖尿病学分会第二十七次学术会议(CDS 2025)上,中山大学附属第三医院陈燕铭教授围绕“糖尿病视网膜病变早期病理改变——代谢损害”这一主题展开了深入分享,从病理演进、临床证据、机制连接及治疗策略四个维度系统阐述了“代谢损害-视网膜病变”的完整框架。其目的在于推动防控前移,实现从“发现病变”到“识别代谢损害表型”的策略转变。

全球约三分之一的糖尿病患者罹患DR,我国约有1950万糖尿病患者合并DR,其中约五分之一具有威胁视力的DR,已成为工作年龄人群致盲的主要原因。1990~2020年间,全球五大致盲原因中,仅DR患病率呈持续上升趋势[1~3]。
DR早期主要表现为微血管病变和神经-血管耦联障碍(图1)。糖尿病会显著损害视网膜神经血管单元,使其互相依赖的血管、神经、胶质和免疫细胞功能受扰,具体病理改变包括神经元损伤、免疫细胞激活和血管功能障碍等。这些变化共同导致神经血管耦联障碍,进而引发血视网膜屏障破坏与视网膜血流调节紊乱。整体来看,代谢异常引发神经-血管单位受损,推动微血管病变的发生发展,是DR早期病理改变的核心机制[4~5]。
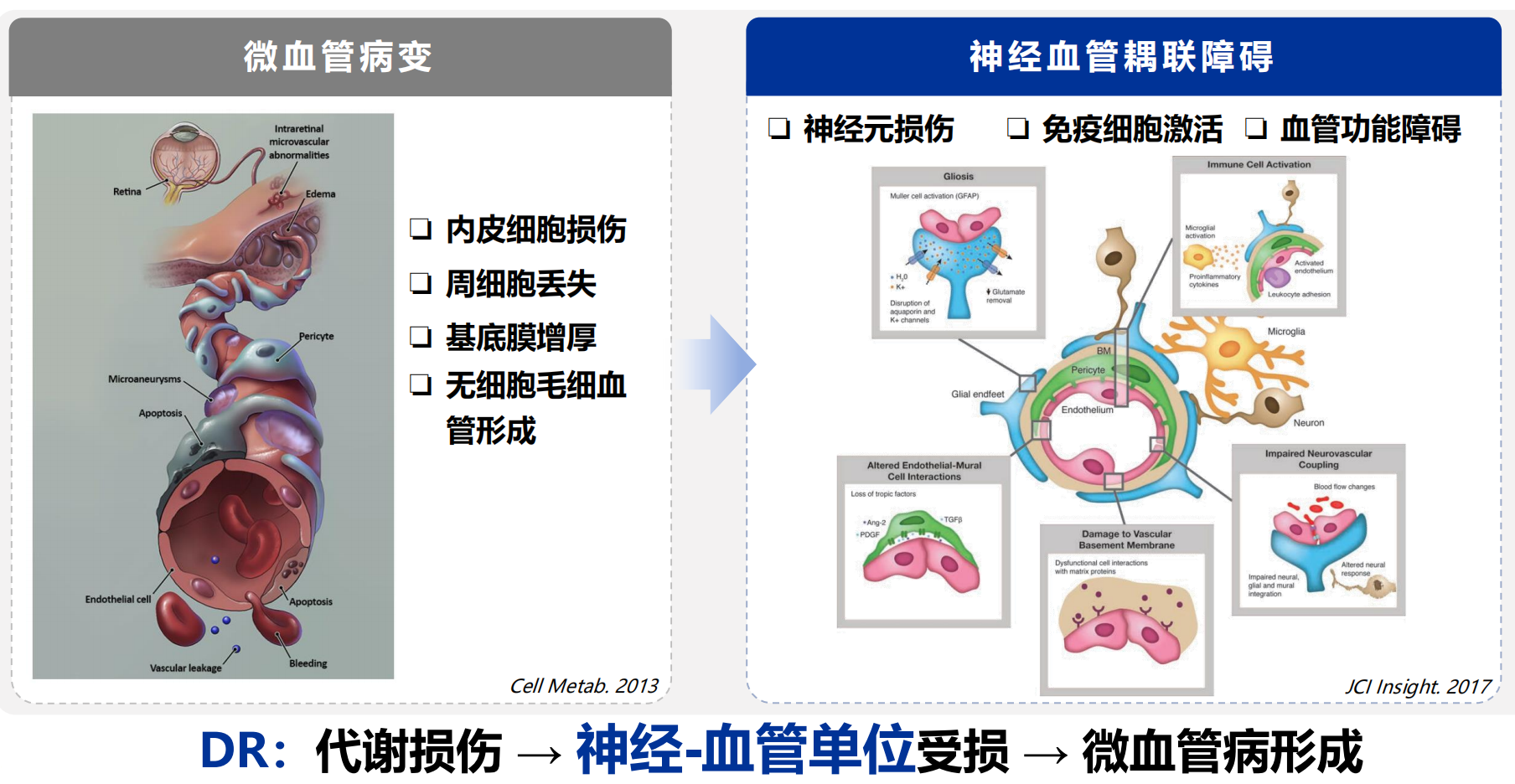
图1. DR早期病理改变
二、临床证据:代谢损害对DR的真实影响
经典临床研究(DCCT、UKPDS、ADVANCE、VADT)均表明,强化血糖控制可显著降低DR发生风险。陈燕铭教授团队的研究进一步表明,在胰岛素强化治疗后继续给予12个月基础胰岛素联合口服药物,可降低短病程2型糖尿病患者DR的发生率[6]。
同时,大量临床证据显示,降脂治疗在DR管理中不可或缺。例如,ACCORD和FIELD等研究证实,降脂药物(如非诺贝特)可显著减少黄斑水肿风险,延缓视网膜病变进程[7,8]。
血压管理同样是DR防控的重要环节。UKPDS证实,严格血压控制可降低DR进展及视力损失风险,并减少激光治疗的需求[9];DIRECT研究进一步提示,坎地沙坦可降低DR发生风险并改善病变进程[10,11]。
更重要的是,多重代谢风险因素的综合控制,如强化降糖与降脂的联合干预,可显著增强对DR进展的抑制效应[12]。因此,在代谢损害导致视网膜血管病变的过程中,综合管理血糖、血脂及血压等代谢指标,依然是当前延缓DR发展的核心防治策略。
三、机制连接:代谢损害致DR病变的分子机制
孟德尔随机化(MR)研究利用遗传变异作为“工具变量”,通过等位基因的自然随机分配推断暴露因素(如生活习惯、代谢因素)与疾病结果之间的因果关系[13]。结果显示:糖毒性层面,HbA1c与DR各阶段(包括增殖性糖尿病视网膜病变,PDR)均存在显著的因果关系;脂毒性层面,高密度脂蛋白胆固醇(HDL-C)和载脂蛋白A(ApoA)对DR的进展具有显著的保护作用;系统性损伤层面,谷丙转氨酶(ALT)与DR存在因果关联。
代谢应激状态下,高糖通过多元醇途径、蛋白激酶C(PKC)激活、己糖胺旁路与晚期糖基化终末产物(AGEs)积累等多通路,促进氧化应激与炎症反应增强,进而引发内皮细胞损伤、血管通透性升高、周细胞凋亡,构成DR分子病理经典框架(图2)[14,15]。与此同时,视网膜细胞由氧化磷酸化转向异常糖解的代谢重编程,导致能量供应低效且伴随乳酸堆积,进一步加重炎症信号与神经功能紊乱。视网膜并非单纯耗能组织,更是代谢与炎症的交汇组织,体现了DR的代谢炎症本质[16]。
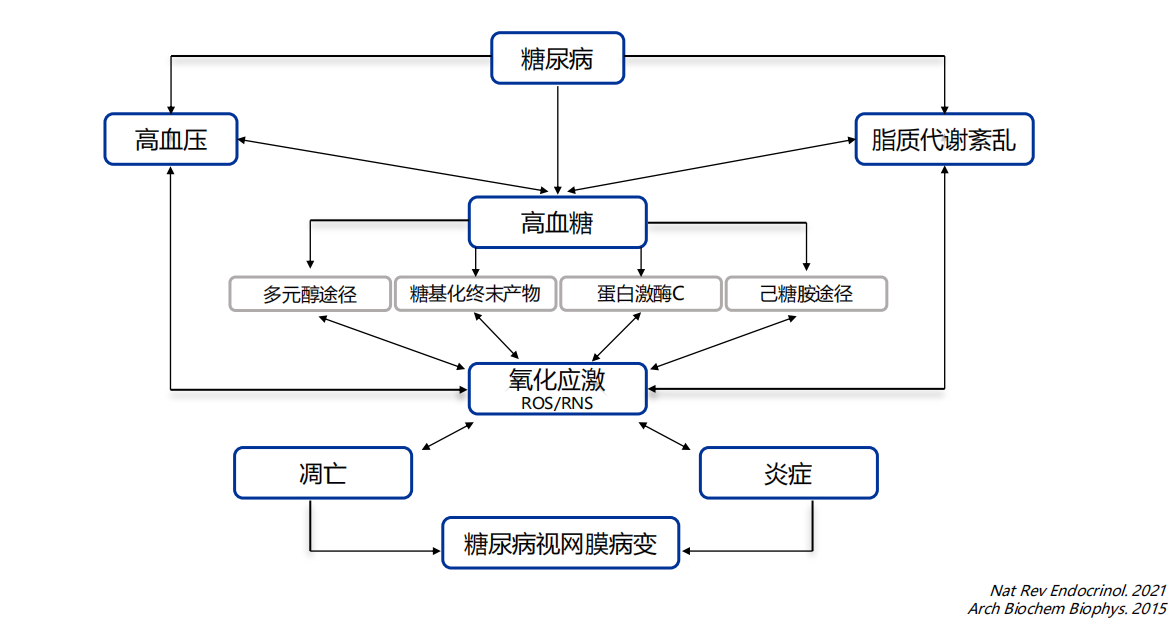
图2. DR发生发展的经典分子机制
此外,特定代谢物在DR中呈现双重作用:神经酰胺作为脂毒性介质,在DR患者玻璃体中显著升高,可激活炎症、诱导内皮细胞凋亡并破坏血视网膜屏障,靶向阻断能显著减轻小鼠视网膜血管渗漏和炎症[17];色氨酸及其代谢产物吲哚-3-丙酸(IPA)则具有抑炎与神经保护作用,DR患者血清中其水平明显下降,补充IPA可改善高糖诱导的视网膜细胞炎症[18]。
陈燕铭教授团队的研究揭示,细胞间通信网络因子1(CCN1)在DR中显著上调,通过募集中性粒细胞导致血管渗漏,引发视网膜内皮炎症反应及毛细血管功能改变[19,20];糖脂代谢紊乱会激活视网膜血管STING通路,进一步促进炎症[21];敲除内皮细胞STING可减轻视网膜炎症细胞浸润,同时,GLP-1受体激动剂(GLP-1RA)可抑制视网膜内皮细胞STING通路激活,改善炎症并保护血管完整性[22]。这些前沿成果为靶向代谢-免疫环路提供了更具靶点精准性的分子依据(图3)。
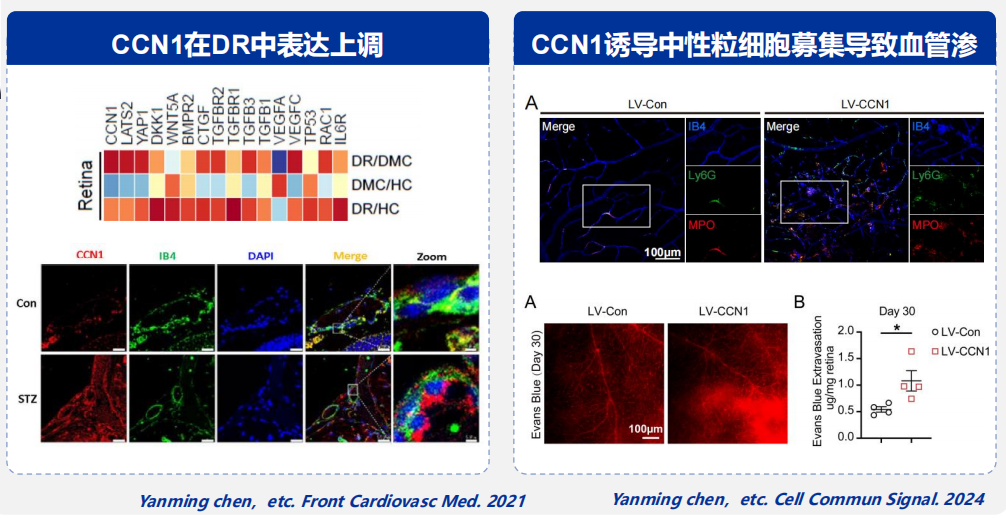
图3. 陈燕铭教授团队成果:CCN1促进DR血管损伤
四、诊断治疗:靶向代谢损害的干预策略
01、基于多组学与AI的精准诊断
多组学技术(基因组、表观组、转录组、蛋白组及代谢组)的应用,使DR在结构性病变出现前即可识别分子层面的代谢失衡。代谢组学发现,亮氨酸/异亮氨酸通路及脂质氧化产物等视网膜相关代谢物的改变早于血管损伤,可作为代谢预警信号[23]。蛋白质组学鉴定ANGPTL4、PPAR相关蛋白等DR分子标志物,并进一步筛选出PLXNB2、GDF15、REN 等血液指标,显著提升DR发生与进展预测能力[24]。此外,多维网络代谢物(如亚油酸、烟尿酸、鸟氨酸、苯乙酰谷氨酰胺等)能够较好地区分DR与非DR糖尿病患者,敏感性达96%,特异性达78%[25];循环L-酪氨酸水平下降提示DR风险及早期神经退变,其预测敏感性达86%,特异性为40%[26]。
人类视网膜单细胞多组学图谱基于大规模单核RNA与ATAC测序数据,构建了200余个转录因子的调控网络,可将全基因组关联(GWAS)风险位点或蛋白质组标志物精准定位至特定细胞类型,为DR分型及个体化干预提供依据[27]。同时,人工智能(AI)技术正从单模态影像诊断迈向多模态代谢指标融合,构建更灵敏的风险预测模型,如ARDA、RetinAI与国产系统SELENA+已进入临床应用前沿。
02、靶向代谢损害的干预路径与研发进展
在干预层面,针对代谢损害的策略不断演进。经典药物如非诺贝特通过神经保护、抗炎抗氧化及改善血管功能等途径缓解代谢损伤,其纳米滴眼液已在db/db小鼠中证实可改善视网膜血流紊乱[28]。糖尿病会导致血管神经耦联受损,引起内皮祖细胞数量减少及功能异常,进而导致谷氨酸/NMDA受体上调、神经保护因子缺乏,最终造成神经元死亡及神经胶质细胞功能紊乱。因此,围绕代谢损害可从多途径干预,包括干细胞治疗、抑制谷氨酸信号通路,以及补充神经保护因子(如PEDF、IRBP、NGF等),以改善视网膜神经及血管功能。
当前,针对代谢损害的DR干预研发聚焦三大方向:多元醇通路抑制剂(如AT-003、AT-001)、改善线粒体功能的药物(如MTP-131)、增强抗氧化防御的Nrf2激活剂等,这些策略均处于临床I/II期或转化研究阶段。同时,脂质补充、调节肠道菌群及靶向氨基酸代谢等新策略也在探索中,但仍面临血-视网膜屏障、DR表型异质性及早期疗效评估(随访时间长)等转化挑战。为突破血-视网膜屏障限制,陈燕铭教授团队开发了TAT-iRGD滴眼液递送STING抑制剂策略:通过TAT促进脂质体穿透眼部屏障到达视网膜,负载的STING抑制剂可显著改善炎症性血管病变[29]。
展望未来,DR管理将从“发现病变”前移至“识别代谢损伤表型”并提前干预。通过整合代谢指标、影像学数据、遗传风险(GWAS)、多组学数据及AI,构建更适合中国人群的代谢-DR风险模型与筛查策略;在控糖、降压、调脂基础上,辅以SGLT-2抑制剂、GLP-1RA、RAAS阻断剂等针对个体代谢损伤表型的多靶点干预,并依托内分泌科与眼科协同,最终实现DR的精准防治。
结语
DR是一种典型的代谢性视网膜病。通过及早识别个体化代谢损伤表型,辅以精准的代谢与炎症干预,有望真正阻断病变发生。未来应构建中国人群适配的风险模型,推动内分泌科与眼科合作,实现提前预测、提前分型、提前治疗的转型目标,让更多患者免于失明威胁。
参考文献
[1]Parmar MS. N Engl J Med. 2020. PMID: 32726545
[2]Lancet Diabetes Endocrino. 2019 Feb;7(2):140-149..
[3]Nat Commun. 2023 Jul 18;14(1):4296. doi: 10.1038/s41467-023-39864-w.
[4]Cell Metab. 2013 Jan 8;17(1):20-33. doi: 10.1016/j.cmet.2012.11.012
[5]JCI Insight. 2017 Jul 20;2(14):e93751. doi: 10.1172/jci.insight.93751.
[6]Chung YR, et al. Diabetes Metab J. 2019. PMID: 31902152
[7]Keech AC, et al. Lancet. 2007;370:1687–1697. PMC+1
[8]Chew EY, et al. Ophthalmology. 2014;121(12):2295–2302
[9]UKPDS Group. BMJ. 1998;317(7160):703–713.
[10]Sjølie AK, et al. Lancet. 2008;372(9647):1385–1393.
[11]Chaturvedi N, et al. Lancet. 2008;372(9647):1394-1402.
[12]N Engl J Med. 2010 Jul 15;363(3):233-44
[13]Diabetes Metab J. 2025 Sep;49(5):1087-1105. doi: 10.4093/dmj.2024.0731
[14]Antonetti DA, Silva PS, Stitt AW. Nat Rev Endocrinol. 2021 Apr;17(4):195-206. doi: 10.1038/s41574-020-00451-4. Epub 2021 Jan 19.
[15]Gong X, Rubin LP.Arch Biochem Biophys. 2015 Apr 15;572:40-48
[16]Invest Ophthalmol Vis Sci. 2025 Jul 1;66(9):24. doi: 10.1167/iovs.66.9.24
[17]Cell Metab. 2024 Jul 2;36(7):1521-1533.e5. doi: 10.1016/j.cmet.2024.04.013. Epub 2024 May 7.
[18]Gut. 2025 Nov 5:gutjnl-2025-336180.doi: 10.1136/gutjnl-2025-336180
[19]Yanming chen, et al. Front Cardiovasc Med. 2021 Aug 11;8:689318. doi: 10.3389/fcvm.2021.689318. eCollection 2021.
[20]Yanming chen,et al.Cell Commun Signal. 2024 May 16;22(1):275. doi: 10.1186/s12964-024-01653-3.
[21]Yanming chen,et al.J Nutr Biochem. 2023 Feb;112:109213. doi: 10.1016/j.jnutbio.2022.109213
[22]Yanming chen,et al.Acta Pharm Sin B.?2024 Jun;14(6):2613-2630.doi: 10.1016/j.apsb.2024.03.011.
[23]Invest Ophthalmol Vis Sci. 2017 May 1;58(6):BIO88-BIO98. doi: 10.1167/iovs.17-21809.
[24]Nat Commun. 2025 Nov 25;16(1):10498. doi: 10.1038/s41467-025-65516-2.
[25]BMJ Open Diabetes Res Care. 2021 Feb;9(1):e001443.
[26]Cardiovasc Diabetol. 2024 Dec 18;23(1):439. doi: 10.1186/s12933-024-02535-1.
[27]Cell. 2023 Oct 26;186(22):4868-4884.e12. doi: 10.1016/j.cell.2023.09.012. Epub 2023 Oct 19.
[28]Pharmaceutics. 2022 Feb 9;14(2):384. doi: 10.3390/pharmaceutics14020384.
[29]Biomaterials. 2025 Dec;323:123424. doi: 10.1016/j.biomaterials.2025.123424. Epub 2025 May 19.
2 comments









 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言