多肽和蛋白质类药物已被发现可用于多种疾病治疗,但只能通过注射给药以及较短的作用时间限制了其在临床的广泛应用。研究人员利用各种分子工程学技术对其进行改造,旨在克服以上限制,其中一项被称为“脂肪酸酰化”的技术已成功应用于多种肽类药品的研发,胰岛素是其应用最成功的领域之一。近期,成功利用该技术研发的全球首个胰岛素周制剂——依柯胰岛素即将问世。那么,这个潜力无限的技术的基本原理是什么?有哪些结构要素?其延长药物作用时间的具体机制有哪些?基础胰岛素又是如何通过这项技术实现从日制剂到周制剂的突破?一篇发表在著名杂志Nature子刊的综述[1]对该技术进行了全面介绍,本刊特邀北京协和医院内分泌科肖新华教授择其部分精要撰写成稿,以飨读者。


什么是脂肪酸酰化技术?
肽类药物可用于治疗多种疾病,药物开发潜力巨大,但因其在体内容易被酶降解,或因肾脏清除及受体介导的清除作用而导致半衰期较短,因此在临床应用的一大挑战为需要频繁注射给药,这严重影响了患者的治疗依从性[2,3]。为了延长肽类制剂的半衰期,科研工作者使用多种分子工程学技术对肽类分子进行改造,通过大量研究而取得了重大进展,其中脂肪酸酰化技术是成功应用的代表之一。
脂肪酸酰化技术的基本原理是脂化过程。“脂化”普遍存在于各种蛋白质翻译和翻译后的修饰过程中,不同脂肪酸侧链通过与肽链连接,赋予蛋白质独特的属性。脂肪酸酰化技术就是基于这一原理,通过人工手段,为肽类连接脂肪酸侧链,增加其自我聚合力以及与白蛋白的结合力,降低肾脏和受体介导的清除率,最终达到延长其半衰期的目的[4]。
脂肪酸酰化技术的结构要素包括脂肪酸侧链、连接子、间隔子和主链(图1)。
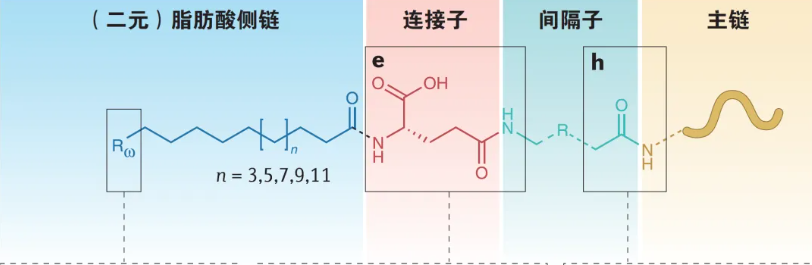
图1. 脂肪酸酰化技术的结构要素
脂肪酸侧链
研究发现,与一元脂肪酸侧链相比,二元脂肪酸侧链与白蛋白的亲和力更强,并由于烷基链ω端增加的羧基而获得更长的半衰期[5,6]。此外,白蛋白的亲和力与脂肪酸的长度呈强相关性。迄今为止,研究发现1,18-十八烷二酸(C18二元酸)和1,20-二十烷二酸(C20二元酸)是与白蛋白亲和力最强的两种脂肪酸。
连接子
连接子是指将脂肪酸侧链连接至间隔子或肽类主链的结构。
间隔子
间隔子存在于肽链与连接子之间,目的是增加空间距离以减轻结合白蛋白后对目标受体结合力的影响。如无间隔子,由于肽链与白蛋白距离较近,可能导致与同源受体的结合受到负面影响。在多数情况下,较长的间隔子使得白蛋白对肽类和受体结合的负面影响较小,但另一方面,较短的间隔子或无间隔子使得肽类与白蛋白之间的物理距离更近,因而可能在空间上保护肽类,避免被降解,从而延长其半衰期。因此,所选择的间隔子的长度非常重要,一定要综合考虑所需的受体结合水平和期望的半衰期,在二者之间找到一个平衡点。
主链
蛋白质或肽类的主链中与脂肪酸侧链结合的位置非常重要,会对最佳效力和半衰期产生直接的影响。
总之,脂肪酸酰化技术通过以上结构的改变达到延长肽类半衰期的目标,其主要作用机制包括:首先,通过形成白蛋白-多肽复合物,脂肪酸酰化显著增加肽类的分子量,皮下注射后组织内扩散速率和透过毛细血管壁的速率显著下降,同时分子量的增加也会降低肽类经肾脏的清除;其次,脂肪酸酰化技术可以介导肽类单体之间的自我聚合,形成“多聚体”,更高程度的自我聚合同样可以降低药物的皮下吸收速率;最后,脂肪酸酰化的肽类药物可以与循环中的白蛋白发生强力且可逆的结合,从而在循环中形成“储库”,进而延长药代动力学半衰期。
脂肪酸酰化技术应用最成功的领域主要为多肽和小分子蛋白质,基础胰岛素类似物是其重要代表。人胰岛素是分子量为5808 Da的小分子蛋白质,包含A链和B链,分别包含21个和30个氨基酸残基,两条肽链之间以两个二硫键相连接[7]。胰岛素的氨基酸序列高度保守,人胰岛素分子中有3个位置可以酰化,分别为A1、B1和B29。其中,B29位是最适合进行修饰的,因为A1位酰化将干扰胰岛素与受体的结合,而B1位酰化会增加胰岛素分子的疏水性,进而影响溶解度[8]。
利用脂肪酸酰化技术延长胰岛素作用时间的首个成功实例是将一种肉豆蔻酸(C14脂肪酸)连接到人胰岛素分子上,形成一种长效基础胰岛素类似物,即地特胰岛素[9]。通过将肉豆蔻酸(C14脂肪酸)改成C16二元脂肪酸后,得到了半衰期更长的新一代超长效基础胰岛素类似物——德谷胰岛素[10]。
为了进一步延长基础胰岛素类似物的作用时间,减少注射次数,研究人员在胰岛素的B29位上通过“L-γGlu-2×Ado”这一“连接子-间隔子”结构,连接了一个二十烷二酸(C20二元酸)侧链,进一步增加胰岛素与白蛋白的亲和力。另外,通过将A14位的酪氨酸替换为谷氨酸(A14E)、B16位的酪氨酸替换为组氨酸(B16H)、B25位的苯丙氨酸替换为组氨酸(B25H),进一步降低了胰岛素与受体的亲和力,从而减少受体介导的清除[11,12]。
经过这一系列调整,研究者成功研发出了首个每周仅需注射一次的基础胰岛素周制剂——依柯胰岛素,其与白蛋白结合的亲和力比地特胰岛素高10倍[13]。在白蛋白浓度为1.5%的情况下,与人胰岛素相比,依柯胰岛素与受体的相对亲和力为0.03%,大幅降低了受体介导的清除[13]。
一项在2型糖尿病患者中进行的双盲、双模拟Ⅰ期多剂量递增试验发现,分别每周注射一次依柯胰岛素12、20、24 nmol/kg,其半衰期可达196 h,满足每周一次注射需求[14](图2);并且,依柯胰岛素每周一次注射,稳态下葡萄糖钳夹试验显示的降糖疗效在一周7天内日间分布接近平均[14](图3)。
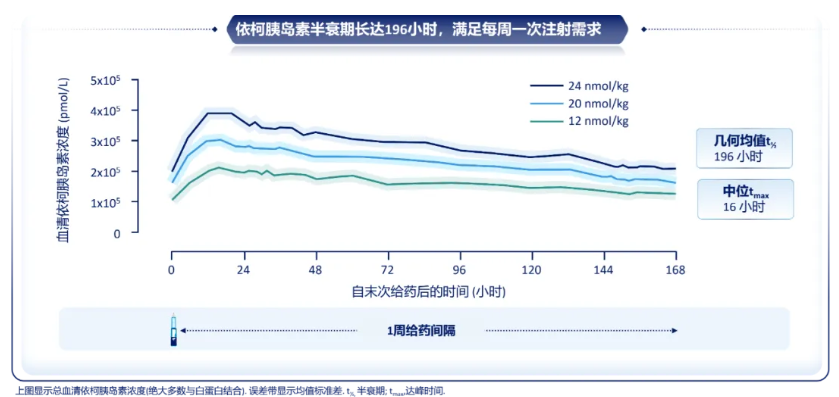
图2. 依柯胰岛素多次注射后的药代动力学特征曲线
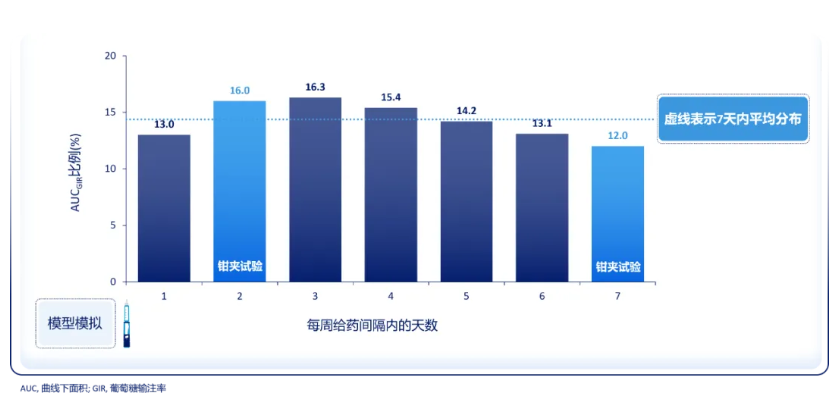
图3. 稳态时依柯胰岛素在一周7天内降糖疗效的日间分布
目前,依柯胰岛素已完成全部3a期临床研究(ONWARDS研究项目)[15-20],正等待美国、欧盟和中国等多地的上市批准。即将到来的胰岛素周制剂将有望重塑基础胰岛素治疗模式,注射次数从日制剂的每年365次减少到52次,这将大大减少患者注射负担,提高患者治疗的依从性和持续性。
综上,通过脂肪酸酰化技术,全球首个基础胰岛素周制剂——依柯胰岛素在皮下注射后,获得强大且可逆的与白蛋白结合的能力,在循环中与白蛋白结合形成储库,并通过降低与胰岛素受体的亲和力,减少受体介导的清除。在多种机制共同作用下,活性胰岛素单体从储库中缓慢、持续地释放,如“涓涓细流”作用于靶器官和组织,在保留降糖疗效的同时有效延长体内药代动力学半衰期,率先实现从日制剂到周制剂的创新性突破。
脂肪酸酰化是一项经过临床验证的具有多用途的研发技术,可用于优化多肽和蛋白质类药物的药理学特性,已成功应用于一系列药物研发。该技术可以延长天然肽类分子的半衰期,从而实现每日一次、每周一次甚至更低频率的给药。未来,脂肪酸酰化还可应用于辅助生物药品的口服递送,并可能改变其在不同组织中的分布等。
脂肪酸酰化技术安全可靠,改造后的药物化学性质明确,并可以通过多种药用化学方法优化,实现具有成本效益的大规模生产。随着该技术在药物研发中的广泛应用,其未来有望在肽类生物制药领域释放出更大的潜能。
参考文献
1. Kurtzhals P, et al. Derivatization with fatty acids in peptide and protein drug discovery. Nat Rev Drug Discov. 2023; 22(1): 59-80.
2. Strohl WR. Fusion proteins for half-life extension of biologics as a strategy to make biobetters. BioDrugs. 2015; 29(4): 215-239.
3. Evans M, et al. Adherence to and persistence with antidiabetic medications and associations with clinical and economic outcomes in people with type 2 diabetes mellitus: a systematic literature review. Diabetes Obes Metab. 2022; 24(3): 377-390.
4. Kurtzhals P, et al. Albumin binding of insulins acylated with fatty acids: characterization of the ligand–protein interaction and correlation between binding affinity and timing of the insulin effect in vivo. Biochem J. 1995; 312(Pt 3): 725-731.
5. Gao X, et al. Fatty acylation enhances the cellular internalization and cytosolic distribution of a cystine-knot peptide. iScience. 2021; 24(11): 103220.
6. Bech EM, et al. Half-life extending modifications of peptide YY3–36 direct receptor-mediated internalization. Mol Pharm. 2019; 16(8): 3665-3677.
7. Nicol DS, Smith LF. Amino-acid sequence of human insulin. Nature. 1960; 187: 483-485.
8. Havelund S, et al. Characterization of B1 and B29 fatty acid acylated insulins. Diabetologia. 1995; 38: A192.
9. Havelund S, et al. The mechanism of protraction of insulin detemir, a long-acting, acylated analog of human insulin. Pharm Res. 2004; 21(8): 1498-1504.
10. Jonassen I, et al. Design of the novel protraction mechanism of insulin degludec, an ultra-long-acting basal insulin. Pharm Res. 2012; 29(8): 2104-2114.
11. Ludvigsen S, et al. A structural switch in a mutant insulin exposes key residues for receptor binding. J Mol Biol. 1998; 279(1): 1-7.
12. Ludvigsen S, et al. High-resolution structure of an engineered biologically potent insulin monomer, B16 Tyr→His, as determined by nuclear magnetic resonance spectroscopy. Biochemistry. 1994; 33(26): 7998-8006.
13. Kjeldsen TB, et al. Molecular engineering of insulin icodec, the first acylated insulin analog for once-weekly administration in humans. J Med Chem. 2021; 64(13): 8942-8950.
14. Nishimura E, et al. Molecular and pharmacological characterization of insulin icodec: a new basal insulin analog designed for once-weekly dosing. BMJ Open Diabetes Res Care. 2021; 9: e002301.
15. Rosenstock J, et al. Weekly Icodec versus Daily Glargine U100 in Type 2 Diabetes without Previous Insulin. N Engl J Med. 2023 Jul 27; 389(4): 297-308.
16. Philis-Tsimikas A, et al. Switching to once-weekly insulin icodec versus once-daily insulin degludec in individuals with basal insulin-treated type 2 diabetes (ONWARDS 2): a phase 3a, randomised, open label, multicentre, treat-to-target trial. Lancet Diabetes Endocrinol. 2023 Jun; 11(6): 414-425.
17. Lingvay I, et al. Once-Weekly Insulin Icodec vs Once-Daily Insulin Degludec in Adults With Insulin-Naive Type 2 Diabetes: The ONWARDS 3 Randomized Clinical Trial. JAMA. 2023 Jul 18; 330(3): 228-237.
18. Mathieu C, et al. Switching to once-weekly insulin icodec versus once-daily insulin glargine U100 in individuals with basal-bolus insulin-treated type 2 diabetes (ONWARDS 4): a phase 3a, randomised, open-label, multicentre, treat-to-target, non-inferiority trial. Lancet. 2023 Jun 10; 401(10392): 1929-1940.
19. Bajaj HS, et al. Once-Weekly Insulin Icodec With Dosing Guide App Versus Once-Daily Basal Insulin Analogues in Insulin-Naive Type 2 Diabetes (ONWARDS 5) : A Randomized Trial. Ann Intern Med. 2023 Nov; 176(11): 1476-1485.
20. Russell-Jones D, et al. Once-weekly insulin icodec versus once-daily insulin degludec as part of a basal-bolus regimen in individuals with type 1 diabetes (ONWARDS 6): a phase 3a, randomised, open-label, treat-to-target trial. Lancet. 2023 Nov 4; 402(10413): 1636-1647.
2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言