编者按:葡萄糖激酶基因(GCK)失活突变所致的葡萄糖激酶功能障碍导致的糖尿病是单基因糖尿病(MDM)的常见类型,GCK基因杂合突变主要表现为青少年起病的成人型糖尿病(MODY),简称为GCK-MODY,并由于葡萄糖感知缺陷常引起家族性轻度空腹高血糖。GCK-MODY的血糖谱、血脂谱、糖尿病相关慢性并发症风险与其他类型的糖尿病特点有所区别,因此其管理方案不同。既往研究显示,胰岛素、二甲双胍、磺脲类药物和格列奈类药物对GCK-MODY患者的血糖控制无效,即在停用上述药物前后患者糖化血红蛋白(HbA1c)水平无明显变化,然而新型降糖药物对此类患者是否有效尚未可知。
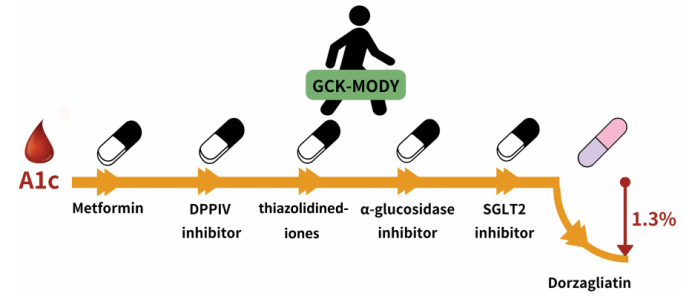
近期,北京大学人民医院纪立农教授和任倩教授等在Diabetes Care杂志公布了一例GCK-MODY患者自确诊后长期随访7年的诊治经验,结果显示,多种新型降糖药物(噻唑烷二酮类、二肽基肽酶IV抑制剂[DPP-4i]、α-糖苷酶抑制剂[AGI]、 钠-葡萄糖共转运蛋白2抑制剂[SGLT2i])均未能有效控制GCK-MODY患者的血糖,而多格列艾汀治疗6个月后却显著降低HbA1c达1.3%,这为多格列艾汀可精准治疗GCK-MODY提供了临床证据。

要点一览
既往研究结果显示,二甲双胍、胰岛素和胰岛素促泌剂不能改善GCK-MODY患者的HbA1c水平。
该病例长期随访结果显示:新型降糖药物(噻唑烷二酮类药物、DPP-4i、AGI和SGLT2i)规律治疗4.5年未降低GCK-MODY患者的HbA1c水平,而转为多格列艾汀治疗6个月后有效且安全地降低HbA1c水平达1.3%。
临床意义:多格列艾汀通过纠正GCK失活突变所致的葡萄糖激酶功能障碍导致的高血糖并使血糖正常化,进一步印证其增强葡萄糖激酶活性的作用机制,为GCK-MODY患者的精准治疗提供新方法。
患者基本信息
男,41岁,2015年在一次体检中被诊断为2型糖尿病。诊断时,体重指数(BMI)21.45 kg/m2、空腹血糖(FBG)7.15 mmol/L、HbA1c6.8%(51 mmol/mol)、甘油三酯(TG)0.44 mmol/L。经过1年的二甲双胍单药治疗(1500 mg/d),HbA1c水平仍为7%(53 mmol/mol)、FBG水平为7.41 mmol/L。
其母亲(BMI 20 kg/m2)于23年前被诊断为2型糖尿病,经二甲双胍(2000 mg/d)和阿卡波糖(150 mg/d)治疗16年后FBG为7.54 mmol/L、HbA1c水平为6.9%(52 mmol/mol)。其儿子和女儿分别为9岁和6岁,HbA1c分别为6.9%(52 mmol/mol)和6.5%(48 mmol/mol)。
该患者的临床特征符合GCK-MODY的DNA筛选标准。基因测序显示,GCK的第9外显子出现杂合突变(p.Val412Glu),其母亲和两个孩子均携带相同的基因突变。该患者于2016年被诊断为GCK-MODY。
治疗过程
二甲双胍、西格列汀、吡格列酮、阿卡波糖和恩格列净规律治疗4.5年未改善GCK-MODY患者的HbA1c水平。
确诊后,患者停用二甲双胍6个月,HbA1c水平无变化。从2016~2023年,患者在接受常规门诊随访时尝试了几种口服降糖药物,如二甲双胍、西格列汀、吡格列酮、阿卡波糖和恩格列净。然而这些降糖药物并未降低HbA1c(7.0±0.2%[53±2 mmol/mol]),其范围为6.8%~7.4%(51~57 mmol/mol)。不同药物治疗期间HbA1c水平波动如下:二甲双胍6.9%~7.1%(52~54 mmol/mol)、西格列汀6.8%~7.1%(51~54 mmol/mol)、吡格列酮6.8%~7.2%(51~55 mmol/mol)、阿卡波糖6.8%~7.2%(51~55 mmol/mol)、恩格列净HbA1c7%(53 mmol/mol)(说明治疗期间HbA1c无变化)。在药物治疗期间,患者未出现酮症。
多格列艾汀治疗6个月显著降低HbA1c达1.3%
2023年5月,患者开始接受多格列艾汀75 mg BID治疗,3个月后,HbA1c水平从7.4%降至6.3%(图1)。继续治疗3个月后,HbA1c水平进一步降至6.1%。同时评估了多格列艾汀对该患者肝肾功能以及脂质和血清尿酸水平的影响。总体而言,在接受多格列艾汀治疗6个月后,患者TG水平略有升高,但仍保持在正常范围内,在此期间,未报告发生低血糖事件。
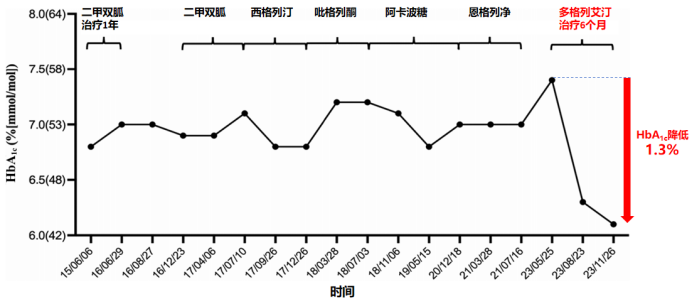
图1. 不同药物治疗期间HbA1c波动情况
总结与展望
GCK-MODY患者一般表现为轻度无症状性高血糖,90%的患者HbA1c范围为5.8 ~7.6%(40~60 mmol/mol);糖尿病并发症风险低,当患者HbA1c>7%(53 mmol/mol)时并发症风险有可能升高。GCK-MODY患者误诊率、误治率较高,因为一般为无症状性轻度血糖,往往被忽视,未明确诊断;有些被当做早发2型糖尿病进行口服降糖药物甚至胰岛素治疗。
对于GCK-MODY患者,一般无需降糖药物治疗,生活方式干预控制血糖即可,建议每年复查1次HbA1c[2]。然而,在一项关于GCK-MODY自然史的长期随访研究中,患者出现了胰岛素抵抗和糖耐量下降,这可能是由其他多基因决定因素和环境因素引起的。日本一项GCK-MODY患者队列研究显示,25%有胰岛素抵抗,同时成人HbA1c水平高于儿童。GCK-MODY是由GCK失活突变所致的葡萄糖激酶功能障碍导致的单基因糖尿病,血糖谱、血脂谱、糖尿病相关慢性并发症风险与其他类型的糖尿病有所区别,因此其管理方案不同。研究发现,胰岛素、二甲双胍、磺脲类和格列奈类药物治疗对GCK-MODY患者的血糖控制无效。
多格列艾汀是全球首个经过我国临床评价后获批上市的葡萄糖激酶激活剂(GKA),具有与其他降糖药物完全不同的作用机制,可同时靶向胰腺和肝葡萄糖激酶,通过与P环上的葡萄糖激酶的变构位点结合,增强葡萄糖激酶活性,提高机体对血糖的控制能力,改善受损的葡萄糖刺激的胰岛素分泌能力,从而改善2型糖尿病患者的血糖控制。
多格列艾汀在GCK-MODY患者中的作用也有迹可循。去年发表在Diabetes杂志上的一项临床研究发现[3],多格列艾汀可直接提高GCK-MODY患者胰岛素的分泌能力和葡萄糖敏感性,并增加突变的葡萄糖激酶的活性,这表明多格列艾汀可能有助于改善GCK-MODY患者GCK失活突变所致的葡萄糖激酶功能障碍,且不同基因突变的葡萄糖激酶对多格列艾汀治疗的反应不同。GCK-MODY患者GCK基因是杂合突变,其仍可合成具有活性的葡萄糖激酶,因而GKA可与具有活性的葡萄糖激酶结合并增强其作用,代偿因为基因突变所导致的酶活性缺陷。此外,不同的GKAs作用机制略有不同,对不同GCK-MODY突变的个体可能具有不同的治疗效果。
迄今,噻唑烷二酮类、DPP-4i和SGLT2i在GCK-MODY患者临床管理中的疗效尚未见报道。该例患者使用上述新型药物治疗后血糖控制并不理想,而使用多格列艾汀治疗6个月后HbA1c降低达1.3%,表明多格列艾汀可能是GCK-MODY患者精准治疗的有效方法,尤其是在胰岛素抵抗和HbA1c>7%的长期慢性并发症风险高的患者中。需要提醒的是,来自病例报告的证据不足以改变临床实践,因此,在提出临床建议之前,需要对GKA治疗GCK-MODY的长期有效性和安全性结果进行随机对照试验。
总之,多格列艾汀有效改善了GCK-MODY患者的血糖控制,这为未来GCK-MODY的精准治疗提供了一种可能的新策略,尤其是对于HbA1c>7%或慢性并发症风险高和其他降糖药物治疗无效的GCK-MODY患者。
参考文献:
1. Zhao Y,et al. Diabetes Care . 2024 May 1:dc232417. doi: 10.2337/dc23-2417. Online ahead of print.
2. 中华医学会内分泌学分会内分泌罕见病学组. 中华糖尿病杂志,2022,14(4):298-306.
仅供医疗卫生专业人士学术沟通使用











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言