编者按
胰高糖素样肽-1受体激动剂(GLP-1RA)已成为2型糖尿病(T2DM)综合管理的重要治疗选择,口服制剂的问世更是拓宽了其临床应用边界。作为全球首个且目前唯一获批上市的口服GLP-1RA,司美格鲁肽片填补了该领域的治疗空白,备受临床关注。近期公布的ACHIEVE-3研究数据,再次引发关于口服GLP-1RA的热议。然而,透过数据表象进行深入剖析,探讨药物的长期价值,仍是临床决策的关键所在。本文旨在系统解析口服司美格鲁肽如何凭借其经临床验证的分子设计、科学的剂量策略、良好的安全耐受性,以及目前唯一拥有心血管硬终点获益证据的地位,在口服GLP-1RA中彰显其独特的临床价值。
一、分子基础:94%高同源性赋予的不仅是靶向性,更是长期用药的安全性底气
口服司美格鲁肽的主要活性成分为司美格鲁肽分子,其本身未经额外结构修饰,而是通过与渗透促进剂N-(8-[2-羟基苯甲酰基]-氨基)辛酸钠(SNAC)共同制备,突破胃肠道粘膜屏障以实现吸收(图1)[1]。该药的核心竞争力源于其高度优化的分子结构——司美格鲁肽分子在天然GLP-1基础上仅进行两处氨基酸替换并连接脂肪酸侧链,与天然GLP-1同源性高达94%[2]。
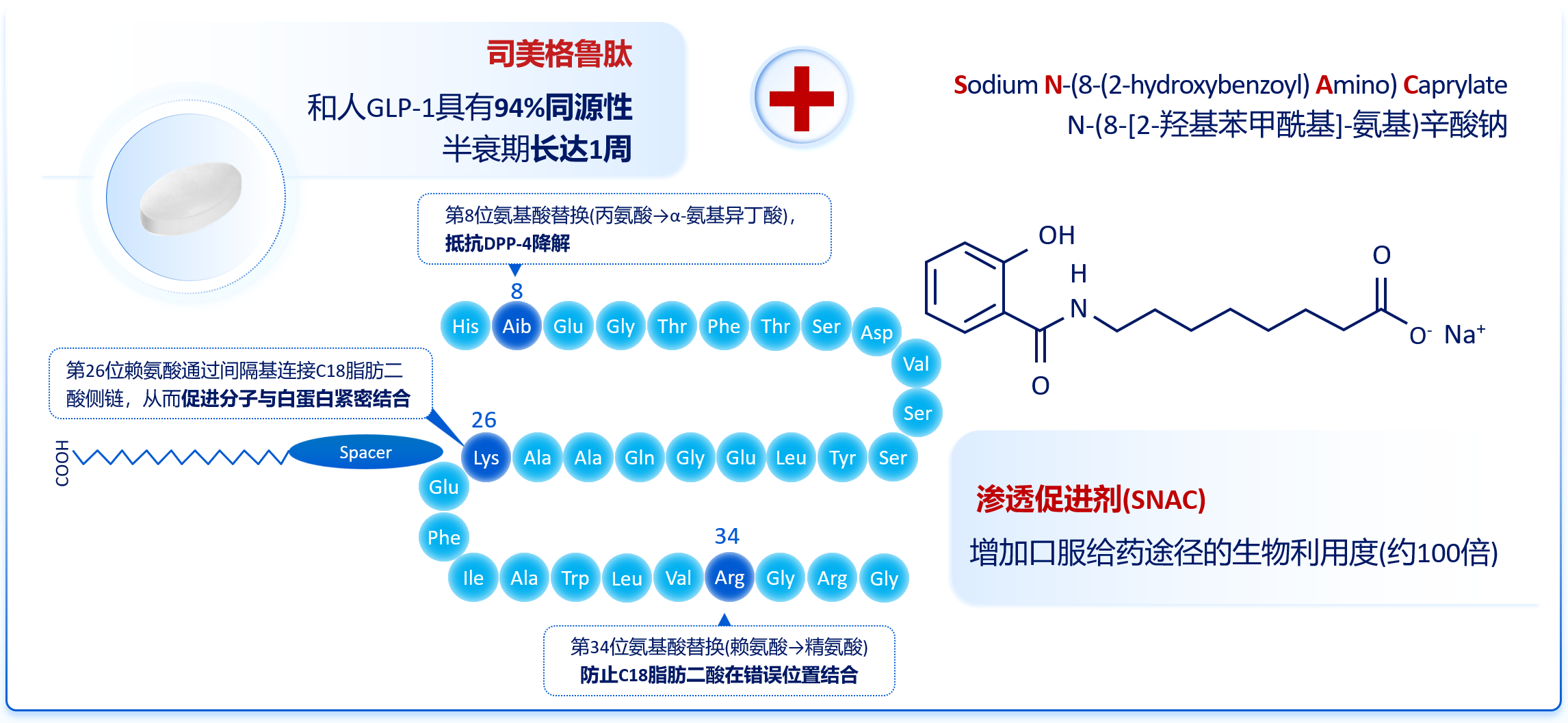
图1. 司美格鲁肽片:司美格鲁肽分子与SNAC的强强联合
这一高度保守的氨基酸序列结构不仅确保了其对GLP-1受体的高亲和力,也决定了其体内代谢产物的结构与功能。高同源性的GLP-1RA可被二肽基肽酶Ⅳ及中性内肽酶代谢,形成与内源性GLP-1接近的代谢片段[2]。研究表明,GLP-1的某些代谢产物如GLP-1(28-36)片段仍具有保护胰岛β细胞、改善糖脂代谢、调节肝脏功能、控制体重及心血管保护等多重生物学效应[3-7]。
由此引出一个值得深思的问题:当追求更强效的受体激动时,是否应更全面考量分子代谢路径的生物学意义?对于与天然结构差异显著的新型分子,其代谢产物的生物学活性、长期蓄积的潜在影响,尚待明晰。司美格鲁肽所遵循的“高同源性”设计,体现的是对人体复杂生理环境的敬畏。对于需要坚持不懈长期管理的慢病,基于审慎选择带来的安全性和耐受性是保障患者长期获益的基础。
二、剂量策略:注重疗效与耐受性的平衡,个体化选择剂量
口服司美格鲁肽借助SNAC实现胃内跨细胞吸收(图2)[8]。其T2DM剂量策略的制定基于严谨的临床药理学依据:300 mg SNAC剂量可支持司美格鲁肽达到最大血药浓度,而3 mg qd起始、每月递增至7 mg qd或14 mg qd维持剂量的滴定方案,则是在确保疗效与胃肠道耐受性之间取得的最佳平衡[9,10]。
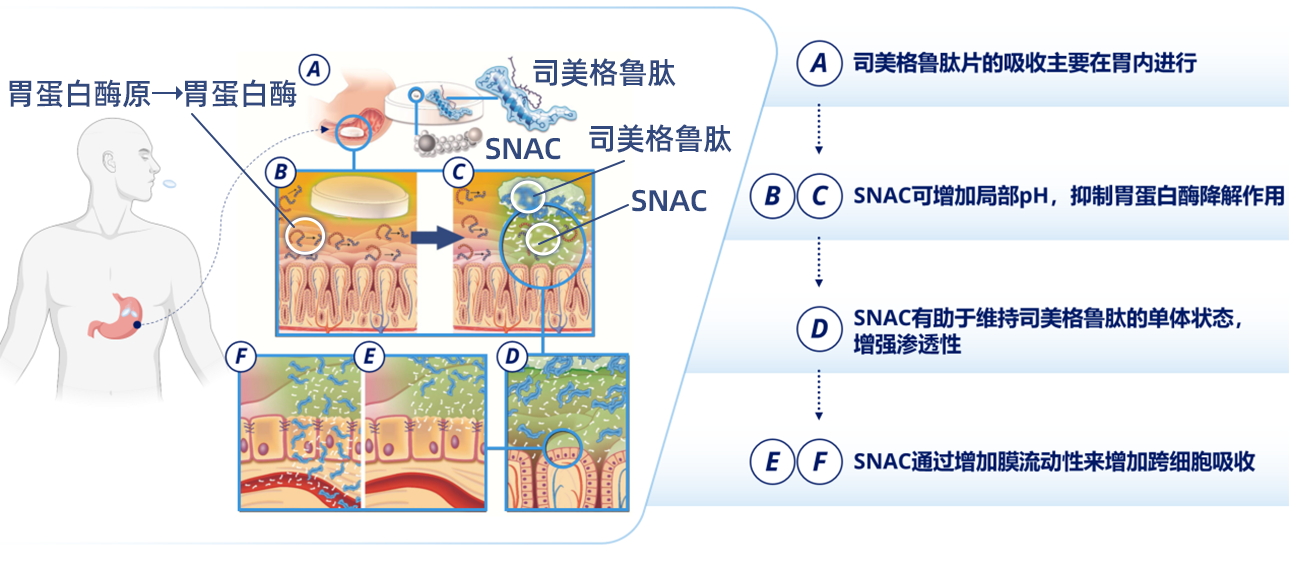
图2. SNAC促进司美格鲁肽吸收作用机制
在T2DM人群中,PIONEER系列研究证实司美格鲁肽片7 mg和14 mg带来明确临床获益:HbA1c最大降幅达1.6%,达标率(HbA1c<7%)最高达92.3%;同时,体重最多下降5.0 kg、收缩压最大降幅达7 mmHg,并显著改善血脂谱(图3)[11-22]。
口服司美格鲁肽更高剂量亦彰显出强大药理潜力:在PIONEER PLUS研究(T2DM患者)中,14 mg、25 mg、50 mg组的HbA1c降幅分别为1.5%、1.8%和2.0%,体重降幅分别为4.7%、7.3%和8.5%[23];而在OASIS 4研究(非糖尿病但伴有肥胖或超重及相关合并症人群)中,25 mg组平均体重下降16.6%,其中34%患者减重≥20%[24]。正是基于OASIS 4研究,司美格鲁肽片成为全球首个获批减重适应症的口服GLP-1RA[25]。

图3. PIONEER系列研究:司美格鲁肽片强效降糖、显著减重、降压调脂,安全性良好
综上,司美格鲁肽片形成了“降糖低剂量、减重高剂量”的科学分层策略,精准对接T2DM与肥胖的不同临床管理需求。需指出的是,ACHIEVE-3研究[26]中,orforglipron使用了与其减重研究ATTAIN 1[27]中相同的较高剂量(12 mg和36 mg),而对照药物司美格鲁肽片则仅使用了T2DM治疗剂量(7 mg和14 mg)。高剂量会取得相对更好的降糖减重效果,似乎并不令人意外。
三、耐受性与依从性:在疗效之外的真实世界临床价值考量
胃肠道不良反应是制约GLP-1RA持续治疗的主要瓶颈。口服司美格鲁肽在PIONEER系列研究(纳入全球超过9000例T2DM患者)中证实,其胃肠道事件多为轻中度、主要发生于剂量递增期、持续时间较短,绝大多数患者可耐受,且中国人群数据与全球一致[11-22,28-30](图4)。
ACHIEVE-3研究[26]恰恰印证了司美格鲁肽片的耐受性优势。数据显示,orforglipron组的恶心发生率(12 mg组26%、36 mg组27%)显著高于司美格鲁肽组(7 mg组13%、14 mg组21%);呕吐发生率同样更高(orforglipron组17%和17% vs. 司美格鲁肽组8%和10%);腹泻和便秘也呈现类似关系[26,31]。而且,orforglipron组总体胃肠道不良事件发生率更高(12 mg组59%、36 mg组58%),且未见明显剂量依赖性[26,31]——这意味着即使采用低剂量起始,患者仍存在较高的胃肠道不良反应风险,通过剂量递增可能无法改善耐受性;而司美格鲁肽组的发生率更低(7 mg组37%、14 mg组45%),且呈剂量依赖性[26,31],提示其剂量递增策略能够帮助患者逐步适应,从而降低胃肠道不良反应风险。相应地,司美格鲁肽组因不良事件或胃肠道反应导致的停药率均更低[26](表1)。
表1. ACHIEVE-3研究中安全性人群的不良事件发生情况
在真实世界临床实践中,较低的不良反应发生率和停药率是确保治疗长期有效的重要前提。对任何药物而言,若因耐受性问题导致患者终止治疗,即便在降糖或减重方面具有良好疗效,其临床价值也将大打折扣。口服司美格鲁肽在大规模人群中验证出的良好耐受性,是提升长期治疗依从性、优化患者治疗体验的可靠保障,也是其临床价值的重要组成。
四、心血管获益:以硬终点为依据的临床决策考量
现行国内外指南(如ADA指南、CDS指南)一致推荐,对于合并动脉粥样硬化性心血管疾病(ASCVD)或其高危因素的T2DM患者,优先使用具有确证心血管获益证据的药物,如GLP-1RA[32,33]。这已成为临床决策的一项重要标准。
口服司美格鲁肽凭借SOUL研究成为目前全球唯一拥有确证心血管获益证据的口服GLP-1RA[34]。这项纳入9650例合并ASCVD和/或慢性肾脏病的T2DM患者、中位随访49.5个月的CVOT证实,口服司美格鲁肽显著降低主要心血管不良事件(MACE)风险达14%,其中非致死性心肌梗死风险降低达26%(图5)。在占比高达23.4%的亚洲人群中,MACE降幅达27%[34]。
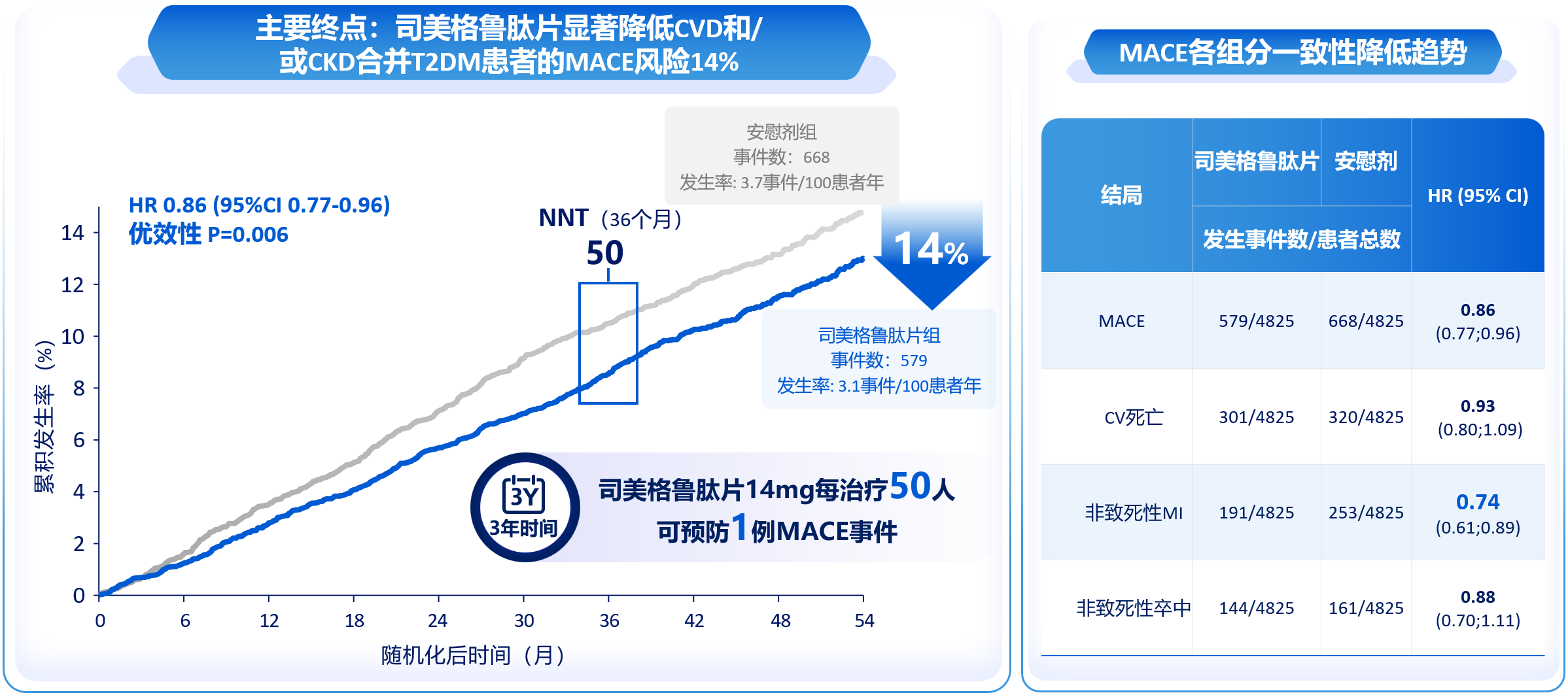
图5. SOUL研究:司美格鲁肽片显著降低MACE风险14%
相比之下,其他口服GLP-1RA目前均缺乏心血管结局的循证支持。积累心血管获益证据需要漫长的随访周期、庞大的样本量,并需克服试验设计与结果的不确定性。即便降糖、减重等指标表现亮眼,也不能直接推演为心血管获益。口服司美格鲁肽作为目前唯一拥有CVOT阳性结果的口服GLP-1RA,其在临床决策中的优先级,是基于高级别证据的必然选择。
五、结语
口服司美格鲁肽的临床价值,源于其从分子设计到临床验证构建的一条完整且坚实的证据链:高度同源的分子结构奠定了安全性基础,科学的剂量策略覆盖从血糖到体重的多元需求,大规模人群验证了长期良好的耐受性,而SOUL研究则为心血管获益提供了确证性证据。此外,多项PIONEER REAL真实世界研究[35-42]亦充分证实了其在真实临床环境中的疗效表现。
在糖尿病的长期管理中,理想的治疗选择应能陪伴患者行稳致远,安全抵达治疗终点。因此,临床决策应回归根本:一个药物能否在长期使用中,为患者带来安全、持久且经得起硬终点检验的临床获益?口服司美格鲁肽通过一系列设计严谨的临床研究,为这一问题提供了明确而有力的回答。
参考文献
1. Buckley ST, et al. Sci Transl Med. 2018; 10(467): eaar7047.
2. 吕晓希, 窦京涛. 中华糖尿病杂志. 2023; 15(5): 383-386.
3. Taing MW, et al. Drug Des Devel Ther. 2014; 8: 677-688.
4. Siraj MA, et al. J Clin Invest. 2020; 130(3): 1392-1404.
5. Zhou B, et al. Open Biochem J. 2014; 8: 107-111.
6. Tomas E, et al. Regul Pept. 2011; 167(2-3): 177-184.
7. Tomas E, et al. Regul Pept. 2011; 169(1-3): 43-48.
8. Kim JC, et al. Pharmaceuticals (Basel). 2022; 15(12): 1585.
9. Granhall C, et al. Clin Pharmacokinet. 2019; 58(6): 781-791.
10. Davies M, et al. JAMA. 2017; 318(15): 1460-1470.
11. Aroda VR, et al. Diabetes Care. 2019; 42(9): 1724-1732. PIONEER 1
12. Rodbard HW, et al. Diabetes Care. 2019; 42(12): 2272-2281. PIONEER 2
13. Rosenstock J, et al. JAMA. 2019; 321(15): 1466-1480. PIONEER 3
14. Pratley R, et al. Lancet. 2019; 394(10192): 39-50. PIONEER 4
15. Mosenzon O, et al. Lancet Diabetes Endocrinol. 2019; 7(7): 515-527. PIONEER 5
16. Husain M, et al. N Engl J Med. 2019; 381(9): 841-851. PIONEER 6
17. Pieber TR, et al. Lancet Diabetes Endocrinol. 2019; 7(7): 528-539. PIONEER 7
18. Zinman B, et al. Diabetes Care. 2019; 42(12): 2262-2271. PIONEER 8
19. Yamada Y, et al. Lancet Diabetes Endocrinol. 2020; 8(5): 377-391. PIONEER 9
20. Yabe D, et al. Lancet Diabetes Endocrinol. 2020; 8(5): 392-406. PIONEER 10
21. Wang W, et al. Diabetologia. 2024 Sep; 67(9): 1783-1799. PIONEER 11
22. Ji L, et al. Diabetologia. 2024 Sep; 67(9): 1800-1816. PIONEER 12
23. Aroda VR, et al. Lancet. 2023; 402(10403): 693-704.
24. Wharton S, et al. N Engl J Med. 2025; 393(11): 1077-1087.
25.https://www.novonordisk.com/content/nncorp/global/en/news-and-media/news-and-ir-materials/news-details.html?id=916472#
26. Rosenstock J, et al. Lancet. 2026 Feb 26: S0140-6736(26)00202-3.
27. Wharton S, et al. N Engl J Med. 2025; 393(18): 1796-1806.
28. Aroda V R, et al. Diabetes Obes Metab. 2023; 25(5): 1385-1397.
29. 王卫庆, 等. 中华内分泌代谢杂志. 2024; 40(11): 932-940.
30. 纪立农, 等. 中华内分泌代谢杂志. 2024; 40(10): 835-843.
31. Nauck MA, et al Lancet. 2026 Feb 26: S0140-6736(26)00360-0.
32. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
33. American Diabetes Association. Diabetes Care. 2026; 49 (Suppl_1): S183-S215.
34. McGuire DK, et al. N Engl J Med. 2025; 392(20): 2001-2012.
35. Jain AB, et al. Diabetes Obes Metab. 2024; 26(5): 1799-1807. PIONEER REAL Canada
36. Anastas Kick, et al. Diabetes Ther. 2024 Mar;15(3):623-637. PIONEER REAL Switzerland
37. van Houtum W, et al. Diabetes Ther. 2024; 15(8): 1749-1768. PIONEER REAL Netherlands
38. Catrina SB, et al. Diabetes Ther. Diabetes Ther. 2024; 15(9): 2079-2095. PIONEER REAL Sweden
39. Suzuki R, et al. J Diabetes Investig. 2024; 15(8): 1047-1056. PIONEER REAL Japan
40. Saravanan P, et al. Adv Ther. 2024; 41(11): 4266-4281. PIONEER REAL UK
41. Manti R, et al. Diabetes Ther. 2025; 16(5): 1019-1032. PIONEER REAL Italy
42. Delgado Álvarez E, et al. Diabetes Obes Metab. 2025; 27(9): 4812-4824. PIONEER REAL Spain 2 comments
胰高糖素样肽-1受体激动剂(GLP-1RA)已成为2型糖尿病(T2DM)综合管理的重要治疗选择,口服制剂的问世更是拓宽了其临床应用边界。作为全球首个且目前唯一获批上市的口服GLP-1RA,司美格鲁肽片填补了该领域的治疗空白,备受临床关注。近期公布的ACHIEVE-3研究数据,再次引发关于口服GLP-1RA的热议。然而,透过数据表象进行深入剖析,探讨药物的长期价值,仍是临床决策的关键所在。本文旨在系统解析口服司美格鲁肽如何凭借其经临床验证的分子设计、科学的剂量策略、良好的安全耐受性,以及目前唯一拥有心血管硬终点获益证据的地位,在口服GLP-1RA中彰显其独特的临床价值。
一、分子基础:94%高同源性赋予的不仅是靶向性,更是长期用药的安全性底气
口服司美格鲁肽的主要活性成分为司美格鲁肽分子,其本身未经额外结构修饰,而是通过与渗透促进剂N-(8-[2-羟基苯甲酰基]-氨基)辛酸钠(SNAC)共同制备,突破胃肠道粘膜屏障以实现吸收(图1)[1]。该药的核心竞争力源于其高度优化的分子结构——司美格鲁肽分子在天然GLP-1基础上仅进行两处氨基酸替换并连接脂肪酸侧链,与天然GLP-1同源性高达94%[2]。

图1. 司美格鲁肽片:司美格鲁肽分子与SNAC的强强联合
这一高度保守的氨基酸序列结构不仅确保了其对GLP-1受体的高亲和力,也决定了其体内代谢产物的结构与功能。高同源性的GLP-1RA可被二肽基肽酶Ⅳ及中性内肽酶代谢,形成与内源性GLP-1接近的代谢片段[2]。研究表明,GLP-1的某些代谢产物如GLP-1(28-36)片段仍具有保护胰岛β细胞、改善糖脂代谢、调节肝脏功能、控制体重及心血管保护等多重生物学效应[3-7]。
由此引出一个值得深思的问题:当追求更强效的受体激动时,是否应更全面考量分子代谢路径的生物学意义?对于与天然结构差异显著的新型分子,其代谢产物的生物学活性、长期蓄积的潜在影响,尚待明晰。司美格鲁肽所遵循的“高同源性”设计,体现的是对人体复杂生理环境的敬畏。对于需要坚持不懈长期管理的慢病,基于审慎选择带来的安全性和耐受性是保障患者长期获益的基础。
二、剂量策略:注重疗效与耐受性的平衡,个体化选择剂量
口服司美格鲁肽借助SNAC实现胃内跨细胞吸收(图2)[8]。其T2DM剂量策略的制定基于严谨的临床药理学依据:300 mg SNAC剂量可支持司美格鲁肽达到最大血药浓度,而3 mg qd起始、每月递增至7 mg qd或14 mg qd维持剂量的滴定方案,则是在确保疗效与胃肠道耐受性之间取得的最佳平衡[9,10]。

图2. SNAC促进司美格鲁肽吸收作用机制
在T2DM人群中,PIONEER系列研究证实司美格鲁肽片7 mg和14 mg带来明确临床获益:HbA1c最大降幅达1.6%,达标率(HbA1c<7%)最高达92.3%;同时,体重最多下降5.0 kg、收缩压最大降幅达7 mmHg,并显著改善血脂谱(图3)[11-22]。
口服司美格鲁肽更高剂量亦彰显出强大药理潜力:在PIONEER PLUS研究(T2DM患者)中,14 mg、25 mg、50 mg组的HbA1c降幅分别为1.5%、1.8%和2.0%,体重降幅分别为4.7%、7.3%和8.5%[23];而在OASIS 4研究(非糖尿病但伴有肥胖或超重及相关合并症人群)中,25 mg组平均体重下降16.6%,其中34%患者减重≥20%[24]。正是基于OASIS 4研究,司美格鲁肽片成为全球首个获批减重适应症的口服GLP-1RA[25]。

图3. PIONEER系列研究:司美格鲁肽片强效降糖、显著减重、降压调脂,安全性良好
综上,司美格鲁肽片形成了“降糖低剂量、减重高剂量”的科学分层策略,精准对接T2DM与肥胖的不同临床管理需求。需指出的是,ACHIEVE-3研究[26]中,orforglipron使用了与其减重研究ATTAIN 1[27]中相同的较高剂量(12 mg和36 mg),而对照药物司美格鲁肽片则仅使用了T2DM治疗剂量(7 mg和14 mg)。高剂量会取得相对更好的降糖减重效果,似乎并不令人意外。
三、耐受性与依从性:在疗效之外的真实世界临床价值考量
胃肠道不良反应是制约GLP-1RA持续治疗的主要瓶颈。口服司美格鲁肽在PIONEER系列研究(纳入全球超过9000例T2DM患者)中证实,其胃肠道事件多为轻中度、主要发生于剂量递增期、持续时间较短,绝大多数患者可耐受,且中国人群数据与全球一致[11-22,28-30](图4)。
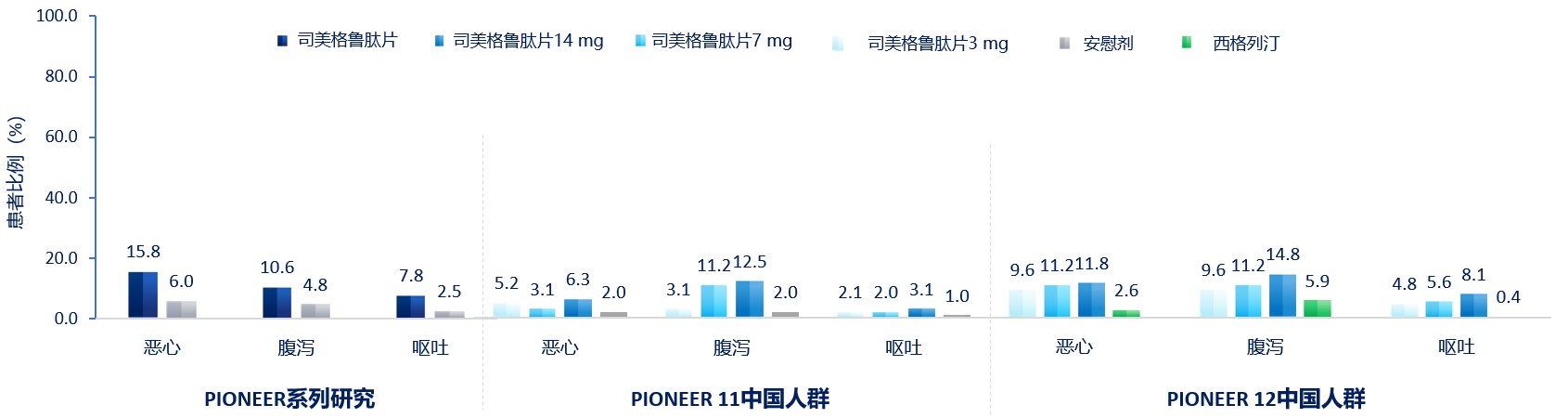
ACHIEVE-3研究[26]恰恰印证了司美格鲁肽片的耐受性优势。数据显示,orforglipron组的恶心发生率(12 mg组26%、36 mg组27%)显著高于司美格鲁肽组(7 mg组13%、14 mg组21%);呕吐发生率同样更高(orforglipron组17%和17% vs. 司美格鲁肽组8%和10%);腹泻和便秘也呈现类似关系[26,31]。而且,orforglipron组总体胃肠道不良事件发生率更高(12 mg组59%、36 mg组58%),且未见明显剂量依赖性[26,31]——这意味着即使采用低剂量起始,患者仍存在较高的胃肠道不良反应风险,通过剂量递增可能无法改善耐受性;而司美格鲁肽组的发生率更低(7 mg组37%、14 mg组45%),且呈剂量依赖性[26,31],提示其剂量递增策略能够帮助患者逐步适应,从而降低胃肠道不良反应风险。相应地,司美格鲁肽组因不良事件或胃肠道反应导致的停药率均更低[26](表1)。
表1. ACHIEVE-3研究中安全性人群的不良事件发生情况
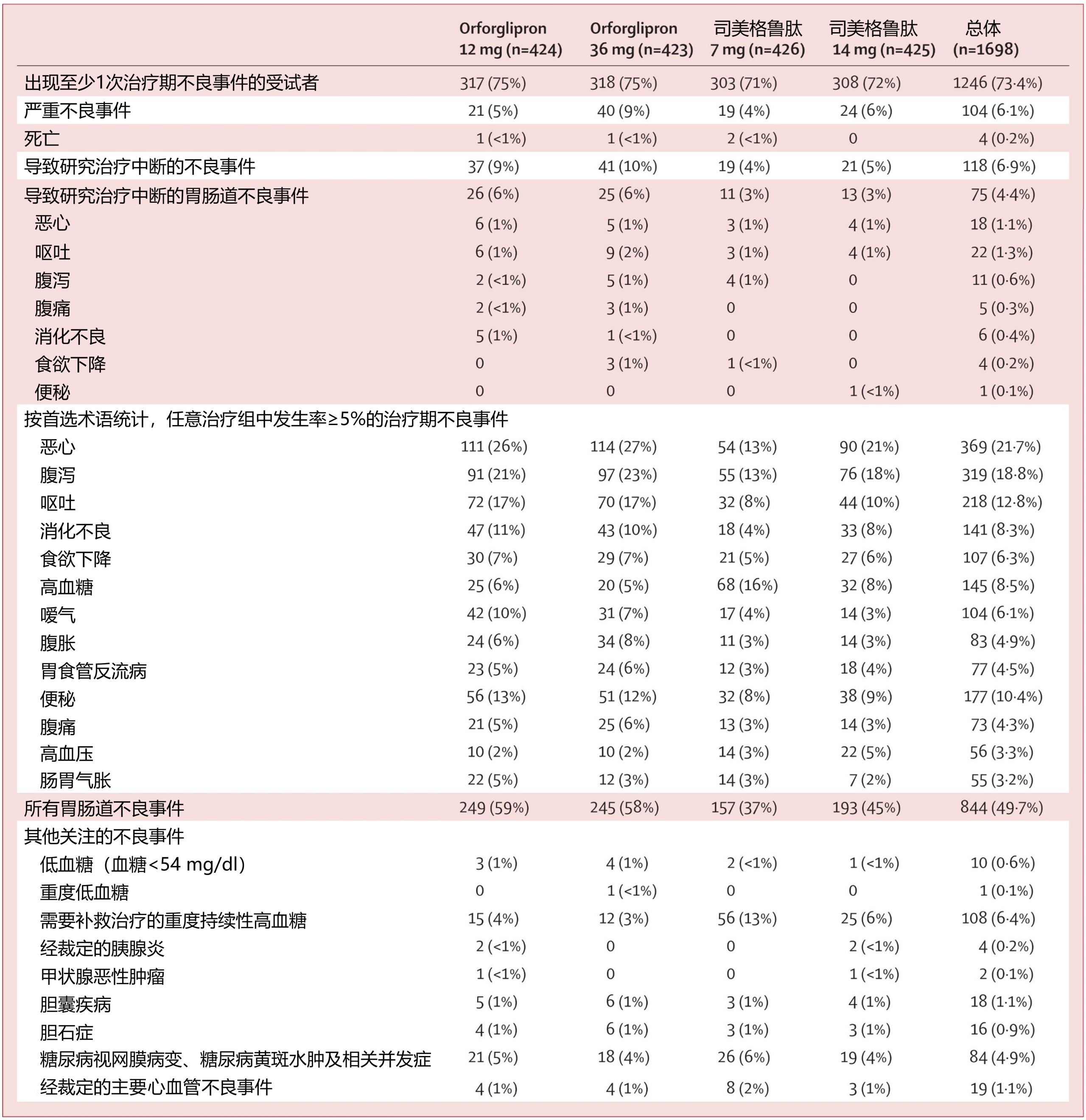
在真实世界临床实践中,较低的不良反应发生率和停药率是确保治疗长期有效的重要前提。对任何药物而言,若因耐受性问题导致患者终止治疗,即便在降糖或减重方面具有良好疗效,其临床价值也将大打折扣。口服司美格鲁肽在大规模人群中验证出的良好耐受性,是提升长期治疗依从性、优化患者治疗体验的可靠保障,也是其临床价值的重要组成。
四、心血管获益:以硬终点为依据的临床决策考量
现行国内外指南(如ADA指南、CDS指南)一致推荐,对于合并动脉粥样硬化性心血管疾病(ASCVD)或其高危因素的T2DM患者,优先使用具有确证心血管获益证据的药物,如GLP-1RA[32,33]。这已成为临床决策的一项重要标准。
口服司美格鲁肽凭借SOUL研究成为目前全球唯一拥有确证心血管获益证据的口服GLP-1RA[34]。这项纳入9650例合并ASCVD和/或慢性肾脏病的T2DM患者、中位随访49.5个月的CVOT证实,口服司美格鲁肽显著降低主要心血管不良事件(MACE)风险达14%,其中非致死性心肌梗死风险降低达26%(图5)。在占比高达23.4%的亚洲人群中,MACE降幅达27%[34]。

图5. SOUL研究:司美格鲁肽片显著降低MACE风险14%
相比之下,其他口服GLP-1RA目前均缺乏心血管结局的循证支持。积累心血管获益证据需要漫长的随访周期、庞大的样本量,并需克服试验设计与结果的不确定性。即便降糖、减重等指标表现亮眼,也不能直接推演为心血管获益。口服司美格鲁肽作为目前唯一拥有CVOT阳性结果的口服GLP-1RA,其在临床决策中的优先级,是基于高级别证据的必然选择。
五、结语
口服司美格鲁肽的临床价值,源于其从分子设计到临床验证构建的一条完整且坚实的证据链:高度同源的分子结构奠定了安全性基础,科学的剂量策略覆盖从血糖到体重的多元需求,大规模人群验证了长期良好的耐受性,而SOUL研究则为心血管获益提供了确证性证据。此外,多项PIONEER REAL真实世界研究[35-42]亦充分证实了其在真实临床环境中的疗效表现。
在糖尿病的长期管理中,理想的治疗选择应能陪伴患者行稳致远,安全抵达治疗终点。因此,临床决策应回归根本:一个药物能否在长期使用中,为患者带来安全、持久且经得起硬终点检验的临床获益?口服司美格鲁肽通过一系列设计严谨的临床研究,为这一问题提供了明确而有力的回答。
参考文献
1. Buckley ST, et al. Sci Transl Med. 2018; 10(467): eaar7047.
2. 吕晓希, 窦京涛. 中华糖尿病杂志. 2023; 15(5): 383-386.
3. Taing MW, et al. Drug Des Devel Ther. 2014; 8: 677-688.
4. Siraj MA, et al. J Clin Invest. 2020; 130(3): 1392-1404.
5. Zhou B, et al. Open Biochem J. 2014; 8: 107-111.
6. Tomas E, et al. Regul Pept. 2011; 167(2-3): 177-184.
7. Tomas E, et al. Regul Pept. 2011; 169(1-3): 43-48.
8. Kim JC, et al. Pharmaceuticals (Basel). 2022; 15(12): 1585.
9. Granhall C, et al. Clin Pharmacokinet. 2019; 58(6): 781-791.
10. Davies M, et al. JAMA. 2017; 318(15): 1460-1470.
11. Aroda VR, et al. Diabetes Care. 2019; 42(9): 1724-1732. PIONEER 1
12. Rodbard HW, et al. Diabetes Care. 2019; 42(12): 2272-2281. PIONEER 2
13. Rosenstock J, et al. JAMA. 2019; 321(15): 1466-1480. PIONEER 3
14. Pratley R, et al. Lancet. 2019; 394(10192): 39-50. PIONEER 4
15. Mosenzon O, et al. Lancet Diabetes Endocrinol. 2019; 7(7): 515-527. PIONEER 5
16. Husain M, et al. N Engl J Med. 2019; 381(9): 841-851. PIONEER 6
17. Pieber TR, et al. Lancet Diabetes Endocrinol. 2019; 7(7): 528-539. PIONEER 7
18. Zinman B, et al. Diabetes Care. 2019; 42(12): 2262-2271. PIONEER 8
19. Yamada Y, et al. Lancet Diabetes Endocrinol. 2020; 8(5): 377-391. PIONEER 9
20. Yabe D, et al. Lancet Diabetes Endocrinol. 2020; 8(5): 392-406. PIONEER 10
21. Wang W, et al. Diabetologia. 2024 Sep; 67(9): 1783-1799. PIONEER 11
22. Ji L, et al. Diabetologia. 2024 Sep; 67(9): 1800-1816. PIONEER 12
23. Aroda VR, et al. Lancet. 2023; 402(10403): 693-704.
24. Wharton S, et al. N Engl J Med. 2025; 393(11): 1077-1087.
25.https://www.novonordisk.com/content/nncorp/global/en/news-and-media/news-and-ir-materials/news-details.html?id=916472#
26. Rosenstock J, et al. Lancet. 2026 Feb 26: S0140-6736(26)00202-3.
27. Wharton S, et al. N Engl J Med. 2025; 393(18): 1796-1806.
28. Aroda V R, et al. Diabetes Obes Metab. 2023; 25(5): 1385-1397.
29. 王卫庆, 等. 中华内分泌代谢杂志. 2024; 40(11): 932-940.
30. 纪立农, 等. 中华内分泌代谢杂志. 2024; 40(10): 835-843.
31. Nauck MA, et al Lancet. 2026 Feb 26: S0140-6736(26)00360-0.
32. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(1): 16-139.
33. American Diabetes Association. Diabetes Care. 2026; 49 (Suppl_1): S183-S215.
34. McGuire DK, et al. N Engl J Med. 2025; 392(20): 2001-2012.
35. Jain AB, et al. Diabetes Obes Metab. 2024; 26(5): 1799-1807. PIONEER REAL Canada
36. Anastas Kick, et al. Diabetes Ther. 2024 Mar;15(3):623-637. PIONEER REAL Switzerland
37. van Houtum W, et al. Diabetes Ther. 2024; 15(8): 1749-1768. PIONEER REAL Netherlands
38. Catrina SB, et al. Diabetes Ther. Diabetes Ther. 2024; 15(9): 2079-2095. PIONEER REAL Sweden
39. Suzuki R, et al. J Diabetes Investig. 2024; 15(8): 1047-1056. PIONEER REAL Japan
40. Saravanan P, et al. Adv Ther. 2024; 41(11): 4266-4281. PIONEER REAL UK
41. Manti R, et al. Diabetes Ther. 2025; 16(5): 1019-1032. PIONEER REAL Italy
42. Delgado Álvarez E, et al. Diabetes Obes Metab. 2025; 27(9): 4812-4824. PIONEER REAL Spain 2 comments









 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言