编者按:
胰岛β细胞功能评估是糖尿病管理的关键核心环节。传统单维度评估方法难以全面、精准地反映β细胞的复杂功能状态。近日,南京医科大学第一附属医院(江苏省人民医院)杨涛教授团队在The Journal of Clinical Endocrinology & Metabolism(JCEM)发表的研究成果首次提出——多维胰岛β细胞功能(PIF)评估,涵盖平稳基线、负荷峰值和加速斜率3个维度,能够对β细胞功能全面量化,为糖尿病风险预测与个性化管理提供了全新工具[1]。
β细胞功能评估的现状与挑战
胰岛β细胞功能障碍是糖尿病发病的核心机制。1型糖尿病(T1DM)由β细胞自身免疫破坏导致,而2型糖尿病(T2DM)则常与胰岛素抵抗相关的相对性β细胞功能不全有关[2,3]。准确评估β细胞功能对于糖尿病的分类、进展监测和治疗规划至关重要[4]。目前评估β细胞功能的方法多样,高血糖钳夹技术虽被视为“金标准”,但其复杂性限制了临床应用[5]。相较而言,口服葡萄糖耐量试验(OGTT)和混合餐耐量试验在临床中更为常用。
尽管已提出针对胰岛素第一、第二时相分泌的指标,但这些指标多存在单维度局限性,仍未能充分反映代谢疾病中激素峰值快速性及分泌阶段变化特征,同时受限于数据源于特定人群且以绝对值呈现,主要应用于研究及流行病学领域,临床应用价值受限[6]。
研究目的:
构建多维β细胞功能评估方法
研究提出了一种多维、相对量化的β细胞功能评估方法,通过分析负荷试验中胰岛素和C肽分泌曲线特征,从三个维度进行评估:
平稳基线(PIF-S):空腹状态下胰岛素或C肽与血糖的比值。
负荷峰值(PIF-L):OGTT中达到的最高胰岛素或C肽水平与对应血糖的比值。
加速斜率(PIF-A):从基线到峰值的变化率,反映β细胞对葡萄糖刺激的反应速度。
研究方法:
严谨的多队列验证
研究在多个独立队列中验证了多维PIF评估方法的有效性:
江苏句容(JR)队列:814名志愿者(195名代谢健康者,619名代谢异常者),完成5时OGTT(空腹、30分钟、60分钟、120分钟、180分钟)。
Botnia钳夹试验队列:从江苏南京招募12名健康志愿者,间隔1周后再次进行5时OGTT,用于验证PIF指标的生理意义。
2型糖尿病(T2DM)队列:纳入2015年至2023年间在南京医科大学第一附属医院内分泌科住院的3394例住院T2DM患者,进行5时OGTT,评估PIF与并发症的关系。
METSIM队列:纳入2005~2010年间的10 197例45~74岁的芬兰男性,进行3时OGTT(空腹、30分钟、120分钟),验证PIF对糖尿病发生风险的预测价值。
通过限制性立方样条(RCS)模型,基于代谢健康个体的数据建立了考虑性别、年龄和身高影响的理想值预测模型。
研究结果:
多维评估揭示β细胞功能异质性
纳入13项β细胞功能指标
基于先前研究,研究团队筛选出13项用于评估胰岛β细胞功能的指标,具体包括:稳态模型评估的β细胞功能(HOMA-β)、估计的第一时相胰岛素释放(PHest_1st)、估计的第二时相胰岛素释放(PHest_2nd)、空腹血C肽指数(FBCI)、胰岛素生成指数(IGI)、改良β细胞功能指数(MBCI)、胰岛素曲线下面积30分钟/葡萄糖曲线下面积30分钟(InsAUC30/GluAUC30)、早期胰岛素释放(INSR30)、胰岛素曲线下面积120分钟/葡萄糖曲线下面积120分钟(InsAUC120/GluAUC120)、总胰岛素释放(INSR120)、BIGTT急性胰岛素反应(BIGTT_AIR)、校正胰岛素反应(CIR)、空腹C肽与胰岛素比值(FCPR)、葡萄糖负荷后C肽与胰岛素比值(PCPR),以及胰岛素增量曲线下面积/血糖增量曲线下面积(iAUCins/g)。这些指标综合反映了胰岛β细胞在不同阶段的胰岛素分泌能力、葡萄糖刺激后的动态反应特征,以及C肽与胰岛素的代谢关联性。
传统β细胞功能指标的局限性
对13项传统β细胞功能指标的主成分分析(PCA)显示,这些指标可分为空腹指标和负荷试验指标两大类(图1)。前三个主成分仅解释73%的方差,表明单一指标无法全面反映β细胞功能的复杂性。
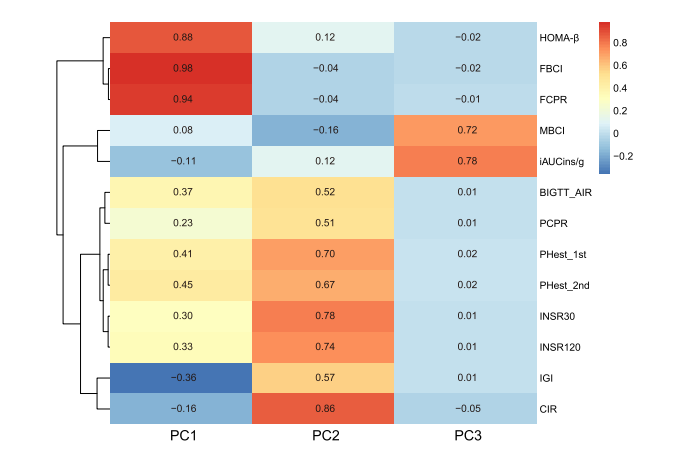
图1. 13项传统β细胞功能指标的聚类分析
性别、年龄和身高对β细胞功能的影响
在JR队列中,研究发现性别、年龄和身高对β细胞功能指标有显著影响(图2):男性在0和30分钟血糖水平较高,120和180分钟胰岛素和C肽水平较低;≥50岁组在多个时间点血糖较高,<30岁组胰岛素和C肽水平较高;身高对血糖和胰岛素水平无显著影响,但矮身材组在180分钟C肽水平显著降低。
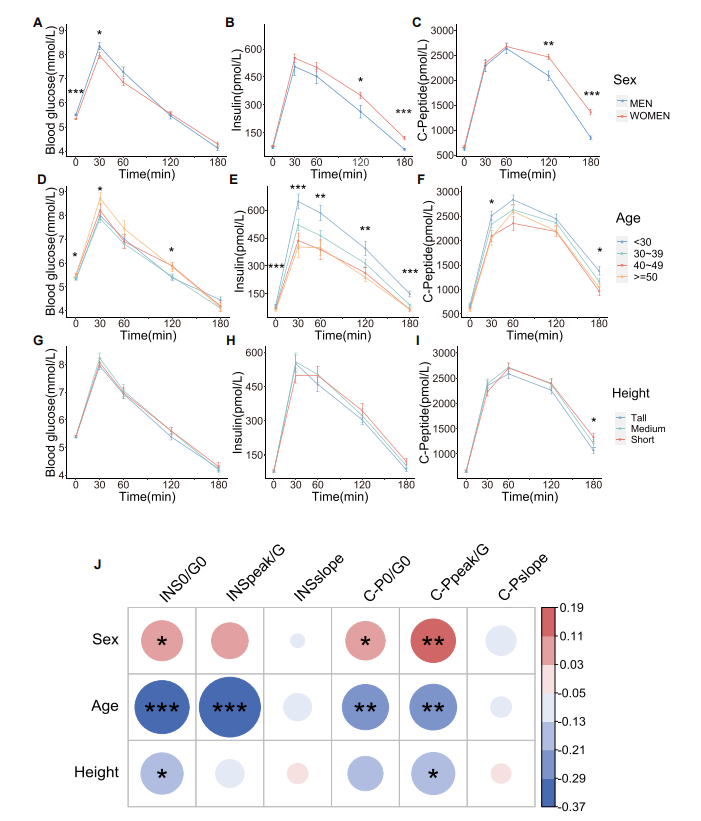
图2. 性别、年龄和身高对胰岛素和C肽分泌曲线的影响
图A-I展示了不同性别、年龄、身高分组下血糖、胰岛素和C肽随时间变化的曲线。图J的相关性矩阵明确指出,加速斜率指标(INSslope, C-Pslope)是评估β细胞功能的独立维度。
在考虑年龄、性别和身高的影响下,研究者采用RCS方法为代谢健康个体建立了以下指标的回归模型(图3):空腹胰岛素/葡萄糖比值(INS0/G0)、胰岛素峰值/葡萄糖比值(INSpeak/G)、空腹C肽/葡萄糖比值(C-P0/G0)及C肽峰值/葡萄糖比值(C-Ppeak/G),并计算了特定性别、年龄和身高对应的理想值。同时,口服葡萄糖耐量试验(OGTT)中的胰岛素分泌斜率(INSslope)和C肽分泌斜率(C-Pslope)的理想值直接取自代谢健康个体的中位数水平:INSslope为0.17(0.11-0.25),C-Pslope为0.076(0.048-0.108)。
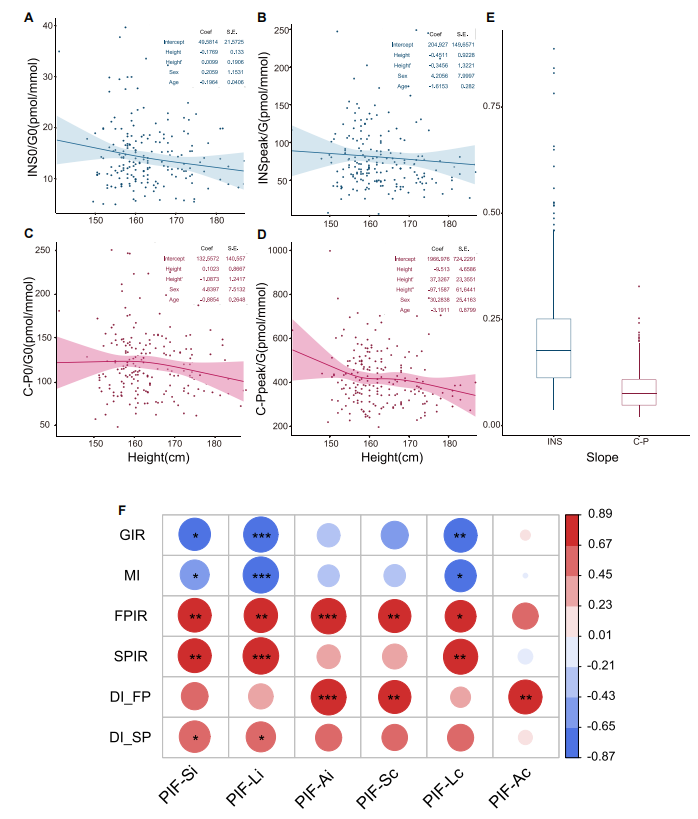
图3. 基于性别、年龄和身高建立的3维PIF参数理想值回归模型
多维PIF指标与金标准的相关性
Botnia钳夹试验验证显示:PIF-S(平稳基线指数)与第一和第二时相胰岛素分泌(FPIR、SPIR)显著正相关,但受胰岛素敏感性影响;PIF-L(负荷峰值指数)与FPIR和SPIR显著相关,同样受胰岛素敏感性影响;PIF-A(加速斜率指数)与FPIR显著相关,且完全独立于胰岛素敏感性,与处置指数(DI)保持显著相关性(图4)。
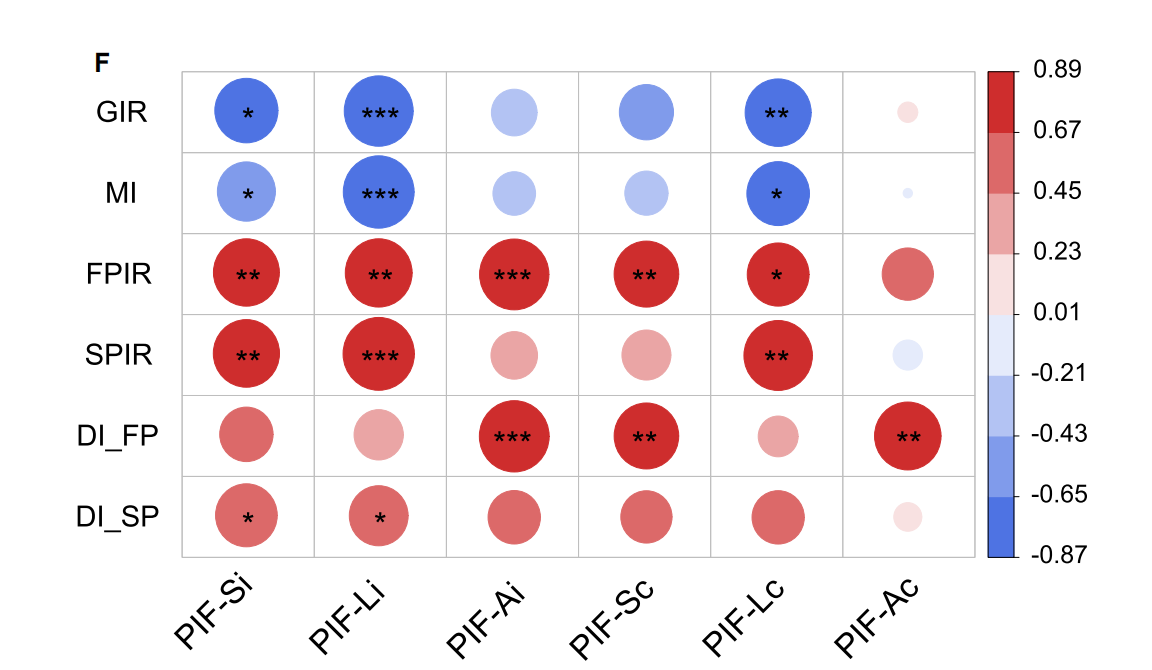
图4. 3维PIF参数与Botnia钳夹试验的相关性
多维PIF指标在代谢异常人群的应用
对JR队列中619例代谢异常个体的聚类分析识别出三个具有独特PIF特征的群体(图5)。
Cluster 3:PIF-S和PIF-L最高,但PIF-A显著降低,表现为基础β细胞分泌高但对葡萄糖刺激反应迟钝,代谢特征最差,疾病风险最高。
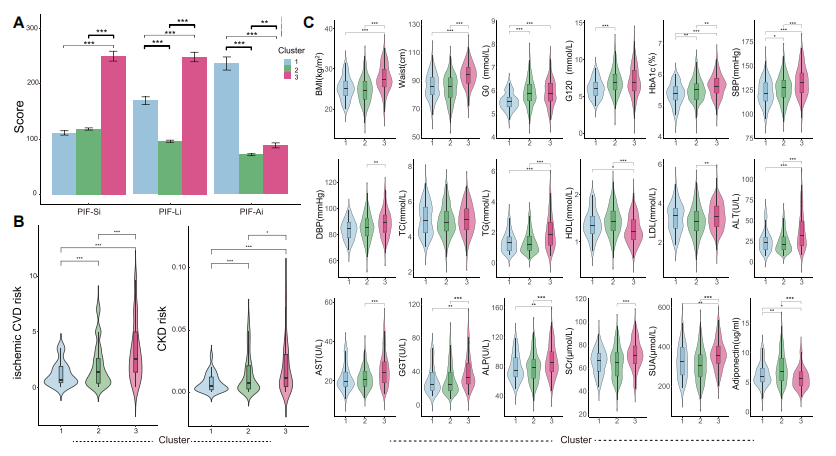
图5. 多维PIF指数在619名代谢异常人群中的应用
多维PIF指标在T2DM人群中的应用
根据多维PIF指标及糖尿病病程,将3394例T2DM患者分为3个群组。各组PIF特征与JR队列中619名代谢异常个体的聚类特征相似。回归分析显示,在调整病程因素后,Cluster 1患者的冠状动脉疾病(CAD,6.25%)、缺血性卒中(IS,5.44%)、慢性肾脏病(CKD,1.71%)及糖尿病肾病(DKD,18.02%)发病率均最低。尽管Cluster 3的平均病程(4.00±0.23年)与Cluster 1(3.00±0.09年)相近,但其CAD、IS和DKD患病率显著更高,且与病程更长的Cluster 2(16.00±0.15年)相当。此外,Cluster 3的CKD患病率在三组中最高(10.18%)。
简版多维PIF指标在METSIM随访队列中的应用
在METSIM随访队列中,研究者计算了简版3时PIF指标,并将人群分为3组。与前期聚类结果一致:Cluster 1,对葡萄糖负荷呈现快速β细胞反应;Cluster 2,对葡萄糖刺激表现出相对平缓的β细胞反应;Cluster 3,基础β细胞分泌水平高,但对葡萄糖刺激的反应显著减弱。
在4537例获得有效随访数据的受试者中,经年龄、体重指数(BMI)、糖化血红蛋白(HbA1c)、吸烟、咖啡摄入量及糖尿病家族史等多因素校正后,Cox回归分析显示:Cluster 1人群的糖尿病发病风险最低。与Cluster 1相比,Cluster 2和Cluster 3的糖尿病风险比(HR)分别为2.499(95%CI:1.932-3.233,P=3.11×10-12)和3.185(95%CI:2.353-4.311,P=6.35×10-12)(图6)。进一步分析显示,Cluster 3的高血压和冠心病发病风险最高(P=0.0015和0.0034),而Cluster 1与Cluster 2之间无显著差异。
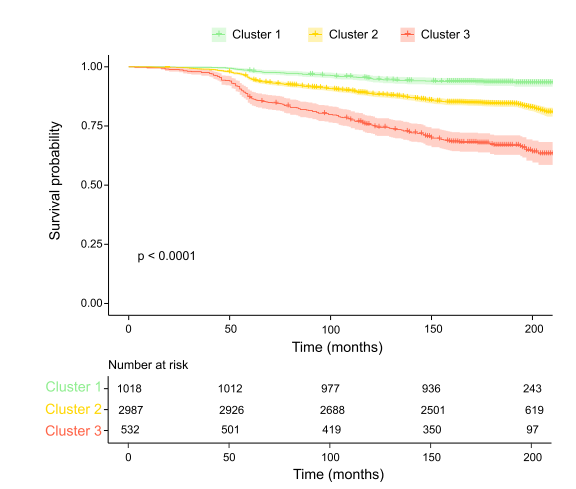
图6. METSIM队列中不同PIF指数的糖尿病发生风险
多维PIF指标的预测效能
ROC曲线分析显示,多维PIF指数组合预测新发糖尿病的效能(AUC=0.71)显著优于传统指标如HOMA-B(AUC=0.63)、CIR(AUC=0.55)和INSR120(AUC=0.60)。相比现有糖尿病风险评分(DRS)模型——Danish DRS、Dutch DRS、ARIC DRS,AUC分别从0.695提高到0.742、从0.706提高到0.747、从0.775提高到0.789(图7)。
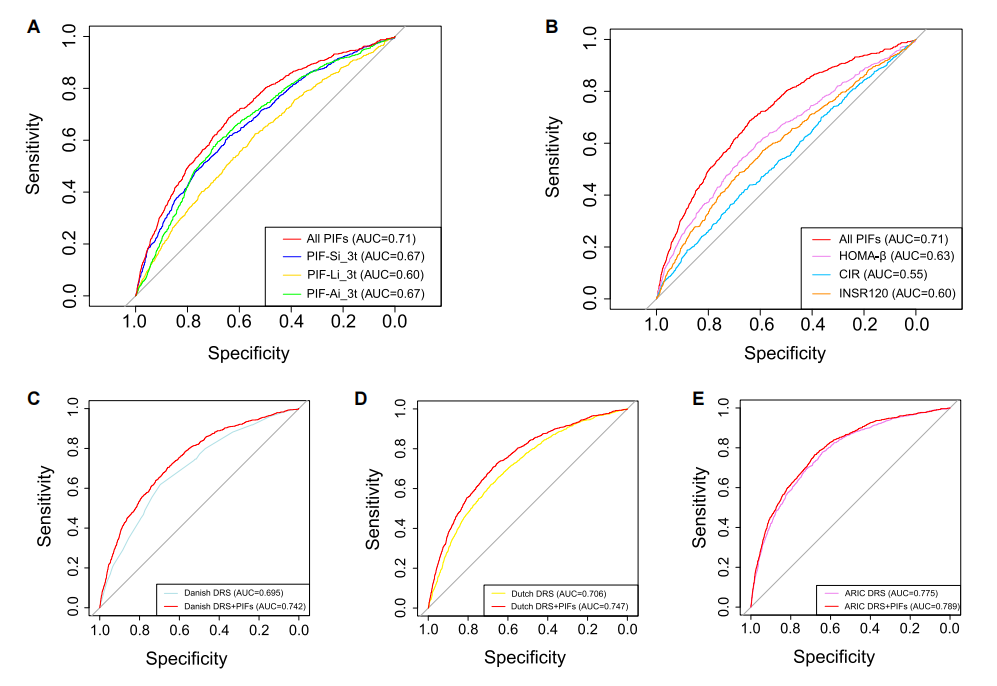
图7. 多维PIF指数组合与其他指标预测糖尿病的效能比较
研究讨论:
多维评估的科学价值与临床启示
本研究突破传统单维度β细胞功能评估局限,首创三维评估体系(PIF-S/L/A),从静息基线、负荷峰值、加速斜率三个维度动态捕捉β细胞功能全貌。该方法解决了胰岛素/C肽分泌曲线在病理状态下的不规则性难题,通过整合静息-应激-调节三阶段特征,为复杂β细胞功能评估提供了全新视角。
研究揭示PIF特征与代谢风险的深层关联:高PIF-A(加速斜率)是代谢健康的标志,反映β细胞快速反应能力;而高PIF-S(基线)和PIF-L(峰值)若伴随低PIF-A,则预示“高输出、低效率”的衰竭模式,代表β细胞在长期胰岛素抵抗压力下已处于功能衰竭边缘,对应最高疾病风险。这种模式独立于传统风险因素(如年龄、BMI),为识别糖尿病并发症高危人群提供了关键生物标志物。
在临床应用层面,PIF体系通过3时OGTT(0/30/120分钟)即可实现与5时OGTT相当的评估效果,显著提升检测便捷性。结合代谢健康人群数据建立的标准化评分模型,将实际检测值转化为具有临床意义的百分位数评分,可精准指导个性化治疗(如对“高负荷-低效型”患者早期干预)。跨人群验证(中国与芬兰)证实该评估方法具有良好的普适性,整合入现有糖尿病风险评分模型后,可显著提升预测效能,为全球不同人群β细胞功能精准评估提供了科学可靠的标准化工具。
结论与展望
多维PIF评估系统通过三个维度捕捉β细胞功能,为糖尿病预测和管理提供新工具。研究表明,PIF-A是评估代谢健康和疾病风险的关键指标。结合多维PIF指数与现有评分,可提高预测效能,支持精准医疗。未来研究将验证系统、探索PIF与并发症的关系,并开发个性化治疗策略。
参考文献
[1] The Journal of Clinical Endocrinology & Metabolism, 2026, 111, 541-552
[2] Lancet. 2023;401(10394):2149-2162.
[3] Lancet Diabetes Endocrinol. 2020;8(3):249-256.
[4] Mol Metab. 2021;46:101158.
[5] Diabetes Care. 2003;26(5):1395-1401.
[6] Diabetes Care. 2013;36(5):1229-1235. 2 comments
胰岛β细胞功能评估是糖尿病管理的关键核心环节。传统单维度评估方法难以全面、精准地反映β细胞的复杂功能状态。近日,南京医科大学第一附属医院(江苏省人民医院)杨涛教授团队在The Journal of Clinical Endocrinology & Metabolism(JCEM)发表的研究成果首次提出——多维胰岛β细胞功能(PIF)评估,涵盖平稳基线、负荷峰值和加速斜率3个维度,能够对β细胞功能全面量化,为糖尿病风险预测与个性化管理提供了全新工具[1]。

β细胞功能评估的现状与挑战
胰岛β细胞功能障碍是糖尿病发病的核心机制。1型糖尿病(T1DM)由β细胞自身免疫破坏导致,而2型糖尿病(T2DM)则常与胰岛素抵抗相关的相对性β细胞功能不全有关[2,3]。准确评估β细胞功能对于糖尿病的分类、进展监测和治疗规划至关重要[4]。目前评估β细胞功能的方法多样,高血糖钳夹技术虽被视为“金标准”,但其复杂性限制了临床应用[5]。相较而言,口服葡萄糖耐量试验(OGTT)和混合餐耐量试验在临床中更为常用。
尽管已提出针对胰岛素第一、第二时相分泌的指标,但这些指标多存在单维度局限性,仍未能充分反映代谢疾病中激素峰值快速性及分泌阶段变化特征,同时受限于数据源于特定人群且以绝对值呈现,主要应用于研究及流行病学领域,临床应用价值受限[6]。
研究目的:
构建多维β细胞功能评估方法
研究提出了一种多维、相对量化的β细胞功能评估方法,通过分析负荷试验中胰岛素和C肽分泌曲线特征,从三个维度进行评估:
平稳基线(PIF-S):空腹状态下胰岛素或C肽与血糖的比值。
负荷峰值(PIF-L):OGTT中达到的最高胰岛素或C肽水平与对应血糖的比值。
加速斜率(PIF-A):从基线到峰值的变化率,反映β细胞对葡萄糖刺激的反应速度。
研究方法:
严谨的多队列验证
研究在多个独立队列中验证了多维PIF评估方法的有效性:
江苏句容(JR)队列:814名志愿者(195名代谢健康者,619名代谢异常者),完成5时OGTT(空腹、30分钟、60分钟、120分钟、180分钟)。
Botnia钳夹试验队列:从江苏南京招募12名健康志愿者,间隔1周后再次进行5时OGTT,用于验证PIF指标的生理意义。
2型糖尿病(T2DM)队列:纳入2015年至2023年间在南京医科大学第一附属医院内分泌科住院的3394例住院T2DM患者,进行5时OGTT,评估PIF与并发症的关系。
METSIM队列:纳入2005~2010年间的10 197例45~74岁的芬兰男性,进行3时OGTT(空腹、30分钟、120分钟),验证PIF对糖尿病发生风险的预测价值。
通过限制性立方样条(RCS)模型,基于代谢健康个体的数据建立了考虑性别、年龄和身高影响的理想值预测模型。
研究结果:
多维评估揭示β细胞功能异质性
纳入13项β细胞功能指标
基于先前研究,研究团队筛选出13项用于评估胰岛β细胞功能的指标,具体包括:稳态模型评估的β细胞功能(HOMA-β)、估计的第一时相胰岛素释放(PHest_1st)、估计的第二时相胰岛素释放(PHest_2nd)、空腹血C肽指数(FBCI)、胰岛素生成指数(IGI)、改良β细胞功能指数(MBCI)、胰岛素曲线下面积30分钟/葡萄糖曲线下面积30分钟(InsAUC30/GluAUC30)、早期胰岛素释放(INSR30)、胰岛素曲线下面积120分钟/葡萄糖曲线下面积120分钟(InsAUC120/GluAUC120)、总胰岛素释放(INSR120)、BIGTT急性胰岛素反应(BIGTT_AIR)、校正胰岛素反应(CIR)、空腹C肽与胰岛素比值(FCPR)、葡萄糖负荷后C肽与胰岛素比值(PCPR),以及胰岛素增量曲线下面积/血糖增量曲线下面积(iAUCins/g)。这些指标综合反映了胰岛β细胞在不同阶段的胰岛素分泌能力、葡萄糖刺激后的动态反应特征,以及C肽与胰岛素的代谢关联性。
传统β细胞功能指标的局限性
对13项传统β细胞功能指标的主成分分析(PCA)显示,这些指标可分为空腹指标和负荷试验指标两大类(图1)。前三个主成分仅解释73%的方差,表明单一指标无法全面反映β细胞功能的复杂性。

图1. 13项传统β细胞功能指标的聚类分析
性别、年龄和身高对β细胞功能的影响
在JR队列中,研究发现性别、年龄和身高对β细胞功能指标有显著影响(图2):男性在0和30分钟血糖水平较高,120和180分钟胰岛素和C肽水平较低;≥50岁组在多个时间点血糖较高,<30岁组胰岛素和C肽水平较高;身高对血糖和胰岛素水平无显著影响,但矮身材组在180分钟C肽水平显著降低。

图2. 性别、年龄和身高对胰岛素和C肽分泌曲线的影响
图A-I展示了不同性别、年龄、身高分组下血糖、胰岛素和C肽随时间变化的曲线。图J的相关性矩阵明确指出,加速斜率指标(INSslope, C-Pslope)是评估β细胞功能的独立维度。
在考虑年龄、性别和身高的影响下,研究者采用RCS方法为代谢健康个体建立了以下指标的回归模型(图3):空腹胰岛素/葡萄糖比值(INS0/G0)、胰岛素峰值/葡萄糖比值(INSpeak/G)、空腹C肽/葡萄糖比值(C-P0/G0)及C肽峰值/葡萄糖比值(C-Ppeak/G),并计算了特定性别、年龄和身高对应的理想值。同时,口服葡萄糖耐量试验(OGTT)中的胰岛素分泌斜率(INSslope)和C肽分泌斜率(C-Pslope)的理想值直接取自代谢健康个体的中位数水平:INSslope为0.17(0.11-0.25),C-Pslope为0.076(0.048-0.108)。

图3. 基于性别、年龄和身高建立的3维PIF参数理想值回归模型
多维PIF指标与金标准的相关性
Botnia钳夹试验验证显示:PIF-S(平稳基线指数)与第一和第二时相胰岛素分泌(FPIR、SPIR)显著正相关,但受胰岛素敏感性影响;PIF-L(负荷峰值指数)与FPIR和SPIR显著相关,同样受胰岛素敏感性影响;PIF-A(加速斜率指数)与FPIR显著相关,且完全独立于胰岛素敏感性,与处置指数(DI)保持显著相关性(图4)。

图4. 3维PIF参数与Botnia钳夹试验的相关性
多维PIF指标在代谢异常人群的应用
对JR队列中619例代谢异常个体的聚类分析识别出三个具有独特PIF特征的群体(图5)。
Cluster 1:PIF-A最高,PIF-S最低,表现为β细胞对葡萄糖负荷的快速反应能力强,代谢特征最佳,缺血性心血管疾病和慢性肾病风险最低。
Cluster 3:PIF-S和PIF-L最高,但PIF-A显著降低,表现为基础β细胞分泌高但对葡萄糖刺激反应迟钝,代谢特征最差,疾病风险最高。

图5. 多维PIF指数在619名代谢异常人群中的应用
多维PIF指标在T2DM人群中的应用
根据多维PIF指标及糖尿病病程,将3394例T2DM患者分为3个群组。各组PIF特征与JR队列中619名代谢异常个体的聚类特征相似。回归分析显示,在调整病程因素后,Cluster 1患者的冠状动脉疾病(CAD,6.25%)、缺血性卒中(IS,5.44%)、慢性肾脏病(CKD,1.71%)及糖尿病肾病(DKD,18.02%)发病率均最低。尽管Cluster 3的平均病程(4.00±0.23年)与Cluster 1(3.00±0.09年)相近,但其CAD、IS和DKD患病率显著更高,且与病程更长的Cluster 2(16.00±0.15年)相当。此外,Cluster 3的CKD患病率在三组中最高(10.18%)。
简版多维PIF指标在METSIM随访队列中的应用
在METSIM随访队列中,研究者计算了简版3时PIF指标,并将人群分为3组。与前期聚类结果一致:Cluster 1,对葡萄糖负荷呈现快速β细胞反应;Cluster 2,对葡萄糖刺激表现出相对平缓的β细胞反应;Cluster 3,基础β细胞分泌水平高,但对葡萄糖刺激的反应显著减弱。
在4537例获得有效随访数据的受试者中,经年龄、体重指数(BMI)、糖化血红蛋白(HbA1c)、吸烟、咖啡摄入量及糖尿病家族史等多因素校正后,Cox回归分析显示:Cluster 1人群的糖尿病发病风险最低。与Cluster 1相比,Cluster 2和Cluster 3的糖尿病风险比(HR)分别为2.499(95%CI:1.932-3.233,P=3.11×10-12)和3.185(95%CI:2.353-4.311,P=6.35×10-12)(图6)。进一步分析显示,Cluster 3的高血压和冠心病发病风险最高(P=0.0015和0.0034),而Cluster 1与Cluster 2之间无显著差异。

图6. METSIM队列中不同PIF指数的糖尿病发生风险
多维PIF指标的预测效能
ROC曲线分析显示,多维PIF指数组合预测新发糖尿病的效能(AUC=0.71)显著优于传统指标如HOMA-B(AUC=0.63)、CIR(AUC=0.55)和INSR120(AUC=0.60)。相比现有糖尿病风险评分(DRS)模型——Danish DRS、Dutch DRS、ARIC DRS,AUC分别从0.695提高到0.742、从0.706提高到0.747、从0.775提高到0.789(图7)。

图7. 多维PIF指数组合与其他指标预测糖尿病的效能比较
研究讨论:
多维评估的科学价值与临床启示
本研究突破传统单维度β细胞功能评估局限,首创三维评估体系(PIF-S/L/A),从静息基线、负荷峰值、加速斜率三个维度动态捕捉β细胞功能全貌。该方法解决了胰岛素/C肽分泌曲线在病理状态下的不规则性难题,通过整合静息-应激-调节三阶段特征,为复杂β细胞功能评估提供了全新视角。
研究揭示PIF特征与代谢风险的深层关联:高PIF-A(加速斜率)是代谢健康的标志,反映β细胞快速反应能力;而高PIF-S(基线)和PIF-L(峰值)若伴随低PIF-A,则预示“高输出、低效率”的衰竭模式,代表β细胞在长期胰岛素抵抗压力下已处于功能衰竭边缘,对应最高疾病风险。这种模式独立于传统风险因素(如年龄、BMI),为识别糖尿病并发症高危人群提供了关键生物标志物。
在临床应用层面,PIF体系通过3时OGTT(0/30/120分钟)即可实现与5时OGTT相当的评估效果,显著提升检测便捷性。结合代谢健康人群数据建立的标准化评分模型,将实际检测值转化为具有临床意义的百分位数评分,可精准指导个性化治疗(如对“高负荷-低效型”患者早期干预)。跨人群验证(中国与芬兰)证实该评估方法具有良好的普适性,整合入现有糖尿病风险评分模型后,可显著提升预测效能,为全球不同人群β细胞功能精准评估提供了科学可靠的标准化工具。
结论与展望
多维PIF评估系统通过三个维度捕捉β细胞功能,为糖尿病预测和管理提供新工具。研究表明,PIF-A是评估代谢健康和疾病风险的关键指标。结合多维PIF指数与现有评分,可提高预测效能,支持精准医疗。未来研究将验证系统、探索PIF与并发症的关系,并开发个性化治疗策略。
参考文献
[1] The Journal of Clinical Endocrinology & Metabolism, 2026, 111, 541-552
[2] Lancet. 2023;401(10394):2149-2162.
[3] Lancet Diabetes Endocrinol. 2020;8(3):249-256.
[4] Mol Metab. 2021;46:101158.
[5] Diabetes Care. 2003;26(5):1395-1401.
[6] Diabetes Care. 2013;36(5):1229-1235. 2 comments









 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言