编者按:在3月12日世界肾脏日前夕,“‘葵’守肾安,马力全开——黄葵胶囊铸就DKD全病程管理循证新高度”线上会议重磅召开。由山东大学齐鲁医院陈丽教授担任主席,北京医院・国家老年医学中心潘琦教授、江苏省中医院孙伟教授、中国药科大学顾丰教授、上海交通大学医学院附属第六人民医院殷峻教授云端聚首,围绕糖尿病肾病(DKD)治疗创新与全程管理优化展开深入交流。
传统中药×分子前沿
黄葵胶囊打开DKD治疗新思路
为揭示黄葵胶囊治疗DKD的分子机制,顾丰教授团队开展了系统性研究。研究显示,黄葵胶囊有效成分为包含7种化合物的总黄酮(TFA)[2]。在单细胞转录组分析中,团队构建了黄葵胶囊治疗DKD的配体→受体→转录因子→靶基因调控网络等。结果表明,TFA与黄葵胶囊一样能够通过调控Tgfbr1、Itgb5、Itga3等受体及Junb、Jun、Stat1等转录因子,影响免疫浸润、纤维化等关键通路,从而缓解DKD[3]。空间转录组数据重现了这一过程,Stat1调控子与其基因表达均受到TFA的负向调控。其分析结果进一步显示,Stat1在DKD样本的CD-PC中呈特异性高强度表达,并与免疫细胞共定位,其靶基因主要富集于免疫相关功能通路,如肽抗原结合、TAP结合、整合素结合及趋化因子活性等。免疫荧光染色趋势与基因表达一致[4]。
相关研究成果已发表在iMeta、Phytotherapy Research、Phytomedicine等国际知名期刊上,标志着对黄葵胶囊这一创新中成药的认识,正从经验性应用迈向基于现代分子生物学的精准理解,为DKD的防治提供了新的思路和可靠药物选择。
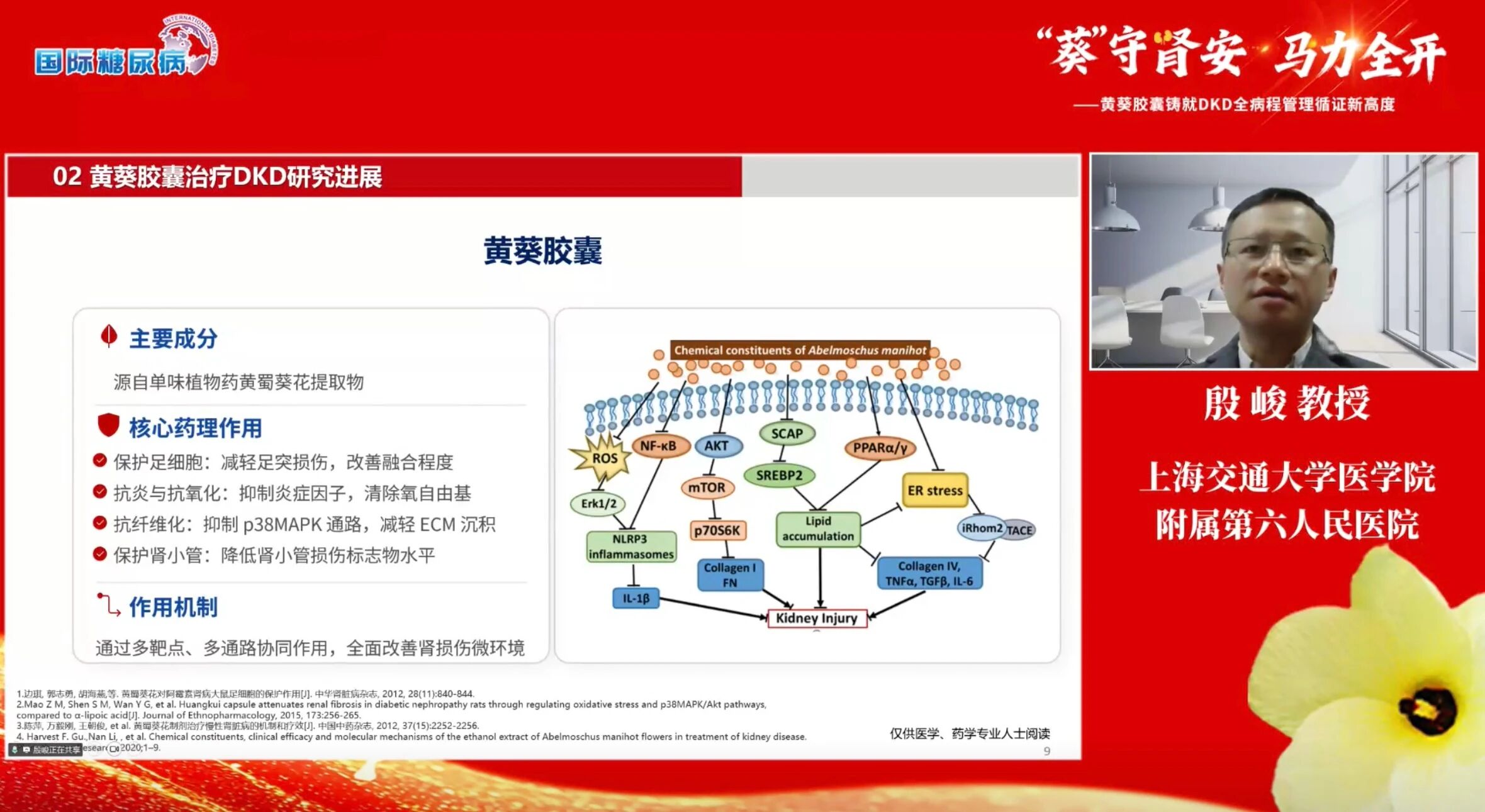
殷峻教授结合团队最新临床研究数据,系统剖析了黄葵胶囊在早期DKD防控中的显著价值。他指出,很多糖尿病患者在肾功能仍处于正常范围时,就已经出现微量白蛋白尿,这不仅是肾脏受损的早期“预警信号”,同时也是促进肾损伤持续进展的危险因素,因此加强DKD的早期识别与干预至关重要[5-6]。然而,当前西医治疗仍存在一定局限:现有治疗手段尚难以完全阻止肾功能持续下降;在部分患者中ACEI/ARB及SGLT2i等药物的应用受限;对水肿、乏力等症状的改善亦不理想。在此背景下,黄葵胶囊作为获得多部指南推荐的中成药,在DKD治疗中的价值日益凸显[7-8]。
在贾伟平院士的带领下,上海交通大学医学院附属第六人民医院联合全国多家医院开展了黄葵胶囊治疗T2DM早期肾损伤的多中心、随机、开放、平行对照临床试验。研究共纳入239例白蛋白/肌酐比值(ACR)30-300 mg/g,估算肾小球滤过率(eGFR)≥60 mL·min-1·1.73 m-2的T2DM患者,随机分配至氯沙坦或黄葵胶囊治疗组。结果显示,两组患者ACR水平均显著下降,组间比较无统计学差异,提示黄葵胶囊在降低ACR方面与氯沙坦疗效相当。进一步按基线ACR进行分层分析发现,在ACR≥100 mg/g的患者中,两组ACR均呈现更为明显的下降趋势,其中黄葵胶囊组的降幅更为明显。此外,两组eGFR变化相近,不良事件发生率亦相当,整体安全性良好[9]。
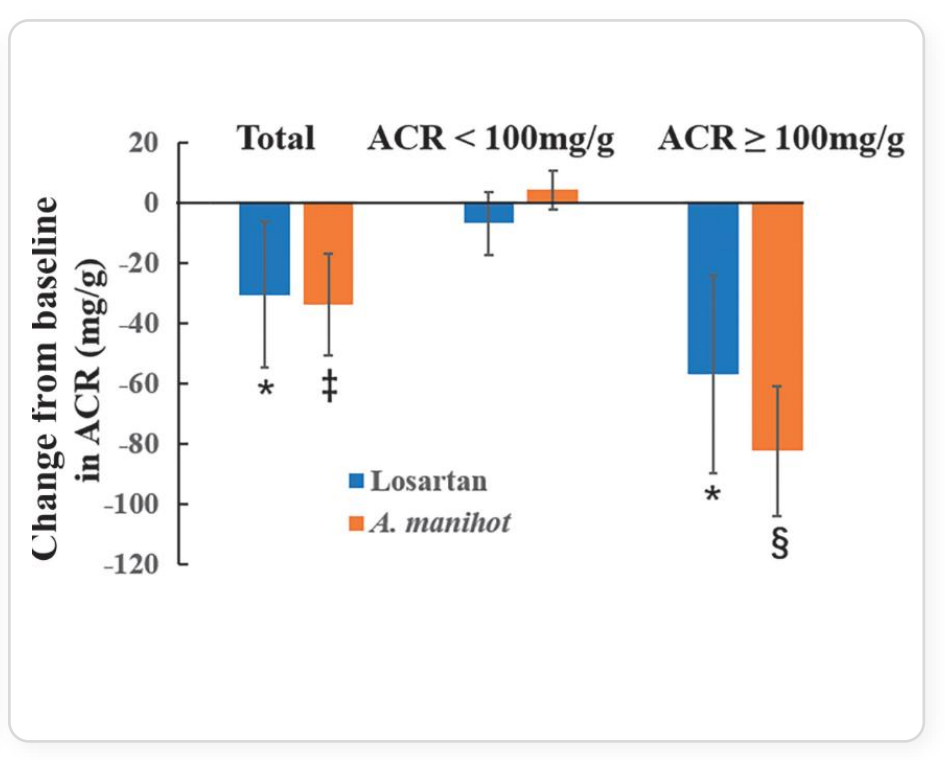
目前,该研究成果已发表于《中华医学杂志英文版》(CMJ)。研究提示,在早期DKD(微量白蛋白尿)人群中,黄葵胶囊在降低ACR方面可达到与氯沙坦相当的疗效,并具有良好的安全性。分层分析进一步提示,在ACR≥100 mg/g的患者中,其降尿蛋白获益更为突出。该研究为黄葵胶囊在DKD早期干预中的应用提供了重要循证依据。
优化全程管理
构建DKD全程管理的“中国方案”
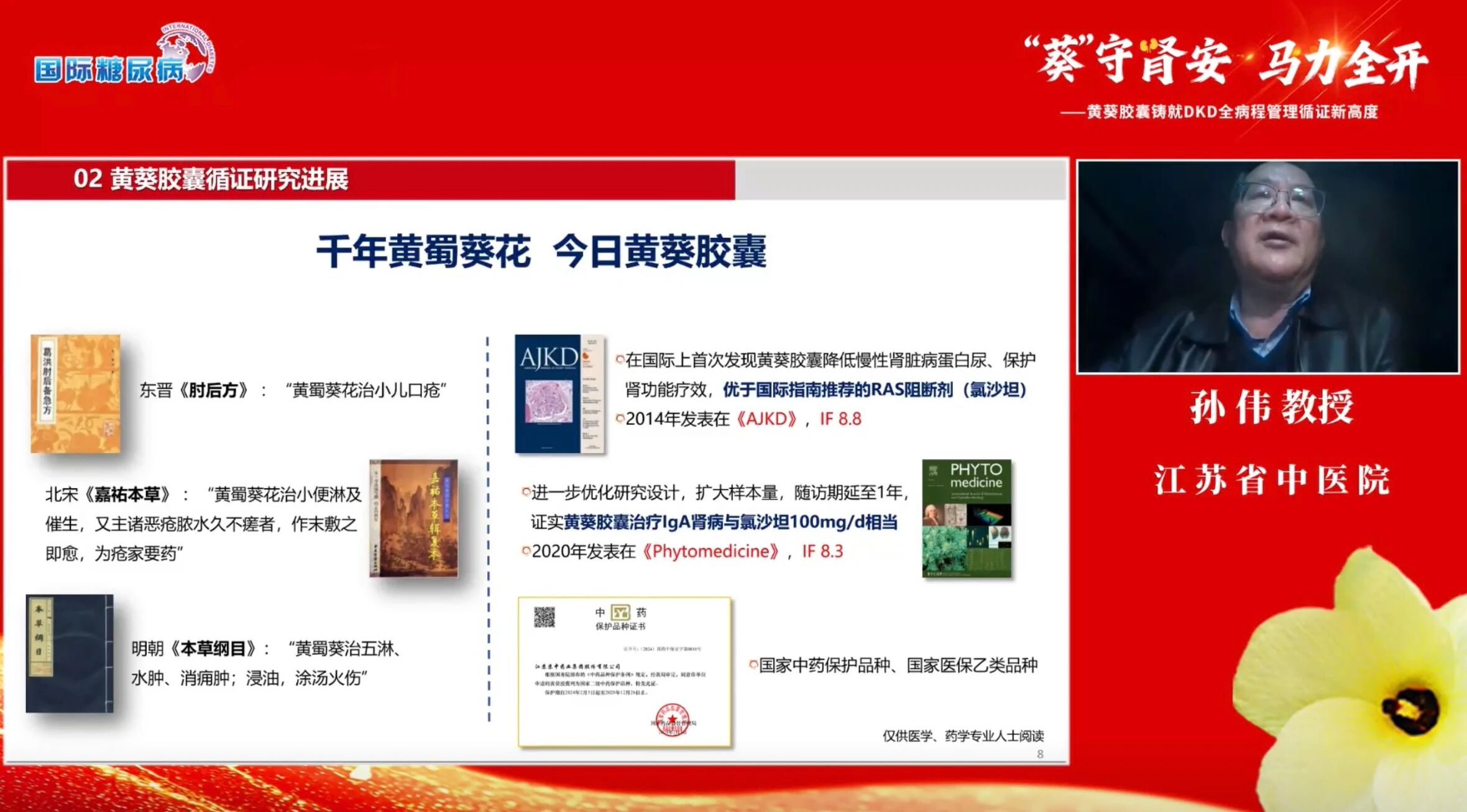
孙伟教授进一步分享了黄葵胶囊在DKD全程管理中的应用价值,并突出强调中西医结合治疗在优化疾病管理中的独特优势。他表示,无论在我国还是全球范围内,糖尿病相关慢性肾病均显著增加患者的经济负担[10-11],因此加强早期筛查与长期规范管理具有重要意义。指南建议,T2DM患者在确诊时即应进行DKD筛查,并在此后每年至少评估一次[8]。尿白蛋白是临床DKD诊断和分期的主要指标,ACR 30~299 mg/g为微量白蛋白尿,ACR≥300 mg/g为大量白蛋白尿[8]。
多项研究为黄葵胶囊在DKD全程管理中的应用提供了循证支持。除上述殷教授介绍的黄葵胶囊单药治疗早期DKD具有显著优势外,一项纳入25项随机对照试验(RCT)共1895例患者的Meta分析显示,在ACEI/ARB类药物的基础上加用黄葵胶囊,在早期DKD患者中降低蛋白尿、改善肾功能的疗效更显著[12]。另一项发表于Diabetes Care的中法合作多中心、随机、双盲、平行对照研究则在大量蛋白尿患者(300 mg/g≤ACR<2000 mg/g,eGFR≥30 ml/min/1.73 m2)中证实,黄葵胶囊在改善ACR方面与厄贝沙坦疗效相当,且联合治疗降蛋白效果更为显著。研究期间未发现严重不良反应,提示其具有良好的长期应用安全性[13]。
随着高质量循证证据的不断积累,中西医结合治疗为DKD管理提供了新的思路。通过在现代医学治疗基础上合理应用创新中成药黄葵胶囊,有望在疾病早期干预、蛋白尿控制及长期肾脏保护等方面形成协同优势,从而推动构建贯穿DKD全程管理的“中国方案”。
专家深度讨论
打造可落地DKD管理路径
关于临床应用策略,专家们认为,黄葵胶囊在DKD早中期患者中疗效明确,可与ACEI/ARB等RAAS阻断剂联合应用,实现蛋白尿优化控制和肾功能保护。在我国DKD高发的背景下,中西医结合治疗的推广需要建立可标准化、可操作的全程管理路径,包括早期筛查、动态随访及联合用药策略,以实现从早期干预到长期管理的全程覆盖,最大化改善患者预后并降低社会医疗负担。
总结
黄葵胶囊在DKD管理中体现了从基础研究到临床实践的完整闭环,其多靶点机制与全程干预理念相结合,为早中期患者提供新的治疗选择。通过科学循证和联合应用策略,中西医结合模式有望形成标准化、可推广的管理路径,实现蛋白尿控制与肾功能保护的协同效果,为DKD防治提供可持续、系统化的“中国方案”。
参考文献:
[1]《糖尿病肾脏病早期筛查与管理专家共识》编写组. 糖尿病肾脏病早期筛查与管理专家共识(2025版)[J]. 中华糖尿病杂志,2025,17(07):786-800.
DOI:10.3760/cma.j.cn115791-20241231-00768
[2]Li N, Tang H, Wu L, et al. Chemical constituents, clinical efficacy and molecular mechanisms of the ethanol extract of Abelmoschus manihot flowers in treatment of kidney diseases. Phytother Res. 2021 Jan;35(1):198-206. doi: 10.1002/ptr.6818. Epub 2020 Jul 27. PMID: 32716080; PMCID: PMC7891592.
[3]Wu C, Tang H, Cui X, et al. A single-cell profile reveals the transcriptional regulation responded for Abelmoschus manihot (L.) treatment in diabetic kidney disease. Phytomedicine. 2024 Jul 25;130:155642. doi: 10.1016/j.phymed.2024.155642. Epub 2024 May 10. PMID: 38759315.
[4]Wu C, Tang H, Yu Y, et al. Single-cell spatial transcriptomics reveals potential molecular mechanisms of Abelmoschus manihot (L.) medic in treating diabetic kidney disease. Imeta. 2025 Dec 8;4(6):e70099. doi: 10.1002/imt2.70099. PMID: 41472859; PMCID: PMC12747534.
[5]RoscioniSS, et al. Kidney Int. 2014;86(1):40-49.
[6]Liu D, et al. Adv Exp Med Biol. 2019;1165:487-500
[7]基本公共卫生服务项目基层糖尿病防治管理办公室, 中华医学会糖尿病学分会. 国家基层糖尿病防治管理指南(2025)[J]. 中华内科杂志, 2025, 64(12): 1169-1186. DOI: 10.3760/cma.j.cn112138-20250924-00572.
[8]中华医学会糖尿病学分会. 中国糖尿病防治指南(2024版). 中华糖尿病杂志,2025,17(01):16-139. DOI:10.3760/cma.j.cn115791-20241203-00705
[9]Yin J, Chen S, Xie L, et al. Efficacy and safety of Abelmoschus manihot in the treatment of type 2 diabetes and early diabetic kidney disease: A multicenter randomized, open-label, parallel-controlled clinical trial. Chin Med J (Engl). 2026 Feb 4. doi: 10.1097/CM9.0000000000003995. Epub ahead of print. PMID: 41640257.
[10]USRDS 2021.https://adr.usrds.org/2021/chronic-kidney-disease/6-healthcare-expenditures-for-persons-with-ckd
[11]Zhang L, et al.Kidney Int Suppl (2011). 2020 Dec;10(2)e97-e185
[12]张苗苗,张庆,李冰,等.黄葵胶囊联合ACEI/ARB类药物治疗早期糖尿病肾病随机对照研究的Meta分析和试验序贯分析[J].中国医院用药评价与分析, 2023, 23(3):329-338.
[13]Zhao J, Tostivint I, Xu L, et al. Efficacy of Combined Abelmoschus manihot and Irbesartan for Reduction of Albuminuria in Patients With Type 2 Diabetes and Diabetic Kidney Disease: A Multicenter Randomized Double-Blind Parallel Controlled Clinical Trial. Diabetes Care. 2022 Jul 7;45(7):e113-e115. doi: 10.2337/dc22-0607. PMID: 35613364; PMCID: PMC9274216. 2 comments

传统中药×分子前沿
黄葵胶囊打开DKD治疗新思路
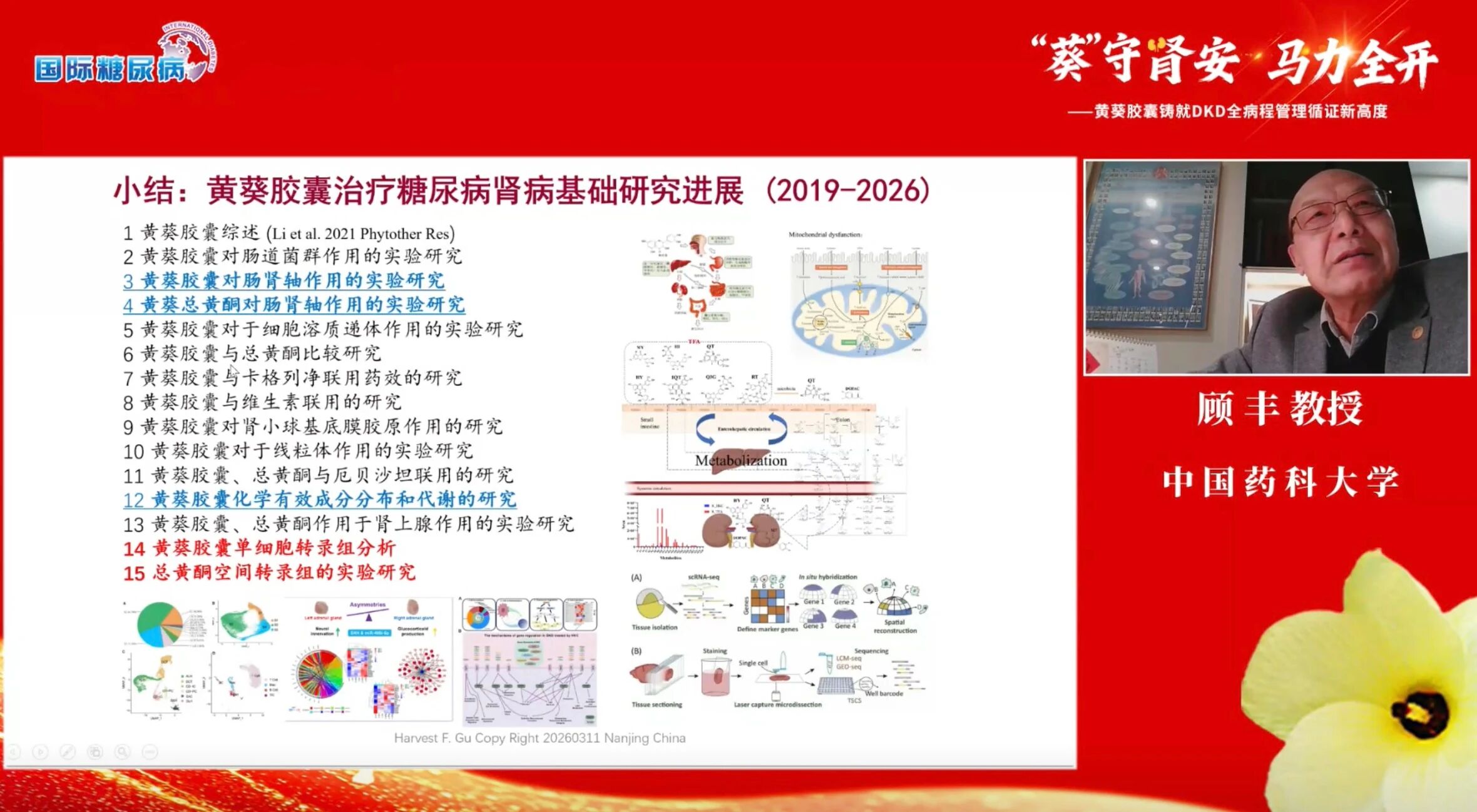
为揭示黄葵胶囊治疗DKD的分子机制,顾丰教授团队开展了系统性研究。研究显示,黄葵胶囊有效成分为包含7种化合物的总黄酮(TFA)[2]。在单细胞转录组分析中,团队构建了黄葵胶囊治疗DKD的配体→受体→转录因子→靶基因调控网络等。结果表明,TFA与黄葵胶囊一样能够通过调控Tgfbr1、Itgb5、Itga3等受体及Junb、Jun、Stat1等转录因子,影响免疫浸润、纤维化等关键通路,从而缓解DKD[3]。空间转录组数据重现了这一过程,Stat1调控子与其基因表达均受到TFA的负向调控。其分析结果进一步显示,Stat1在DKD样本的CD-PC中呈特异性高强度表达,并与免疫细胞共定位,其靶基因主要富集于免疫相关功能通路,如肽抗原结合、TAP结合、整合素结合及趋化因子活性等。免疫荧光染色趋势与基因表达一致[4]。
相关研究成果已发表在iMeta、Phytotherapy Research、Phytomedicine等国际知名期刊上,标志着对黄葵胶囊这一创新中成药的认识,正从经验性应用迈向基于现代分子生物学的精准理解,为DKD的防治提供了新的思路和可靠药物选择。
防治关口前移
黄葵胶囊在早期DKD防控中的价值
殷峻教授结合团队最新临床研究数据,系统剖析了黄葵胶囊在早期DKD防控中的显著价值。他指出,很多糖尿病患者在肾功能仍处于正常范围时,就已经出现微量白蛋白尿,这不仅是肾脏受损的早期“预警信号”,同时也是促进肾损伤持续进展的危险因素,因此加强DKD的早期识别与干预至关重要[5-6]。然而,当前西医治疗仍存在一定局限:现有治疗手段尚难以完全阻止肾功能持续下降;在部分患者中ACEI/ARB及SGLT2i等药物的应用受限;对水肿、乏力等症状的改善亦不理想。在此背景下,黄葵胶囊作为获得多部指南推荐的中成药,在DKD治疗中的价值日益凸显[7-8]。
在贾伟平院士的带领下,上海交通大学医学院附属第六人民医院联合全国多家医院开展了黄葵胶囊治疗T2DM早期肾损伤的多中心、随机、开放、平行对照临床试验。研究共纳入239例白蛋白/肌酐比值(ACR)30-300 mg/g,估算肾小球滤过率(eGFR)≥60 mL·min-1·1.73 m-2的T2DM患者,随机分配至氯沙坦或黄葵胶囊治疗组。结果显示,两组患者ACR水平均显著下降,组间比较无统计学差异,提示黄葵胶囊在降低ACR方面与氯沙坦疗效相当。进一步按基线ACR进行分层分析发现,在ACR≥100 mg/g的患者中,两组ACR均呈现更为明显的下降趋势,其中黄葵胶囊组的降幅更为明显。此外,两组eGFR变化相近,不良事件发生率亦相当,整体安全性良好[9]。

目前,该研究成果已发表于《中华医学杂志英文版》(CMJ)。研究提示,在早期DKD(微量白蛋白尿)人群中,黄葵胶囊在降低ACR方面可达到与氯沙坦相当的疗效,并具有良好的安全性。分层分析进一步提示,在ACR≥100 mg/g的患者中,其降尿蛋白获益更为突出。该研究为黄葵胶囊在DKD早期干预中的应用提供了重要循证依据。
优化全程管理
构建DKD全程管理的“中国方案”

孙伟教授进一步分享了黄葵胶囊在DKD全程管理中的应用价值,并突出强调中西医结合治疗在优化疾病管理中的独特优势。他表示,无论在我国还是全球范围内,糖尿病相关慢性肾病均显著增加患者的经济负担[10-11],因此加强早期筛查与长期规范管理具有重要意义。指南建议,T2DM患者在确诊时即应进行DKD筛查,并在此后每年至少评估一次[8]。尿白蛋白是临床DKD诊断和分期的主要指标,ACR 30~299 mg/g为微量白蛋白尿,ACR≥300 mg/g为大量白蛋白尿[8]。
多项研究为黄葵胶囊在DKD全程管理中的应用提供了循证支持。除上述殷教授介绍的黄葵胶囊单药治疗早期DKD具有显著优势外,一项纳入25项随机对照试验(RCT)共1895例患者的Meta分析显示,在ACEI/ARB类药物的基础上加用黄葵胶囊,在早期DKD患者中降低蛋白尿、改善肾功能的疗效更显著[12]。另一项发表于Diabetes Care的中法合作多中心、随机、双盲、平行对照研究则在大量蛋白尿患者(300 mg/g≤ACR<2000 mg/g,eGFR≥30 ml/min/1.73 m2)中证实,黄葵胶囊在改善ACR方面与厄贝沙坦疗效相当,且联合治疗降蛋白效果更为显著。研究期间未发现严重不良反应,提示其具有良好的长期应用安全性[13]。
随着高质量循证证据的不断积累,中西医结合治疗为DKD管理提供了新的思路。通过在现代医学治疗基础上合理应用创新中成药黄葵胶囊,有望在疾病早期干预、蛋白尿控制及长期肾脏保护等方面形成协同优势,从而推动构建贯穿DKD全程管理的“中国方案”。
专家深度讨论
打造可落地DKD管理路径

关于临床应用策略,专家们认为,黄葵胶囊在DKD早中期患者中疗效明确,可与ACEI/ARB等RAAS阻断剂联合应用,实现蛋白尿优化控制和肾功能保护。在我国DKD高发的背景下,中西医结合治疗的推广需要建立可标准化、可操作的全程管理路径,包括早期筛查、动态随访及联合用药策略,以实现从早期干预到长期管理的全程覆盖,最大化改善患者预后并降低社会医疗负担。
总结
黄葵胶囊在DKD管理中体现了从基础研究到临床实践的完整闭环,其多靶点机制与全程干预理念相结合,为早中期患者提供新的治疗选择。通过科学循证和联合应用策略,中西医结合模式有望形成标准化、可推广的管理路径,实现蛋白尿控制与肾功能保护的协同效果,为DKD防治提供可持续、系统化的“中国方案”。
参考文献:
[1]《糖尿病肾脏病早期筛查与管理专家共识》编写组. 糖尿病肾脏病早期筛查与管理专家共识(2025版)[J]. 中华糖尿病杂志,2025,17(07):786-800.
DOI:10.3760/cma.j.cn115791-20241231-00768
[2]Li N, Tang H, Wu L, et al. Chemical constituents, clinical efficacy and molecular mechanisms of the ethanol extract of Abelmoschus manihot flowers in treatment of kidney diseases. Phytother Res. 2021 Jan;35(1):198-206. doi: 10.1002/ptr.6818. Epub 2020 Jul 27. PMID: 32716080; PMCID: PMC7891592.
[3]Wu C, Tang H, Cui X, et al. A single-cell profile reveals the transcriptional regulation responded for Abelmoschus manihot (L.) treatment in diabetic kidney disease. Phytomedicine. 2024 Jul 25;130:155642. doi: 10.1016/j.phymed.2024.155642. Epub 2024 May 10. PMID: 38759315.
[4]Wu C, Tang H, Yu Y, et al. Single-cell spatial transcriptomics reveals potential molecular mechanisms of Abelmoschus manihot (L.) medic in treating diabetic kidney disease. Imeta. 2025 Dec 8;4(6):e70099. doi: 10.1002/imt2.70099. PMID: 41472859; PMCID: PMC12747534.
[5]RoscioniSS, et al. Kidney Int. 2014;86(1):40-49.
[6]Liu D, et al. Adv Exp Med Biol. 2019;1165:487-500
[7]基本公共卫生服务项目基层糖尿病防治管理办公室, 中华医学会糖尿病学分会. 国家基层糖尿病防治管理指南(2025)[J]. 中华内科杂志, 2025, 64(12): 1169-1186. DOI: 10.3760/cma.j.cn112138-20250924-00572.
[8]中华医学会糖尿病学分会. 中国糖尿病防治指南(2024版). 中华糖尿病杂志,2025,17(01):16-139. DOI:10.3760/cma.j.cn115791-20241203-00705
[9]Yin J, Chen S, Xie L, et al. Efficacy and safety of Abelmoschus manihot in the treatment of type 2 diabetes and early diabetic kidney disease: A multicenter randomized, open-label, parallel-controlled clinical trial. Chin Med J (Engl). 2026 Feb 4. doi: 10.1097/CM9.0000000000003995. Epub ahead of print. PMID: 41640257.
[10]USRDS 2021.https://adr.usrds.org/2021/chronic-kidney-disease/6-healthcare-expenditures-for-persons-with-ckd
[11]Zhang L, et al.Kidney Int Suppl (2011). 2020 Dec;10(2)e97-e185
[12]张苗苗,张庆,李冰,等.黄葵胶囊联合ACEI/ARB类药物治疗早期糖尿病肾病随机对照研究的Meta分析和试验序贯分析[J].中国医院用药评价与分析, 2023, 23(3):329-338.
[13]Zhao J, Tostivint I, Xu L, et al. Efficacy of Combined Abelmoschus manihot and Irbesartan for Reduction of Albuminuria in Patients With Type 2 Diabetes and Diabetic Kidney Disease: A Multicenter Randomized Double-Blind Parallel Controlled Clinical Trial. Diabetes Care. 2022 Jul 7;45(7):e113-e115. doi: 10.2337/dc22-0607. PMID: 35613364; PMCID: PMC9274216. 2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言