撰稿/审校
毛晓兵 徐勇
西南医科大学附属医院
泛素化/去泛素化作为一种蛋白质翻译后修饰,在调节蛋白质的稳定性、定位和功能,参与多种疾病的病理生理中起着至关重要的作用。去泛素化酶(DUBs)通过去除底物蛋白中的泛素分子,负向调节泛素化过程。目前关于DUBs对糖尿病肾病(DN)影响的研究已引起医学界的广泛重视。近日,西南医科大学附属医院徐勇教授团队在cell子刊Trends in Pharmacological Sciences在线发表了题为“Deubiquitinating enzymes as therapeutic targets in diabetic nephropathy”的综述(该综述被选为当期封面文章),系统阐述了DUBs在DN发生发展中的作用及其临床转化价值,展示了DUBs抑制剂在DN治疗中的应用前景。

图片该综述被选为Trends Pharmacol Sci. 2026;47(2)封面文章
去泛素化酶(DUBs)是泛素–蛋白酶体系统(UPS)中的“精细调控者”,通过特异性去除蛋白质特定氨基酸位点泛素修饰,精准调控关键蛋白的稳定性和亚细胞定位,在代谢稳态维持、细胞应激应答及信号转导等过程中发挥不可替代的作用。根据结构和功能特点,DUBs可分为多个家族,包括USP家族、UCH家族、OTU家族、MJD家族、JAMM家族、MINDY家族以及ZUFSP/ZUP1家族。近年来的研究发现,多种去泛素化酶在DN状态下发生异常改变,提示DUBs可能深度参与了疾病的发生和进展。
在DN进展过程中,持续加重的氧化应激和线粒体功能障碍是导致肾小管损伤的重要驱动因素。为了应对氧化损伤,细胞会主动启动多条防御通路:一方面,PINK1/Parkin介导的线粒体自噬负责清除受损线粒体;另一方面,Nrf2通路促进抗氧化基因的表达,而AMPK通路则通过调控能量代谢降低活性氧(ROS)水平。
然而,在DN状态下,部分DUBs的异常激活却成为这些保护机制发挥作用的“障碍”。有研究发现,USP30通过移除线粒体外膜蛋白的泛素修饰链,对抗PINK1/Parkin介导的线粒体自噬,导致受损线粒体堆积及氧化应激状态;USP15通过稳定Keap1、加速Nrf2降解,抑制抗氧化基因的转录,导致细胞抗氧化能力减弱;而USP21下调ATP柠檬酸裂解酶ACLY泛素化修饰,抑制能量代谢核心枢纽AMPK的磷酸化修饰及活性水平,削弱细胞的能量感应和代谢调节能力。靶向抑制这些异常活化的DUBs,能够重新“释放”细胞的内源性防御通路,有效缓解氧化应激损伤,并展现出显著的肾脏保护潜力。
此外,持续存在的慢性炎症被认为是推动DN不断进展的关键动力之一。DUBs在炎症微环境调控中起到“双刃剑”作用。USP15靶向调控并稳定TAK1,通过促炎症核心因子核因子-κB(NF-κB)持续激活下游炎症通路,从而加速炎症进程。相反,USP25通过精准调控TRAF6泛素化修饰状态,阻断促炎症关键信号通路丝裂原活化蛋白激酶(MAPK)通路,抑制炎症信号的传递,发挥抗炎作用。因此,精准靶向阻断特定促炎型DUBs,有效阻断肾脏局部的慢性炎症反应,有望成为DN新的治疗思路。
越来越多的临床前研究证据表明,DUB抑制剂在延缓DN进展方面展现出积极疗效。USP4靶向抑制剂Vialinin A干预显著减轻肾脏纤维化和瘢痕形成。还有研究发现,拓扑异构酶II抑制剂米托蒽醌(Mitoxantrone)可靶向抑制USP11,有效延缓肾纤维化进程。这些研究为DUBs作为潜在治疗靶点提供了有力支持。
然而,DUB抑制剂的临床转化仍面临多重挑战。一方面,DUB家族成员之间高度的结构同源性,使得药物难以实现理想的靶点特异性,并增加了脱靶效应的风险;另一方面,许多DUB具有广泛且依赖细胞环境的底物特异性,其潜在的系统性毒性也亟需谨慎评估。因此,提高肾脏靶向性、降低脱靶效应与毒性风险,仍是DUB抑制剂研发中亟待突破的关键问题,也是影响其临床转化的核心瓶颈。聚焦基于结构的药物设计,提升抑制剂的选择性;结合肾脏靶向递送系统,实现对病变部位的“精准打击”——这些策略可能为延缓DN进展至终末期肾病、改善患者长期预后提供新的治疗思路。
第一作者为西南医科大学2024级硕士刘静,通讯作者为龙洋副研究员、毛晓兵助理研究员、徐勇教授。该团队长期致力于代谢性血管疾病的基础与临床转化研究。
文献引用:Liu J, Tan X, Fang X, et al. Deubiquitinating enzymes as therapeutic targets in diabetic nephropathy. Trends Pharmacol Sci. 2026;47(2):198-215. doi: 10.1016/j.tips.2025.07.015 2 comments
毛晓兵 徐勇
西南医科大学附属医院
泛素化/去泛素化作为一种蛋白质翻译后修饰,在调节蛋白质的稳定性、定位和功能,参与多种疾病的病理生理中起着至关重要的作用。去泛素化酶(DUBs)通过去除底物蛋白中的泛素分子,负向调节泛素化过程。目前关于DUBs对糖尿病肾病(DN)影响的研究已引起医学界的广泛重视。近日,西南医科大学附属医院徐勇教授团队在cell子刊Trends in Pharmacological Sciences在线发表了题为“Deubiquitinating enzymes as therapeutic targets in diabetic nephropathy”的综述(该综述被选为当期封面文章),系统阐述了DUBs在DN发生发展中的作用及其临床转化价值,展示了DUBs抑制剂在DN治疗中的应用前景。

图片该综述被选为Trends Pharmacol Sci. 2026;47(2)封面文章
去泛素化酶(DUBs)是泛素–蛋白酶体系统(UPS)中的“精细调控者”,通过特异性去除蛋白质特定氨基酸位点泛素修饰,精准调控关键蛋白的稳定性和亚细胞定位,在代谢稳态维持、细胞应激应答及信号转导等过程中发挥不可替代的作用。根据结构和功能特点,DUBs可分为多个家族,包括USP家族、UCH家族、OTU家族、MJD家族、JAMM家族、MINDY家族以及ZUFSP/ZUP1家族。近年来的研究发现,多种去泛素化酶在DN状态下发生异常改变,提示DUBs可能深度参与了疾病的发生和进展。
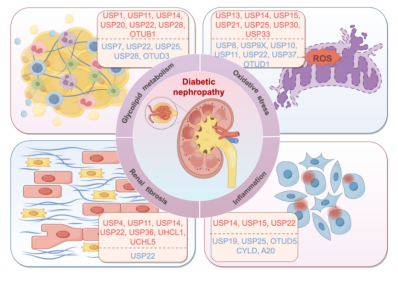
在DN进展过程中,持续加重的氧化应激和线粒体功能障碍是导致肾小管损伤的重要驱动因素。为了应对氧化损伤,细胞会主动启动多条防御通路:一方面,PINK1/Parkin介导的线粒体自噬负责清除受损线粒体;另一方面,Nrf2通路促进抗氧化基因的表达,而AMPK通路则通过调控能量代谢降低活性氧(ROS)水平。
然而,在DN状态下,部分DUBs的异常激活却成为这些保护机制发挥作用的“障碍”。有研究发现,USP30通过移除线粒体外膜蛋白的泛素修饰链,对抗PINK1/Parkin介导的线粒体自噬,导致受损线粒体堆积及氧化应激状态;USP15通过稳定Keap1、加速Nrf2降解,抑制抗氧化基因的转录,导致细胞抗氧化能力减弱;而USP21下调ATP柠檬酸裂解酶ACLY泛素化修饰,抑制能量代谢核心枢纽AMPK的磷酸化修饰及活性水平,削弱细胞的能量感应和代谢调节能力。靶向抑制这些异常活化的DUBs,能够重新“释放”细胞的内源性防御通路,有效缓解氧化应激损伤,并展现出显著的肾脏保护潜力。
此外,持续存在的慢性炎症被认为是推动DN不断进展的关键动力之一。DUBs在炎症微环境调控中起到“双刃剑”作用。USP15靶向调控并稳定TAK1,通过促炎症核心因子核因子-κB(NF-κB)持续激活下游炎症通路,从而加速炎症进程。相反,USP25通过精准调控TRAF6泛素化修饰状态,阻断促炎症关键信号通路丝裂原活化蛋白激酶(MAPK)通路,抑制炎症信号的传递,发挥抗炎作用。因此,精准靶向阻断特定促炎型DUBs,有效阻断肾脏局部的慢性炎症反应,有望成为DN新的治疗思路。
越来越多的临床前研究证据表明,DUB抑制剂在延缓DN进展方面展现出积极疗效。USP4靶向抑制剂Vialinin A干预显著减轻肾脏纤维化和瘢痕形成。还有研究发现,拓扑异构酶II抑制剂米托蒽醌(Mitoxantrone)可靶向抑制USP11,有效延缓肾纤维化进程。这些研究为DUBs作为潜在治疗靶点提供了有力支持。
然而,DUB抑制剂的临床转化仍面临多重挑战。一方面,DUB家族成员之间高度的结构同源性,使得药物难以实现理想的靶点特异性,并增加了脱靶效应的风险;另一方面,许多DUB具有广泛且依赖细胞环境的底物特异性,其潜在的系统性毒性也亟需谨慎评估。因此,提高肾脏靶向性、降低脱靶效应与毒性风险,仍是DUB抑制剂研发中亟待突破的关键问题,也是影响其临床转化的核心瓶颈。聚焦基于结构的药物设计,提升抑制剂的选择性;结合肾脏靶向递送系统,实现对病变部位的“精准打击”——这些策略可能为延缓DN进展至终末期肾病、改善患者长期预后提供新的治疗思路。
第一作者为西南医科大学2024级硕士刘静,通讯作者为龙洋副研究员、毛晓兵助理研究员、徐勇教授。该团队长期致力于代谢性血管疾病的基础与临床转化研究。
文献引用:Liu J, Tan X, Fang X, et al. Deubiquitinating enzymes as therapeutic targets in diabetic nephropathy. Trends Pharmacol Sci. 2026;47(2):198-215. doi: 10.1016/j.tips.2025.07.015 2 comments







 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言