慢性肾脏病(CKD)患者的心血管疾病风险较普通人群显著升高,心血管事件往往早于终末期肾病(ESRD)发生,成为CKD患者死亡的首要原因。钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)作为CKD治疗的核心药物,既往重磅研究如DAPA-CKD等证实其在广泛CKD患者中具有显著的心肾获益,但具体作用机制长期以来尚未完全明确。近期,一项发表于顶刊NEJM Evidence的DECODE-CKD研究[1,2]首次披露了SGLT2i对CKD患者心脏结构和功能的直接影响,为解析其心肾保护机制提供了关键临床证据,也为CKD患者的心血管风险管控带来了全新思路。
一、研究背景
CKD与心血管疾病之间存在紧密的病理生理关联,心脏结构和功能的不良重塑是驱动CKD患者心血管风险升高的核心因素。左心室重构是心力衰竭的典型特征,在CKD患者中也较为普遍,且与CKD患者心血管疾病发病率、死亡率以及ESRD的进展密切相关[3-5]。左心室质量指数(LVMi)作为心脏重构的核心指标,即便在无明确心血管疾病的人群中,也是预测未来心血管事件的强力指标[2],因此成为探究CKD患者心血管保护机制的关键靶点。
SGLT2i最初作为降糖药开发,后续发现其在降低CKD患者肾脏疾病进展、心力衰竭事件以及心血管和全因死亡风险方面具有显著效果,且这些效果独立于患者是否合并糖尿病[6-8],现已成为CKD治疗的基石药物。尽管如此,SGLT2i在CKD中发挥心肾保护作用的具体机制尚未完全阐明。目前主流假说认为,SGLT2i可通过渗透性利尿作用减少心脏负荷,改善心室负荷,进而可能逆转心脏重构[9-11]。然而,以往关于SGLT2i对心脏重构影响的研究主要集中在心力衰竭和/或糖尿病患者中,对于CKD患者的研究相对较少,这也成为DECODE-CKD研究开展的核心科学背景。
二、研究设计
DECODE-CKD是一项单中心、随机、双盲、安慰剂对照的试验,旨在评估达格列净对CKD患者心脏结构和功能的影响。研究纳入了估算肾小球滤过率(eGFR)在20~59或≥60 ml/(min·1.73m2)且尿白蛋白肌酐比(UACR)≥200 mg/g的患者。参与者在基线和6个月随访时接受了临床评估,包括超声心动图和生化分析。
主要终点设定为6个月时LVMi的变化,次要终点包括心脏收缩和舒张功能的变化以及高敏肌钙蛋白I、B型利钠肽原、血红蛋白、UACR等心肾生物标志物的变化。三、研究结果
01、基线特征
在筛选的268例CKD患者中,222例被随机分配到达格列净组(n=110)或安慰剂组(n=112)。两组基线人口学特征以及超声心动图指标均衡。
总体来说,患者平均年龄为67.5岁,29.3%为女性;在入组时,34.2%有心血管疾病史,5.9%有心力衰竭史,75.7%有高血压,8.6%有糖尿病。CKD的最常见原因是高血压性肾病(25.7%)和多囊肾病(16.7%)。治疗前,两组平均LVMi均处于正常范围,左室肥厚(女性:LVMi>95 kg/㎡;男性:LVMi>115 kg/㎡)的总体患病率为10.4%。
02、主要终点
治疗6个月后,结果显示,达格列净组的LVMi平均降低了5.53 g/m2,而安慰剂组增加了4.35 g/m2,两组之间的估计平均差异为-8.44 g/m2(95%CI:-11.83~-5.06;P<0.001,图1左)。这一变化主要由室间隔厚度的减少驱动,达格列净组的室间隔厚度平均减少了0.08 cm(95%CI:-0.013~-0.05)。
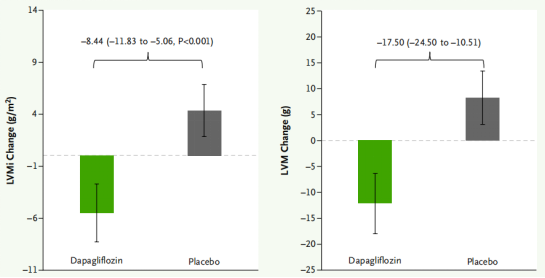
图1. 达格列净对LVMi和左室质量(LVM)参数的影响
亚组分析显示,无论患者性别、年龄、体重指数(BMI)、基线eGFR水平、UACR分级、左室射血分数(LVEF)水平 、N末端B型利钠肽原水平、是否合并心血管疾病或使用肾素-血管紧张素系统抑制剂(RASi),达格列净降低LVMi的效果均保持一致,表明其心脏保护作用具有广泛的适用性。
03、次要终点
在心脏收缩功能指标方面,达格列净组左室质量(LVM)下降12.14 g,安慰剂组则增加8.27 g,组间差异达17.5 g(95%CI:-24.50~-10.51,图1右),进一步佐证了心脏结构的改善;但在LVEF、整体纵向应变(GLS)等收缩功能指标以及舒张功能相关指标方面,两组未出现显著差异。这提示达格列净对CKD患者的心血管保护效应,主要通过逆转心脏结构重塑实现,而非直接改善心脏收缩或舒张功能。
生物标志物检测结果显示,eGFR较安慰剂组下降更明显[6个月时平均差异-2.15 ml/(min·1.73m2),95%CI:-3.71~- 0.59],但eGFR的短期下降符合SGLT2i的已知药理效应,通常不反映肾脏实质损伤,也不影响持续用药带来的远期心肾获益。其他指标组间无显著差异。
04、安全性评估
达格列净组与安慰剂组的不良事件发生率相近,整体安全性良好,与既往研究中达格列净的耐受性特征一致。达格列净组血红蛋白水平升高(平均差异+0.23 mmol/l,95%CI:0.04~0.41),严重不良事件发生率为4.5%,包括急性肾盂肾炎、血红蛋白升高、缺铁性贫血、便秘和缺血性卒中各1例,无死亡病例报告。
四、讨论与总结
DECODE-CKD研究通过严谨的试验设计,填补了SGLT2i在CKD患者心脏结构影响领域的研究空白,核心价值在于首次为SGLT2i的心脏保护机制提供了直接的结构学证据——达格列净通过显著降低CKD患者LVMi、逆转心脏重构,成为其降低心血管事件风险的关键机制之一。这一发现与此前DAPA-CKD试验结果相互印证:DAPA-CKD证实达格列净能降低CKD患者的心血管死亡和心力衰竭风险,而DECODE-CKD则揭示了这一获益的核心来源是心脏结构重塑的早期改善。
尤为重要的是,DECODE-CKD纳入的患者中仅8.6%合并糖尿病,远低于DAPA-CKD试验(67.5%)[7],这一特征明确证实达格列净的心脏保护作用独立于降糖效应,为非糖尿病CKD患者的心血管风险管控提供了强有力的循证支持,进一步拓展了SGLT2i的适用人群边界。
临床实践中,应关注CKD患者的心脏结构评估。超声心动图检测LVMi可作为评估心血管风险和治疗反应的重要指标,即使无明显心血管症状的CKD患者,也可考虑进行常规心脏结构筛查,为SGLT2i的使用提供参考。此外,试验中达格列净在不同eGFR水平、UACR分级、CKD病因、合并症情况以及用药背景等患者中的一致疗效,提示其适用范围广泛,临床医生可根据患者具体情况灵活选用。
尽管DECODE-CKD试验设计严谨,但仍存在一定局限性。首先,人群以白种人和男性为主,糖尿病患病率低但多囊肾患病率高于真实世界CKD队列,可能影响结果外推;其次,干预组基线心血管疾病患病率(40.0% vs. 28.6%)较高,虽敏感性分析调整后结果未变,但仍可能残留混杂;再者,随访时间仅为6个月,达格列净对心脏超声其他参数的影响需长期随访才能全面评估;最后,样本量不足以支持探索性比较和亚组分析,且亚组分析为事后分析,未预先设定假设,结果需谨慎解读。
综上所述,DECODE-CKD研究是CKD心血管保护领域的一项突破性成果,首次证实达格列净在CKD人群中通过降低左室重构、改善心脏结构实现心脏保护,且获益广泛、安全性良好。这一发现不仅深化了对SGLT2i心肾保护机制的理解,更将推动CKD治疗策略的优化升级,为广大CKD患者带来更全面的心血管风险防护。
参考文献
1.Bartholdy KV, et al. NEJM Evid 2025;4(11): 1-11. DOI: 10.1056/EVIDoa2500158.
2.Bartholdy KV, et al. Kidney360. 2023; 4: 143-149.
3.Shlipak MG, et al. JAMA. 2005; 293: 1737-1745.
4.Chen S-C, et al. Nephrol Dial Transplant. 2012; 27: 1064-1070.
5.Paoletti E, et al. Nephrol Dial Transplant. 2011; 26: 670-677.
6.Perkovic V, et al. N Engl J Med. 2019; 380: 2295-2306.
7.Heerspink HJL, et al. N Engl J Med. 2020; 383: 1436-1446.
8.EMPA-KIDNEY Collaborative Group. N Engl J Med. 2023; 388: 117-127.
9.Dhingra NK, et al. ESC Heart Fail. 2021; 8: 4693-4700.
10.Savage P, et al. ESC Heart Fail. 2024; 11: 3636-3648.
11.Zhang N, et al. Eur J Prev Cardiol. 2022; 28: 1961-1973.
2 comments







 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言