传统观念认为,慢性肾脏病(CKD)是一种不可逆转的进行性疾病,治疗目标仅限于延缓其向终末期肾病发展。然而,近年来一系列新型疗法的涌现,从根本上改变了这一悲观叙事。钠-葡萄糖协同转运蛋白2抑制剂、非甾体类盐皮质激素受体拮抗剂、胰高血糖素样肽-1受体激动剂以及针对IgA肾病的靶向免疫疗法等,通过临床试验证实了持续稳定肾小球滤过率并使白蛋白尿恢复正常已成为可能。这标志着CKD的治疗目标正从“延缓进展”转向“实现缓解”。近期,Navdeep Tangri等发表了一篇综述[1],系统阐述了这一治疗范式的转变,明确CKD缓解的定义与可能性,并展望其在糖尿病肾病与肾小球疾病中的实践路径,以推动肾脏病学临床思维的革新。
引言:治疗范式的根本转变
慢性肾脏病(CKD)在全球范围内广泛流行,长期以来被视为一种慢性、进行性疾病。患者和临床医生普遍认为肾功能持续下降不可避免,因此治疗的可接受目标仅是延缓CKD进展,从而推迟进入肾衰竭以及需要透析或肾移植的时间。
然而,随着对肾脏疾病认识的深入,以及能够维持肾功能的新型疗法的研发与普及,这一观点发生了根本性改变。从肾素-血管紧张素系统抑制剂开始,到用于糖尿病肾病的钠-葡萄糖协同转运蛋白2抑制剂(SGLT2i)等药物,再延伸到针对IgA肾病(IgAN)的B细胞靶向疗法和补体靶向疗法,现今的治疗方案有望完全阻止CKD的进展。特别是在糖尿病肾病领域,联合治疗时代已经到来。在肾素-血管紧张素-醛固酮系统抑制剂(RAASi)和SGLT2i的基础上,加用非甾体类盐皮质激素受体拮抗剂(ns-MRA)和胰高血糖素样肽-1受体激动剂(GLP-1RA)的三联或四联疗法,已使伴有显著临床意义白蛋白尿(例如尿白蛋白肌酐比[UACR] > 100 mg/mmol)的患者能够实现白蛋白尿降低超过50%,使UACR值恢复到接近正常范围,同时维持估算肾小球滤过率(eGFR)稳定。因此,CKD的治疗前景已从根本上从“延缓不可避免的肾功能丧失”转变为“维持eGFR与肾功能稳定”,从而达到可被定义为 “CKD缓解” 的状态。
慢性肾脏病缓解的定义
疾病缓解通常定义为体征和症状在较长时期内消失,可分为部分缓解或完全缓解。必须区分缓解与治愈,因为缓解意味着在停止治疗或疾病复发时,病情可能再现。
对于大多无症状的CKD,缓解可通过客观的肾功能标志物来界定,特别是eGFR和UACR。对于中重度CKD患者[eGFR <45 ml/(min·1.73 m²)],若其长期eGFR年下降斜率(慢性斜率)<1 ml/(min·1.73 m²)——这与健康衰老相关的预期下降水平一致——可被视为缓解的一个标准。对于疾病早期阶段的患者[eGFR >45 ml/(min·1.73 m²)],恢复到正常肾功能[eGFR >60 ml/(min·1.73 m²)]且无白蛋白尿,可被视为疾病缓解的明确指标。作者提出一个综合定义,可广泛适用于所有CKD患者,其核心是稳定的eGFR轨迹(慢性eGFR斜率<1 ml/min/1.73 m²/年,或eGFR与白蛋白尿均无异常)。
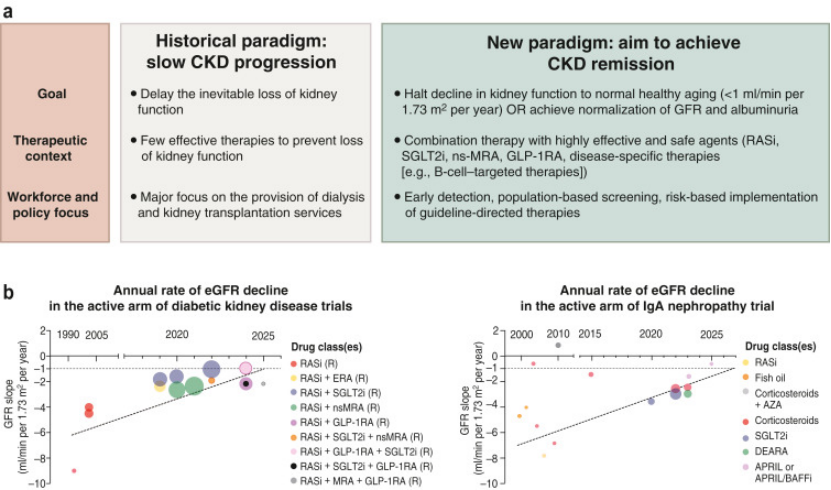
图1. CKD缓解的拟议范式(引自发表文章)
实现缓解的可能性
在长期随访的大规模人群研究中,一部分CKD患者随时间推移出现了病情逆转或缓解。然而,缓解的可能性与白蛋白尿的存在及严重程度密切相关。例如,UACR >30 mg/mmol的患者实现疾病逆转或缓解的可能性是无白蛋白尿患者的五分之一。因此,能够降低白蛋白尿的疗法,通过使UACR水平恢复正常范围,并增加实现正常慢性eGFR斜率或恢复至正常eGFR值的概率,从而提高了CKD缓解的可能性。这些研究也强调了基于白蛋白尿进行CKD筛查的重要性,因为白蛋白尿通常从A2期(UACR 3~30 mg/mmol)进展到更晚期的A3期(UACR >30 mg/mmol)。在更早期检测到白蛋白尿,更有可能实现疾病缓解,而这只有通过筛查才能实现。
在不同疾病中实现缓解的策略
01.在糖尿病肾病中实现缓解
对于合并CKD的糖尿病患者,在过去三十年里,标准治疗下的eGFR下降速率已发生显著变化。早期研究显示,糖尿病肾病患者的安慰剂组eGFR年下降速率接近10~15 ml/(min·1.73 m²),使用卡托普利后仅略微减缓至8~10 ml/(min·1.73 m²)。21世纪初的血管紧张素受体阻滞剂试验显示,治疗组eGFR年下降率为4.4 ml/(min·1.73 m²),而安慰剂组为5.2 ml/(min·1.73 m²)。即使起始eGFR在50~60 ml/(min·1.73 m²)之间,这样的下降速率仍将导致患者在大约10年内进展至肾衰竭。
SGLT2i的引入迅速改变了这一典型临床病程。针对糖尿病和非糖尿病CKD患者的专项试验表明,SGLT2i能显著减缓慢性eGFR下降斜率。例如,在CREDENCE试验中,在背景RAASi治疗基础上,加用卡格列净组的eGFR年斜率为-1.85 ml/(min·1.73 m²),而安慰剂组为-4.52 ml/(min·1.73 m²)。DAPA-CKD试验报告,达格列净组的慢性eGFR年斜率为-1.58 ml/(min·1.73 m²),而仅用RAASi治疗组为-3.84 ml/(min·1.73 m²)。
近期,在RAASi和SGLT2i基础上联合使用ns-MRA和GLP-1RA,进一步减缓了这些人群的eGFR下降和白蛋白尿。现有的临床试验汇总数据(包括FLOW试验)表明,SGLT2i与GLP-1RA联合治疗比任一单药更能改善eGFR下降,使慢性eGFR年斜率达到-1.3至-1.5 ml/(min·1.73 m²)。此外,近期发表的CONFIDENCE试验数据显示,大多数接受SGLT2i与ns-MRA联合治疗的患者实现了白蛋白尿降低超过50%。对于作为全球CKD和肾衰竭首要原因的2型糖尿病患者,这些发现提示缓解是可能且可实现的,并可能显著改善肾脏和心血管疾病负担。因此,治疗目标应是大幅降低白蛋白尿,并将eGFR年下降率减缓至约1 ml/(min·1.73 m²)。
02.在肾小球疾病中实现缓解
缓解的概念在某些肾小球疾病中已确立,如微小病变肾病和膜性肾病。对于这些疾病,治疗预期是实现蛋白尿的完全或接近完全缓解。此外,诊断时eGFR通常得以保留,治疗及恢复到与年龄相关的肾功能丧失速率是治疗的隐含目标。
相比之下,对于进行性肾小球疾病(如IgA肾病)患者,历史上的治疗重点是延缓进展而非实现缓解。针对这些疾病的新疗法要求我们将思维模式再次转变:从仅仅延缓进展转向以完全缓解为目标。事实上,多项IgA肾病靶向B细胞疗法的临床试验数据显示,接受治疗患者的eGFR年下降斜率 consistently 约为1 ml/(min·1.73 m²)或更低,而此前通过最佳支持治疗和针对非免疫性肾损伤机制的疗法所能达到的下降速率为2-3 ml/min/1.73 m²/年。对于全球最常见的肾小球疾病——IgA肾病患者,这些发现再次强调,需要通过使用针对潜在免疫生物学的疗法,并联合前述的RAASi、SGLT2i等CKD基础治疗及实现血压达标,来以缓解为目标,实现终生的肾脏健康维护。与糖尿病肾病相似,IgA肾病的联合治疗似乎也最有可能实现疾病缓解。
展望与行动呼吁
充分证据支持这一假说:即使对于已确诊肾脏病和存在高水平白蛋白尿的患者,也有相当大比例可以实现CKD缓解。鉴于CKD缓解对于降低过早死亡和肾衰竭风险具有深远意义,我们主张将CKD缓解确立为一个明确且可实现的临床目标。
CKD缓解最有可能在疾病早期(即在eGFR丧失或出现严重白蛋白尿之前)被检测到时实现。因此,可能需要在风险人群中进行结合eGFR和白蛋白尿检测的基于人群的筛查,以识别这些患者,并为他们提供实现缓解的最佳机会。
为了使这些筛查策略取得成功,必须结合风险分层和临床决策支持,以优化指南指导的药物治疗应用。越来越多的证据表明,联合治疗更有可能实现缓解,尤其是在糖尿病肾病患者中。必须克服临床惰性;当安全有效的疗法有可能使UACR降低60%至80%甚至达到正常化时,我们不应满足于30%~50%的降幅。通过基于风险的方法,可以加速启动这些疗法,例如同时启动RAASi和SGLT2i,并根据需要添加其他治疗以实现缓解。这一治疗范式应以初级保健为主导,肾脏科医生提供一致的信息和支持,以便在肾功能丧失之前进行有效治疗。
在能够获得这些变革性疗法的地区,特别是那些支付肾脏替代治疗费用的地区,应考虑引入和推广综合性筛查计划。在其他疗法尚未广泛普及的地区,卫生政策工作必须致力于将肾脏疾病列为重要的非传染性疾病,从而增加肾脏诊断和治疗手段的可及性。此外,随着旨在将这些有效疗法重新用于新适应症[1型糖尿病、多囊肾病、肾移植以及eGFR <20 ml/(min·1.73 m²)的个体]的试验结果陆续公布,针对这些存在巨大未满足需求的疾病,以实现缓解为目标的努力也应得到效仿和扩展。
总结而言,改变肾脏病学叙事的时刻已经到来。CKD不应再被视为必然进行性和不可逆转的疾病。借助新疗法,尤其是联合应用,对许多患者而言,CKD缓解既是现实的,也是可实现的。肾脏病学界现在必须将我们的重点从“延缓CKD进展”转向拥抱这一“维护肾脏健康”的前所未有的机遇。








 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言