目前,盐皮质激素受体拮抗剂(MRAs)是指南推荐用于治疗PA的药物,但传统甾体类MRA存在明显局限。非奈利酮作为第三代非甾体类MRA(ns-MRA),具有更高的盐皮质激素受体(MR)选择性和亲和力。基于此,天津医科大学总医院刘铭教授团队开展的一项研究[1],评估了在低钾血症的PA患者中,非奈利酮治疗后低血钾的纠正效果、血压调控作用及安全性,为PA治疗提供新的循证医学依据。本刊特邀刘教授对该研究予以深度点评,解析非奈利酮在PA治疗中新的价值与应用前景。
一、研究背景
PA指肾上腺皮质自主分泌醛固酮,导致体内潴钠排钾,血容量增多,肾素-血管紧张素系统活性受抑制,临床主要表现为高血压和低血钾[2]。有研究表明,9%~37%的PA患者存在低钾血症[2]。低钾血症一旦出现往往提示病情更严重、预后更差,可能会通过心律失常、肾小球变性、肾髓质血流减少等机制直接导致心肾靶器官损害,因此改善低钾血症使血清钾维持在正常水平是PA治疗的关键目标之一。
非奈利酮作为第三代非甾体类MRA,与传统甾体类MRA相比,对MR具有更高的选择性和亲和力,且对糖皮质激素、雄激素、孕激素受体的选择性较低,此前已在2型糖尿病相关慢性肾脏病(CKD)患者中证实具有良好的心肾保护作用。但该药物在低钾血症的PA患者中的疗效和安全性研究极少,因此有必要通过临床研究进一步验证。
二、研究设计
本研究为前瞻性单臂临床研究,纳入2023年4月-2024年9月天津医科大学总医院确诊的15例低钾血症的PA患者,所有患者均不适合或不愿意接受手术治疗,符合药物治疗指征。
纳入标准:确诊PA[符合高血压、低钾血症<3.5 mmol/L,醛固酮/肾素比值≥3.7(ng/dL)/(μIU/mL),卡托普利试验阳性或血浆醛固酮浓度>20 ng/dL、血浆肾素浓度<2.5 μIU/mL且伴低钾血症];入组前1个月未使用螺内酯、依普利酮等保钾利尿剂,前2周未使用除钙通道阻滞剂、α受体阻滞剂外的降压药;不适合或不愿接受手术治疗。
排除标准:认知障碍、终末期疾病、妊娠或哺乳期、血清钾>5.0 mmol/L、使用强效CYP3A4抑制剂、估算肾小球滤过率(eGFR)<25 ml/min/1.73m2,或近90天内有心肌炎、急性心肌梗死等病史。
干预措施:根据临床评估给予非奈利酮治疗,初始剂量为10 mg/d或20 mg/d(血清钾≤3.0 mmol/L且eGFR>60 ml/min/1.73m2者起始剂量20 mg/d,其余为10 mg/d),最大剂量不超过30 mg/d。随访期间根据患者情况调整补钾剂量或逐渐停用补钾药物。
主要终点:治疗4周时无需补钾且血钾水平恢复正常的患者比例。次要终点:血清钾、24小时尿钾、收缩压(SBP)、舒张压(DBP)的变化。安全性指标:血清肌酐、eGFR、血尿酸、血清钠水平及高钾血症发生率等。
三、研究结果
(一)基线特征
15例患者中男性占67%,平均年龄57岁,平均体重指数(BMI)28.46 kg/m2;基线SBP 148.13 mmHg,DBP 92.73 mmHg;血清钾2.99 mmol/L,均为低钾血症;eGFR 95.95 ml/min/1.73m2;血浆醛固酮浓度29.00 ng/dL,血浆肾素浓度1.60 μIU/mL;24小时尿钾平均为69.00 mg/24h。
(二)主要终点
治疗4周时,15例患者中有8例无需补钾治疗,其中7例(47%)血清钾维持在正常范围,1例仍存在轻度低钾血症。其余7例仍需少量补钾。治疗8周时(12例完成随访),6/15例(40%)患者仅通过非奈利酮治疗维持血清钾正常(图1)。
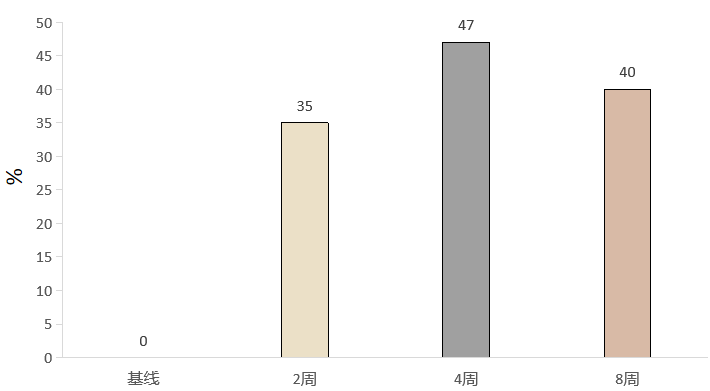
图1. 随访期间无需补钾即可使血钾水平恢复正常的患者比例
(三)次要终点
治疗期间,血清钾水平呈现显著变化:2周、4周、8周时血清钾水平均较基线显著升高(P<0.05,图2A),平均升高幅度分别为0.98 mmol/L、0.79 mmol/L、0.73 mmol/L(图2B)。血清钾水平在2周时达到峰值,之后略有下降但无统计学意义。随访期间24小时尿钾与基线相比无显著变化(图2C)。
按CKD状态分层分析显示,无论是否合并CKD,患者血清钾水平均较基线显著升高(P<0.05);其中无CKD患者8周时血清钾水平显著低于2周、4周(P<0.05),提示无CKD患者可能需要更密切的血钾监测及剂量调整(图3)。
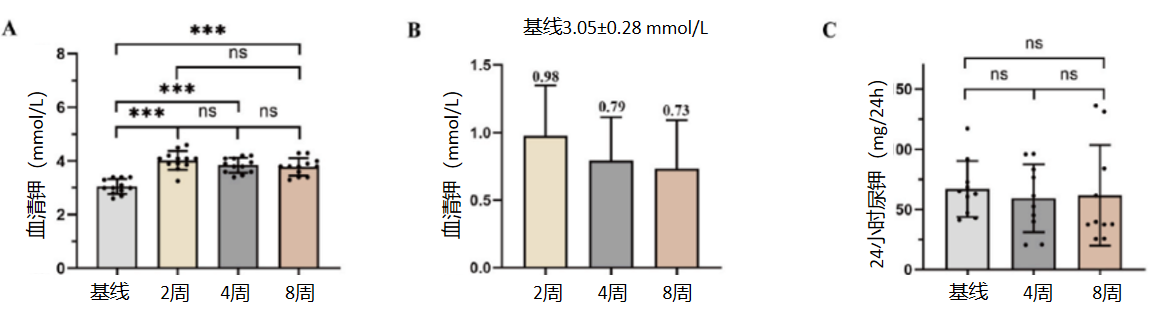
图2. 血清钾、24小时尿钾的变化***:P<0.001;ns:无显著差异,P>0.05.
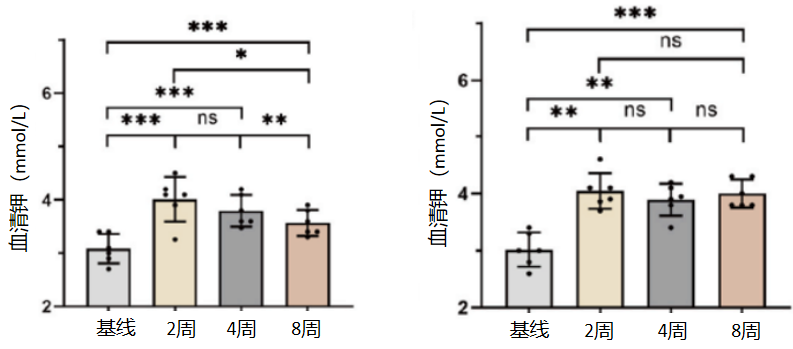
图3. 未合并CKD(左)、合并CKD(右)的患者血清钾变化*:P<0.05;**:P<0.01;***:P< 0.001;ns:无显著差异,P>0.05.
15例患者中,10例在治疗期间未增加降压药物种类或减少剂量(2例减少降压药剂量,8例维持原有剂量)。对该部分患者的血压分析显示,SBP在治疗4周、8周时较基线显著下降(P<0.05,图4A),平均降幅分别为13.0 mmHg、15.0 mmHg;2周时SBP较基线下降10.3 mmHg,但差异无统计学意义(P>0.05,图4B)。与2周时相比,4周、8周时SBP进一步下降,平均降幅分别为2.8 mmHg、4.6 mmHg(图4C)。DBP在治疗各时间点与基线相比均无显著变化。
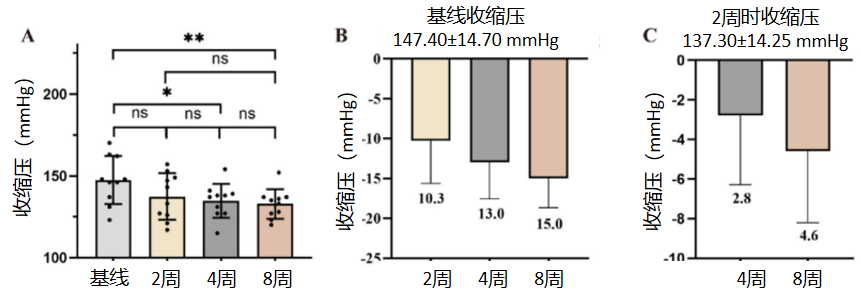
图4. 在治疗期间未增加降压药物种类或减少降压药剂量的10例患者的血压变化*:P<0.05;**:P< 0.01;ns:无显著差异,P>0.05.
(四)安全性指标
随访期间未出现高钾血症、低钠血症等不良事件。合并CKD的患者治疗4周、8周时血清肌酐略有升高,eGFR略有下降(短期下降与非奈利酮已知的药理特性一致,通常不反映肾脏实质性损伤),但均无统计学意义(P>0.05);非CKD的患者血清肌酐和eGFR变化趋势与整体一致,也未出现显著异常。
(五)其他指标
治疗4周时,血浆肾素浓度较基线显著升高,血浆醛固酮浓度无显著变化。
四、研究结论
非奈利酮能有效升高低钾血症PA患者的血清钾水平,且在不增加其他降压药种类和剂量的情况下可降低收缩压,治疗期间未出现高钾血症等严重不良反应,安全性良好,具有治疗PA的潜力。
专家点评
(一)非奈利酮对PA患者低钾血症的纠正作用
低钾血症可引起PA患者靶器官损伤,纠正低钾血症是PA药物治疗的重要目标之一。目前,药物治疗是双侧肾上腺增生或不适合手术的PA患者的主要治疗方式,MRAs是常用药物[2]。既往临床常用的甾体类MRAs螺内酯虽疗效明确,但易引发性激素相关副作用(如男性乳房发育、女性月经紊乱),限制了其临床应用。因此,临床亟需探索更安全、有效的新型治疗药物。
非奈利酮作为新一代ns-MRA,为PA的治疗带来新选择。本研究显示,非奈利酮能有效升高低钾血症PA患者的血清钾水平,所有患者的血清钾水平均较基线显著升高,治疗4周时47%的患者无需补钾即可维持血清钾正常,8周时仍有40%的患者仅靠非奈利酮治疗保持血钾正常,证实了非奈利酮纠正低钾血症PA患者血钾的有效性。
(二)非奈利酮对PA患者血压的影响
高血压是PA患者最常见的临床表现,也是导致靶器官损伤的主要危险因素,有效控制血压是PA治疗的另一目标。本研究显示,非奈利酮能显著降低低钾血症PA患者的收缩压,在未增加降压药或减少剂量的患者中,4周、8周时收缩压较基线分别显著下降13.0 mmHg、15.0 mmHg。这一结果与国际知名期刊Circulation发表的CONPASS研究结论相互印证——该研究显示非奈利酮可降低PA患者日间SBP 9.9 mmHg、24小时SBP 10.9 mmHg[3],充分证实了其降压疗效的一致性。
非奈利酮的降压机制源于:通过阻断醛固酮介导的水钠潴留,减少血容量,同时抑制醛固酮对血管平滑肌的促纤维化作用,改善血管弹性,从而降低血压。目前正在开展的为期12周、多中心、随机纳入306例患者的FAIRY研究(NCT06457074),将进一步明确非奈利酮在PA血压管理中的定位,为其拓展应用提供更坚实的证据支持。
(三)非奈利酮的安全性与肾功能影响
与传统MRAs相比,非奈利酮纠正低钾血症的优势不仅在于疗效,更在于安全性。螺内酯治疗PA时,剂量依赖性副作用(内分泌紊乱)发生率高达52%~63%[4,5];为避免高钾血症的发生,肾功能不全CKD 3期[GFR<60 ml/(min·1.73㎡)]患者慎用,肾功能不全4期及4期以上禁止服用[GFR<30 ml/(min·1.73㎡)][2]。而本研究中,低钾血症的PA患者无高钾血症发生,即使合并CKD的患者也未出现肾功能恶化或严重电解质紊乱。对于治疗初期血清肌酐轻微升高、eGFR轻微下降的现象,结合PA患者长期高醛固酮导致的肾脏“高滤过”状态,这一变化更可能是药物有效阻断MR作用的标志,而非肾脏损伤,临床无需过度担忧,但需长期监测肾功能变化。
非奈利酮的安全性优势可从三方面得到解释:一是非甾体立体结构使其高选择性作用于MR,避免了传统甾体类MRA对性激素受体的影响,规避了相关内分泌紊乱和高钾血症风险[6,7];二是药物在心脏和肾脏组织中分布较为均衡[8],而螺内酯在肾脏中的浓度更高,从而导致肾脏相关不良反应风险增加;三是螺内酯在体内的代谢产物仍具有MR拮抗的药物活性,而非奈利酮不具有活性代谢产物,避免了代谢产物蓄积带来的潜在风险[9,10]。
尽管本研究具有重要价值,但仍存在一定局限性:样本量较小(n=15),且为单中心单臂研究,缺乏对照组,可能导致结果存在偏倚,相关研究结论需要进一步验证;血压测量采用诊室血压而非24小时动态血压监测,再者多种降压药物的联合使用使非奈利酮对收缩压的降压效果解读变得复杂,因此未来研究需进一步专门评估非奈利酮对PA患者血压的影响;未进行肾上腺静脉采血(AVS)分型,无法分析不同PA亚型对非奈利酮的治疗反应差异;随访时间较短(8周),无法评估非奈利酮的长期疗效与安全性。这些局限性为未来研究指明了方向。
总体而言,本研究为低钾血症PA治疗提供了新的思路和证据,非奈利酮凭借其疗效与安全性优势,有望在PA治疗领域占据重要地位,未来随着更多临床研究的开展,其临床价值将得到进一步明确,为PA患者带来更优质的治疗选择。
专家简介

教授,主任医师,博士生导师,天津市特聘教授。
天津医科大学总医院内分泌代谢科主任,内科教研室和规培基地主任。
中华内分泌学会 副主任委员。
中国医师协会内分泌代谢医师分会 常委 兼内分泌罕见病学组组长。
天津市糖尿病学会 主任委员。
研究方向:胰岛功能和糖尿病发病机制、单基因糖尿病、垂体肾上腺疾病。
主持国际项目6项,基金委重点和科技部重点研发课题6项。牵头开展全国多中心临床研究20余项。
在JCI, PNAS, Science Advances, Nature Communications等发表SCI论文180余篇,天津市科技进步一等奖。
参考文献
1.Li S, et al. Diabetes Metab Syndr . 2025 Dec 27; 20(1): 103369. doi: 10.1016/j.dsx.2025.103369. Online ahead of print.
2.中华医学会内分泌学分会. 中华内分泌代谢杂志. 2025; 41(01): 12-24.
3.Hu J, et al. Circulation. 2025; 151: 196-198.
4.Huffman DH, et al. Clin Pharmacol Ther. 1978; 24: 465-73.
5.Pech`ere-Bertschi A, et al. Ann Endocrinol (Paris). 2016; 77: 226-34.
6.万瑾瑾,等. 医药导报. 2022; 41(10): 1486-1490.
7.李航.中华内科杂志. 2021; 60 (1): 5-8.
8.Kolkhof P, et al. J Cardiovasc Pharmacol. 2014; 64: 69-78.
9.许丹华, 等. 中国临床药理学杂志. 2009; 25 (03): 227-230.
10.可申达®说明书
2 comments








 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言