糖尿病周围神经病理性疼痛(DPNP)严重困扰众多糖尿病患者,其发病机制复杂,治疗极具挑战性。日益增多的证据表明,神经系统的微循环障碍在DPNP的发生发展中也起重要作用,改善微循环应作为治疗的核心靶点之一。在中华医学会糖尿病学分会第二十七次学术会议(CDS 2025)上,复旦大学附属华山医院内分泌科李益明教授系统阐述了DPNP的流行病学特征、微循环障碍的核心作用机制及多维度治疗策略,为临床实践提供了重要参考。

一、DPNP:糖尿病最常见的“隐匿性”并发症
糖尿病周围神经病理性疼痛(diabetic peripheral neuropathic pain, DPNP)是指糖尿病患者因躯体感觉神经系统损伤导致的疼痛,其中远端对称性多发性神经病变(DSPN)是其最常见的原因(占比超过95%)。作为糖尿病最常见的慢性并发症之一,DPNP的流行病学数据令人担忧:国际研究显示在糖尿病患者中患病率高达10%~26%[1],我国糖尿病患者中DPNP发生率约为16%,据此推算国内约有2200万患者受其困扰[2]。更值得关注的是,临床中12.5%的DPNP患者未被诊断,39%确诊患者未接受规范治疗[3],凸显出DPNP认知与管理的严峻现状。
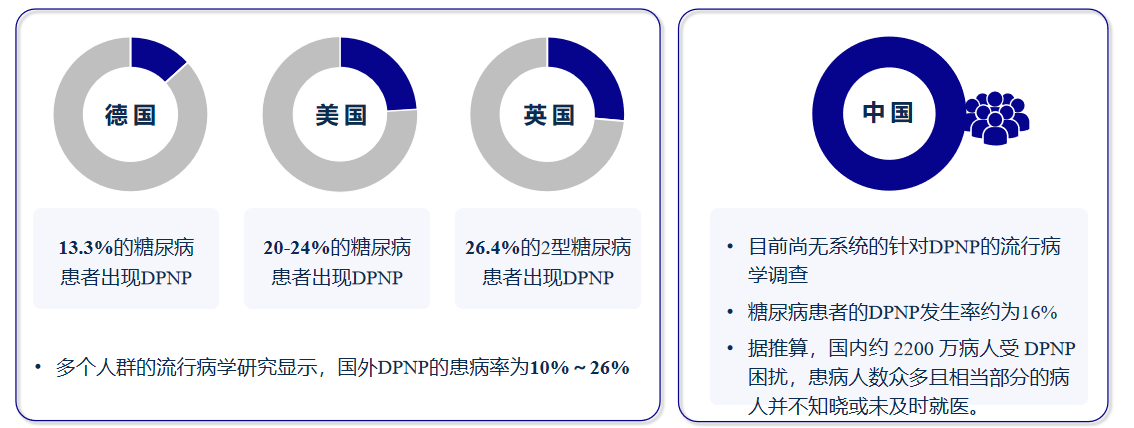
图1. 不同国家DPNP的发生率
DPNP的临床表现以麻木、刺痛、针刺痛和灼热感最为常见,超过70%的患者表现为中至重度持续疼痛。疼痛不仅导致患者生活质量显著下降,还引发一系列连锁问题。一项研究显示,65%的DPNP患者因疼痛丧失工作能力或工作效率下降,72%存在睡眠障碍,53%合并抑郁,62%出现焦虑症状[4]。毋庸置疑的是,DPNP已成为影响糖尿病患者生活质量的主要因素,但其临床重视程度仍显不足,亟需提升诊疗规范化水平。
二、DPNP的复杂机制:多系统交互作用的结果
DPNP的发病机制错综复杂,包括神经系统的外周敏化、中枢敏化、下行抑制系统的失能、离子通道的改变等,并且多种机制互相影响(图1)。中枢层面,脊髓及以上痛觉相关神经元兴奋性异常升高、突触传递增强,直接放大痛觉信号的传导;同时脑干主导的下行抑制系统功能降低,对脊髓痛觉信息的抑制性调控减弱,进一步让痛觉信号被放大,引发疼痛等表现。外周层面,组织损伤后,降钙素基因相关肽等物质增多,叠加离子通道(如钙离子通道、钠离子通道)的异常改变,使伤害感受器呈持续超敏状态,神经冲动过度放大,最终经中枢机制的协同作用,引发痛觉过敏。
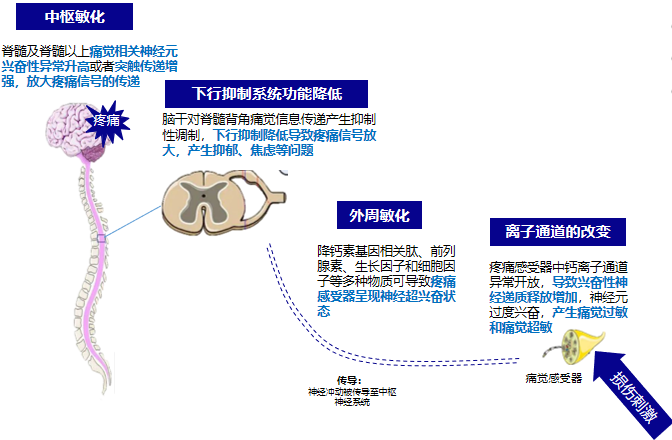
图2. DPNP形成的多机制交互作用
三、微循环障碍:DPNP的核心病理生理基础
01、DPNP患者微循环异常的临床证据
多项研究证实DPNP患者存在显著的神经系统的微循环结构与功能异常。早在1993年,腓肠神经外膜血管活体观察显示,糖尿病神经病变患者存在静脉扩张、动脉变细及动静脉分流迂曲等改变,而糖尿病无神经病变患者仅表现为动脉变细[5]。激光多普勒技术进一步揭示,糖尿病神经病理性疼痛患者存在微血管内皮功能障碍和交感神经反应性下降,微血管舒张和收缩受损导致局部血流调节不当可能在糖尿病神经病变疼痛的发病机制中起重要作用[6]。血清学标志物检测为微循环障碍提供了进一步证据。DPNP患者血清可溶性细胞间黏附分子(sICAM)水平显著升高,且高于无痛性神经病变患者,提示血管内皮损伤和炎症激活[7]。这些多维度证据共同证实,微循环障碍是DPNP的重要病理特征。
02、微循环障碍导致DPNP的关键机制
微循环障碍诱发DPNP存在四条关键通路:首先,长期高血糖导致微血管基膜增厚、周细胞缺失及内皮细胞增生导致血-神经屏障(BNB)破坏(图3),使炎症因子侵入神经内膜,引发神经炎症和缺氧;其次,缺血缺氧导致神经元ATP合成减少,抑制轴突运输,引起轴突变性;第三,微循环障碍激活多元醇通路,果糖和山梨醇蓄积导致神经元渗透压升高、肌醇摄入减少,进一步加重轴突损伤;最后,脊髓微血管内皮细胞凋亡导致脊髓微循环障碍,诱发中枢神经元过度激活,形成中枢敏化。
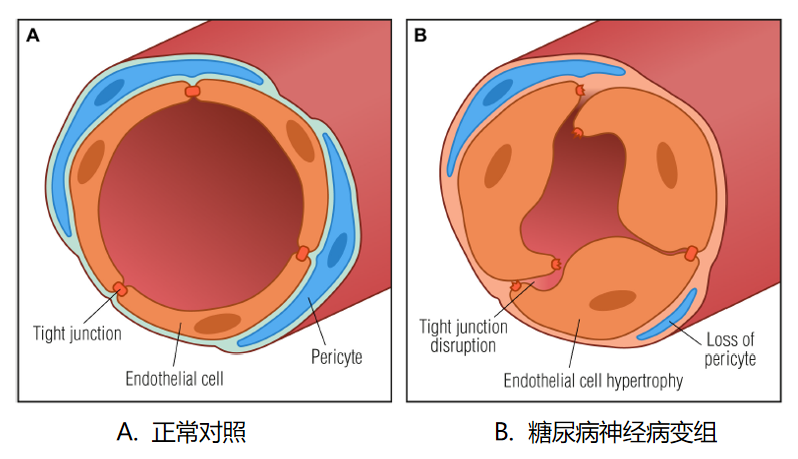
图3. DPNP存在血-神经屏障受损
中医理论对DPNP的认识与现代医学研究高度契合。明代李中梓在《医宗必读·心腹诸痛》中提出“通则不痛,痛则不通”的病机理论,DPNP属“气虚血瘀、阴虚血瘀”范畴,迁延不愈可发展为“痰瘀互结”,痹阻脉络而致疼痛。这种“血瘀致痛”的理论与现代医学中的微循环障碍机制异曲同工,为中西医结合治疗提供了理论基础。
四、微循环评估:DPNP诊断的“新维度”
鉴于微循环障碍在DPNP中的核心作用,应将微循环评估纳入DPNP常规诊断路径。目前临床常用的评估方法包括无创和有创两类。无创评估技术因其安全性和可重复性,更适合临床常规应用,而有创检查主要用于科研或疑难病例诊断。
(1)无创评估技术:经皮氧分压(TcPO2)监测可无创评估局部组织氧供,反映微循环灌注状态。激光多普勒血流仪(LDF)通过检测红细胞运动速度评估皮肤微血管血流,结合乙酰胆碱(Ach)和硝普钠(SNP)离子导入试验,可分别评估内皮依赖性和非内皮依赖性血管舒张功能;深吸气试验则用于评估交感神经介导的血管收缩功能,是反映神经-血管调节的重要指标。
(2)有创评估技术:皮肤活检可定量检测表皮内神经纤维密度(IENFD)和微血管密度,两者均与DPNP严重程度显著相关。
五、改善微循环:DPNP治疗的经典策略
01、经典改善微循环药物
《糖尿病神经病变诊治专家共识(2021年版)》将改善微循环药物列为DPNP治疗之一(表1)。其中,前列腺素E及其类似物(如贝前列腺素钠)通过增加血管平滑肌细胞cAMP含量,舒张血管平滑肌、降低血液黏度,从而改善微循环。己酮可可碱通过升高cAMP水平扩张血管,同时具有抗炎、抑制血小板聚集作用;胰激肽原酶则通过激活纤溶酶、降低血液黏度改善组织灌注。外源性补充VEGF-A165b,可以阻止内皮细胞死亡,恢复脊髓微血管结构和功能,减少神经元激活标志物(c-Fos),预防机械/热痛觉过敏。
表1. 改善微循环的常见药物和作用机制
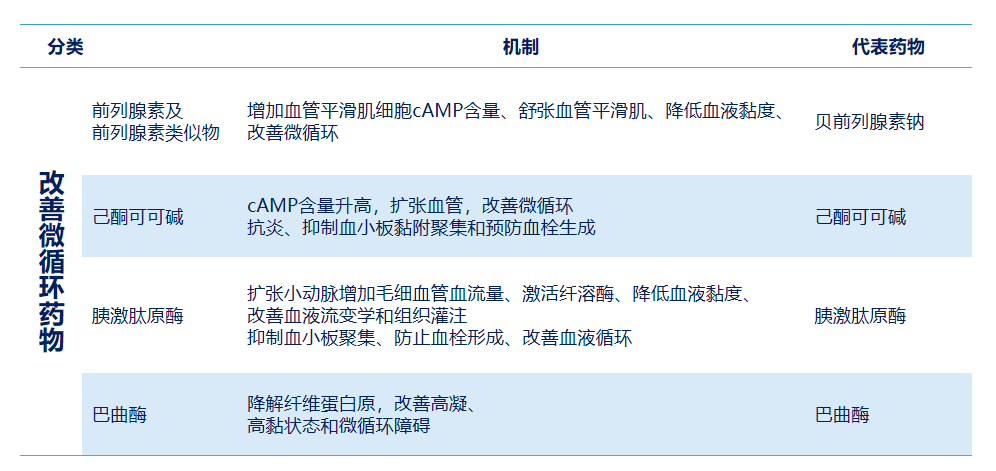
02、脊髓电刺激(SCS):微创介入治疗新选择
脊髓电刺激(SCS)作为一种微创介入治疗技术,通过双重机制改善微循环:一方面抑制中枢交感神经活性,减少交感性血管收缩;另一方面逆向激活感觉纤维,释放血管舒张因子。在血管痉挛和严重缺血状态下,这两种机制协同作用,有效改善局部血流灌注。荟萃分析显示,SCS治疗可使59%~66.4%的DPNP患者疼痛缓解≥50%,显著优于药物治疗(5%~11.7%)[9]。
另一项随访5年的前瞻性研究进一步证实SCS的长期疗效:治疗5年后,患者疼痛缓解率仍达55%,80%的患者持续使用SCS治疗;治疗期间,患者白天和夜晚疼痛数字评分(NRS)均较基线显著降低,生活质量持续改善[10]。SCS为药物治疗无效的难治性DPNP患者提供了新选择,但因其价格高及有创,其临床应用需严格把握适应证。
03、中医药治疗:活血化瘀通络
中医药在DPNP治疗中具有独特优势。活血化瘀中药通过“通络活血”改善微循环而起效。临床研究显示,在基础治疗上加用活血化瘀中药可以显著改善患者多伦多神经病变评分(TCSS)从10.80±2.36降至8.52±2.48,视觉模拟评分(VAS)从4.12±1.46降至3.20±1.20,均显著优于硫辛酸对照组(P<0.05)[11]。中西医结合治疗可发挥协同作用,为DPNP患者提供更多治疗选择,但需进一步开展高质量临床研究证实其疗效并探索机制。
结语
DPNP严重威胁着糖尿病患者的生活质量,而微循环障碍构成了其核心的病理生理基础。在临床实践中,应提高对DPNP的认识,高度重视微循环评估,并将其纳入常规诊断路径;同时,将改善微循环作为治疗的关键策略。现有证据显示,前列腺素E类药物、脊髓电刺激以及活血化瘀中药等多种方法,通过改善微循环,能有效缓解疼痛并延缓疾病进展。未来,随着对微循环障碍机制的深入理解及新型治疗技术的进步,DPNP的诊疗水平将不断提升,从而为患者带来更多益处。
参考文献
1.糖尿病性周围神经病理性疼痛诊疗专家共识[J].中国疼痛医学杂志,2018,24(08):561-567.
2.周围神经病理性疼痛诊疗中国专家共识[J]. 中国疼痛医学杂志,2020,26(5):321-328.
3.中华医学会糖尿病学分会神经并发症学组, 等. 中华糖尿病杂志. 2021, 13(6): 540-555.
4.Zhang Y, et al. Pain Ther. 2021, 10: 1355-1373.
5.Diabetologia(1993) 36;1266-1274.
6.Diabetes Care 30:655–659, 2007.
7.J Clin Endocrinol Metab. 2009,10;94(6):2157-2163
8.糖尿病周围神经病变中医诊疗规范初稿[J].中华中医药杂志,2010,25(02):260-264.
9. Diabetes 2023;72(Supplement_1):493-P
10.Diabetes Care. 2018 Jan;41(1):32-38
11.参蝎止痛胶囊治疗糖尿病周围神经病变的临床疗效观察[J].西部中医药,2021,34(08):6-10.
2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言