COMBINE 4研究全球首次公布,彰显我国糖尿病研发贡献及国际影响力提升。
首个中国人群数据公布,证实IcoSema在中国T2DM患者中兼具有效性和安全性。
为帮助临床医生更好地了解相关进展,本刊对西北大学附属国际医学中心医院姬秋和教授和北京大学人民医院纪立农教授进行专访,从降糖药物研发创新出发,深入解读IcoSema最新研究数据。
一、降糖药物的研发创新:多维度考量下,创新联合制剂研发取得重要进展
降糖药物研发创新:需从多维度进行综合考量
不同机制药物联合治疗是T2DM管理的重要策略之一。姬秋和教授指出,创新性降糖药物的研发需从疾病、患者、监管等多维度进行综合考虑,主要聚焦于以下三个方面:
针对疾病发病机制:T2DM发病机制复杂,目前已知涉及12种病理生理缺陷(即“12恶源”)、甚至更多[1]。降糖药物研发需针对疾病发病机制,不同机制药物联合可覆盖T2DM多重病理生理机制,带来更佳临床获益[2-4]。目前,联合制剂在临床中应用广泛,例如在美国食品药品监督管理局(FDA)批准的降糖药中,其占比近40%[5]。
简化治疗方案:从患者角度,希望尽量减少用药频次,降低治疗负担,降糖药物的研发创新需要以患者为中心,尽量简化治疗方案。降糖药物周制剂显著减少用药次数,有助于改善治疗依从性和患者满意度[6-9]。
超越降糖的获益:良好的血糖控制效果固然重要,但仍不够。国内外监管部门提倡降糖药物的研发应从多维度评估临床结局,例如对胰岛素治疗的评估除糖化血红蛋白(HbA1c)外,还要关注胰岛素剂量减少、体重改变和低血糖事件减少等相关指标。
创新联合制剂研发的重大进展:全球首个基础胰岛素/GLP-1RA周制剂
姬秋和教授介绍,基础胰岛素和GLP-1RA机制互补,首个基础胰岛素周制剂依柯胰岛素和以司美格鲁肽为代表的GLP-1RA周制剂成功上市,为创新联合周制剂的进一步创新研发提供可能。IcoSema是首个基础胰岛素/GLP-1RA周制剂,实现依柯胰岛素和司美格鲁肽的创新联合。1剂量单位IcoSema包含1 U依柯胰岛素和0.0029 mg司美格鲁肽,每周最大剂量为350剂量单位(即350 U依柯胰岛素和1 mg司美格鲁肽)。在3a期临床试验中,IcoSema以每周40剂量单位起始,剂量调整简单方便,根据空腹血糖(FPG),每周调整10剂量单位(图1)[10-12]。
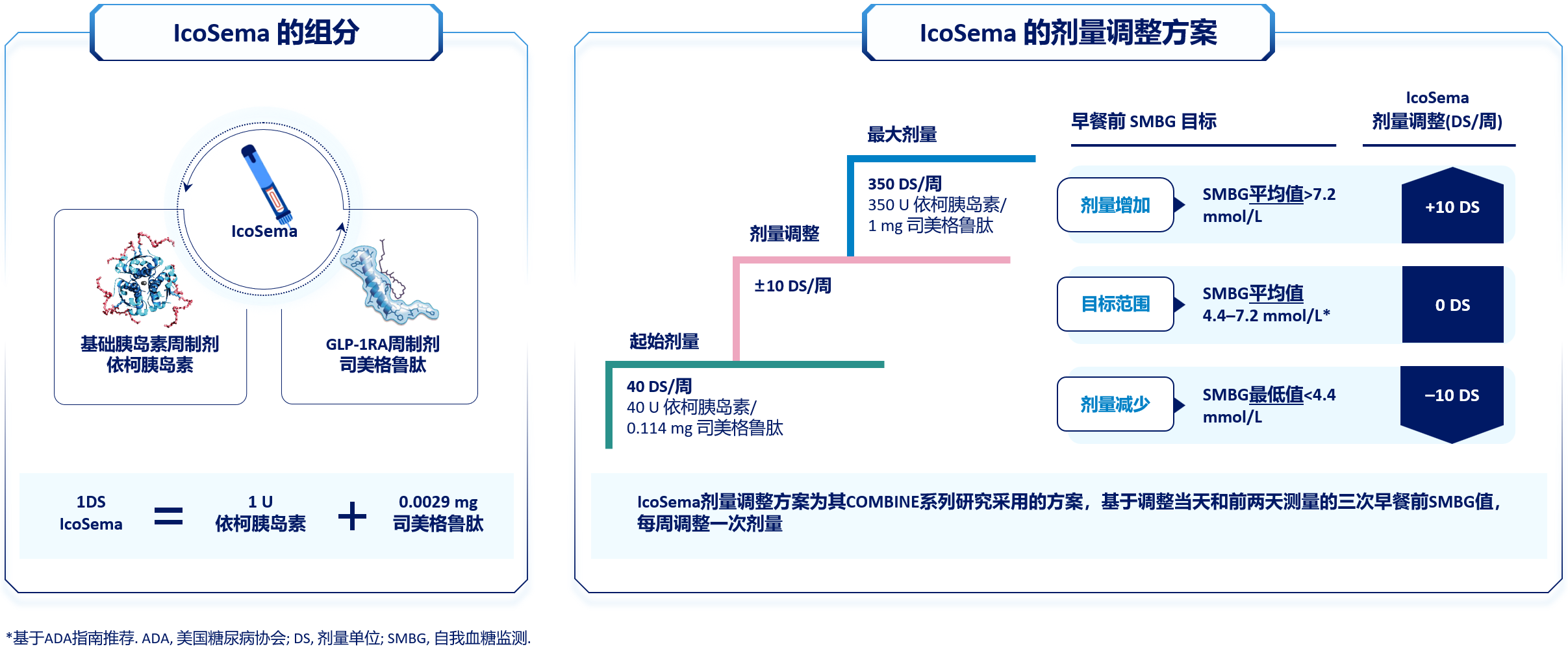
图1. IcoSema的组分和剂量调整方案
IcoSema每周注射一次,即可实现基础胰岛素与GLP-1RA的联合治疗。与基础胰岛素日制剂(每年365次注射)以及基础-餐时胰岛素方案(每年高达1460次注射)相比,IcoSema每年仅需52次注射,显著减轻注射负担,有助于提高治疗依从性和满意度。
因此,从疾病、患者和监管维度来看,IcoSema覆盖多重病理生理机制,简化治疗方案,在全球3期临床研究的不同治疗背景人群中,评估了多维度的临床终点,其研发契合创新降糖药物研发的综合考量维度(图2)。
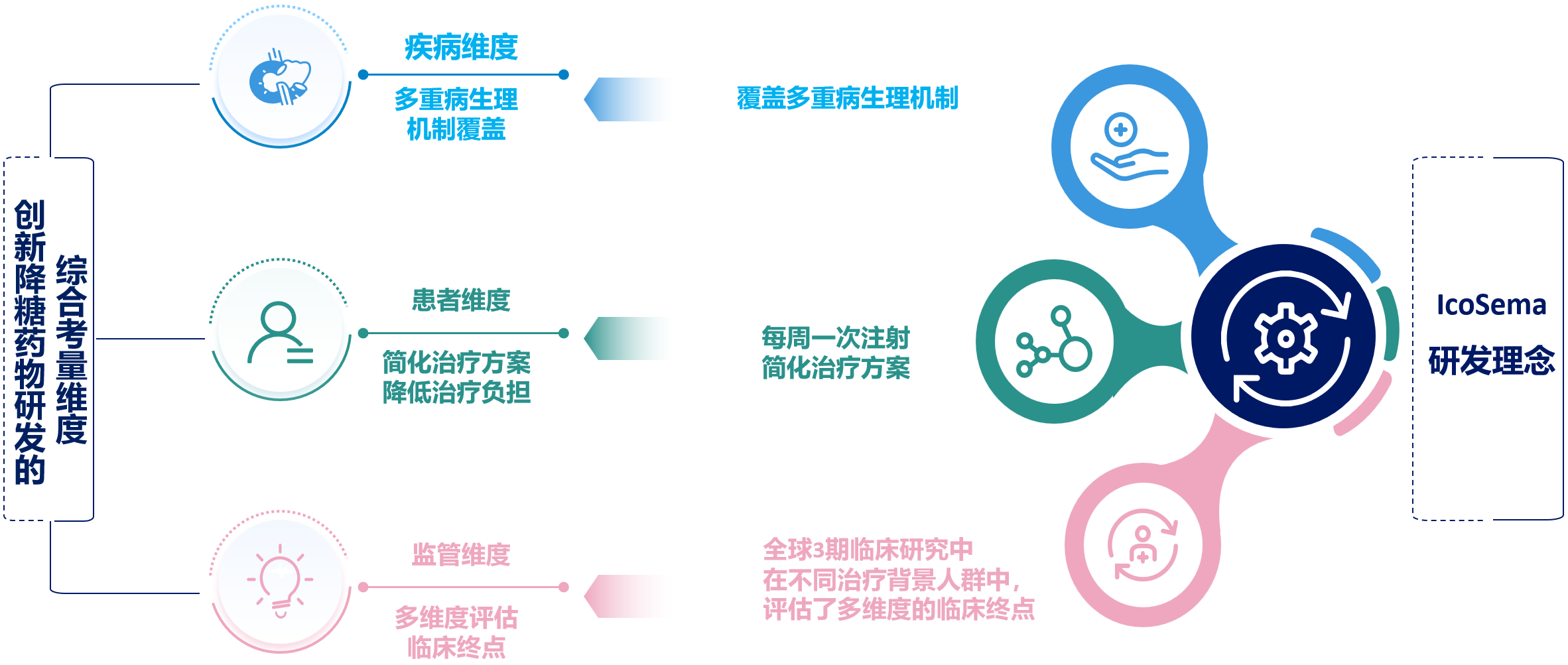
图2. IcoSema的研发契合创新药物研发的多维度考量
二、COMBINE系列研究进展:IcoSema为不同治疗背景T2DM患者带来多重获益
COMBINE 1~3研究回顾:既往使用基础胰岛素日制剂或GLP-1RA的T2DM患者,转换为IcoSema治疗可强效降糖且安全便捷
COMBINE系列研究是IcoSema的3期临床试验,在全球和中国同步开展,纪立农教授作为全球主要研究者之一,对相关进展进行了详细介绍。COMBINE系列研究评估IcoSema在既往不同治疗背景T2DM患者中的疗效和安全性,其中3a期临床试验包括COMBINE 1~3,均已完成且正式发表[10-12]。结果证实(图3):
对于既往使用基础胰岛素日制剂血糖控制不佳的T2DM患者(COMBINE 1和3研究):相较基础胰岛素周制剂或基础-餐时胰岛素方案,IcoSema降低HbA1c效果更优(相较基础胰岛素周制剂)或相似(相较基础-餐时胰岛素方案),有临床意义或严重低血糖风险显著降低,体重获益显著(组间体重变化差异达5.59~6.72 kg),每周胰岛素剂量减少近半[10,12]。
对于既往使用GLP-1RA血糖控制不佳的T2DM患者(COMBINE 2研究):相较GLP-1RA周制剂,IcoSema降低HbA1c效果更优,有临床意义或严重低血糖风险相似,HbA1c达标率显著更高[11]。
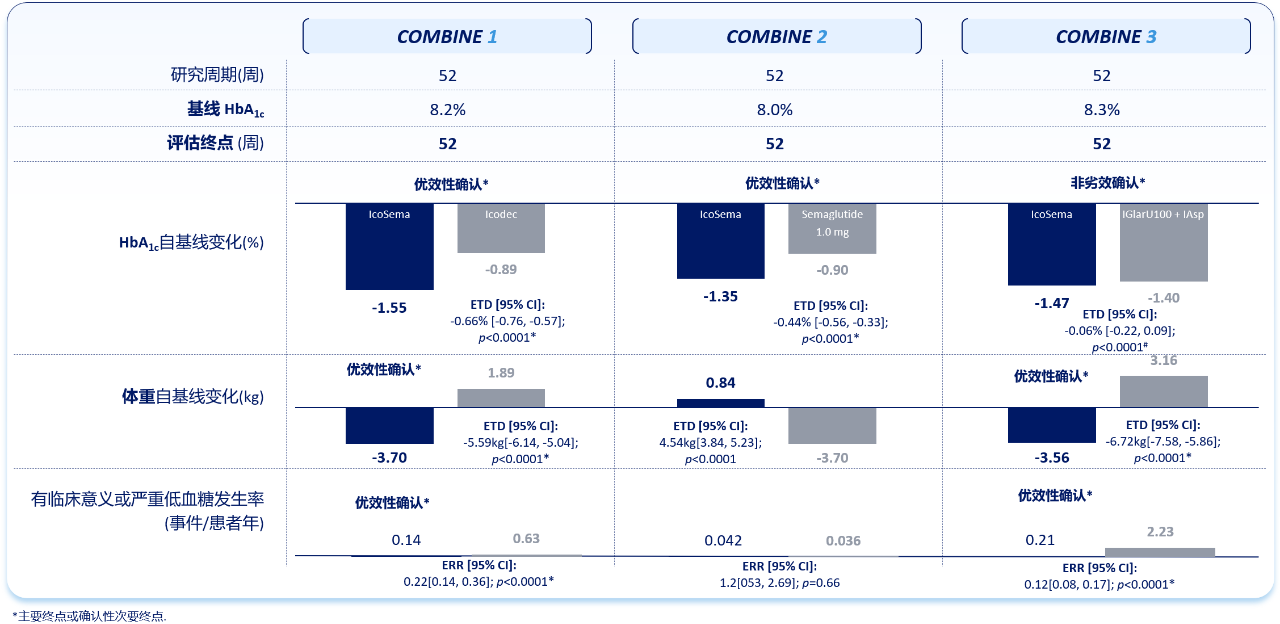
图3. IcoSema 3a期临床研究主要结果概览
COMBINE 4研究重磅首发:既往OAD治疗血糖控制不佳的T2DM患者,起始IcoSema治疗在血糖控制、体重获益和低血糖风险上,均优于甘精胰岛素U100
COMBINE 4是IcoSema的3b期临床试验,旨在口服降糖药(OAD)治疗血糖控制不佳的T2DM患者中,评估每周一次IcoSema相较于每日一次甘精胰岛素U100的疗效和安全性。纪立农教授代表研究团队在本次CDS会议上首次公布其研究结果,这也是COMBINE系列研究结果首次选择在中国进行全球首发。
COMBINE 4研究是在9个国家(含中国)开展的开放、治疗达标试验,共纳入485例使用过1~3种OAD、未使用过胰岛素的成人T2DM患者(HbA1c≥8%),1:1随机分为IcoSema组(n=243)和甘精胰岛素U100组(n=242),治疗40周,之后再随访5周。研究根据更严格的FPG滴定目标(3.9~5.0 mmol/L),调整IcoSema和甘精胰岛素U100的剂量。主要终点是从基线至第40周的HbA1c变化;确证性次要终点是从基线至第40周的体重变化。其他次要终点包括第36~40周葡萄糖目标范围内时间(TIR3.9~10.0mmol/L)、第38~40周基础胰岛素周剂量、从基线至第45周有临床意义或严重低血糖的发生率。
结果显示,从降糖疗效到安全性,IcoSema在多维指标上均优于甘精胰岛素U100(图4):
主要终点确证优效性:IcoSema组HbA1c从基线(9.57%)至第40周的变化为-3.32%,优效于甘精胰岛素U100组从基线(9.50%)的降幅-2.44%[估计治疗差异(ETD):-0.88%,95%CI:-1.12~-0.63,优效性P<0.0001]。
体重变化确证优效性:IcoSema组从基线至第40周的体重变化为-0.79 kg,优效于甘精胰岛素U100组的+3.81 kg(ETD:-4.61 kg,95%CI:-5.46~-3.75,优效性P<0.0001)。
TIR显著改善:IcoSema组第36~40周TIR3.9~10.0mmol/L显著更高(79.8% vs. 64.5%,ETD:13.3%,95%CI:9.46~17.2,P<0.0001)。
基础胰岛素周剂量显著减少:IcoSema组第38~40周基础胰岛素周剂量显著更低(ETD:-126 U,95%CI:-154~-98,P<0.0001)。
低血糖风险显著降低:IcoSema组有临床意义或严重低血糖的发生率显著更低(0.29 vs. 0.59事件/患者年,估计率比0.56,95%CI:0.32~0.97,P=0.0381)。
HbA1c达标率及复合达标率显著提高:第40周时,IcoSema组HbA1c<7.0%、HbA1c<7.0%且无体重增加和不伴有临床意义或严重低血糖的达标率均显著更高(分别为80.0% vs. 49.5%、43.1% vs. 8.9%,均P<0.0001)。
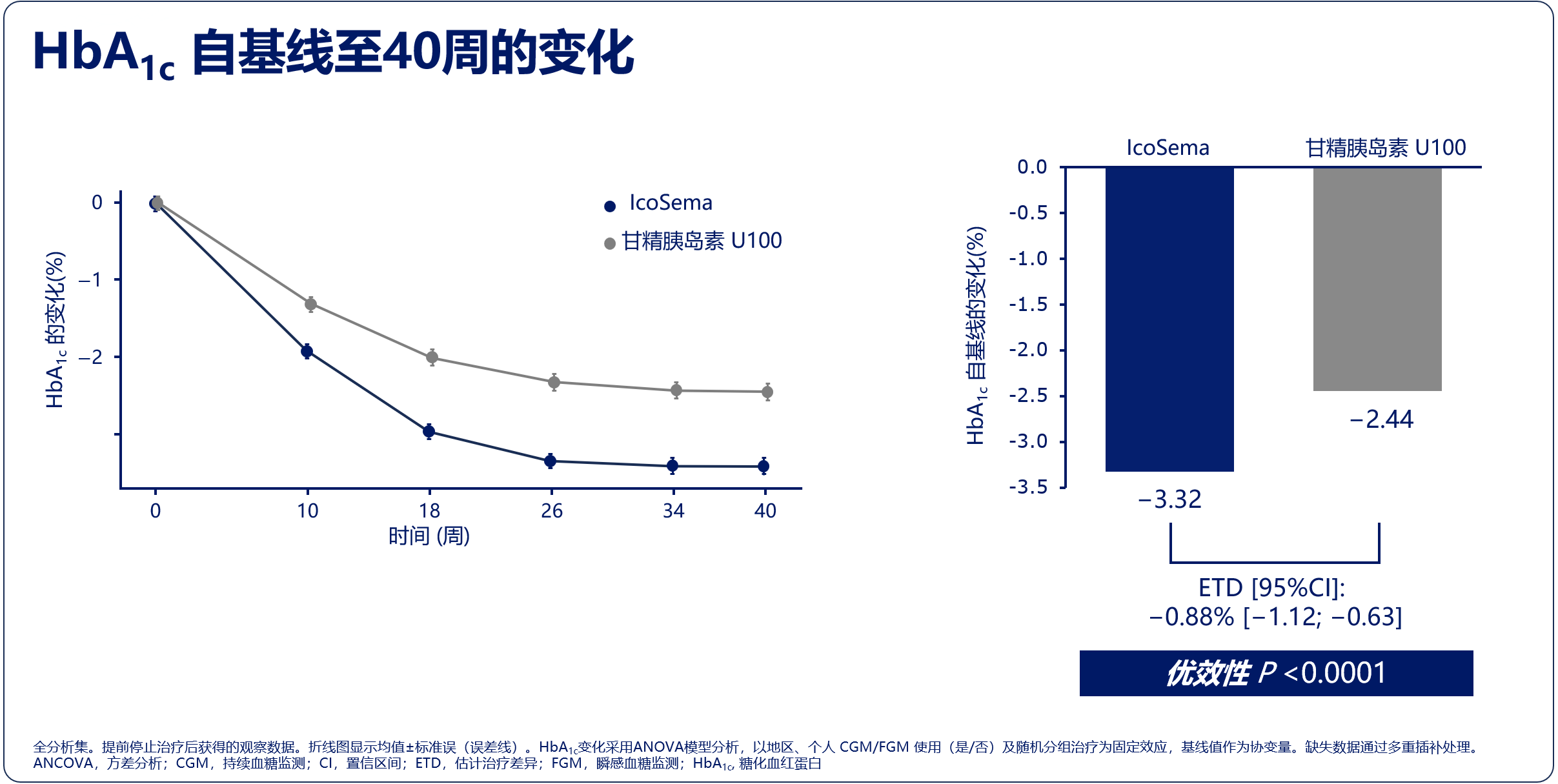
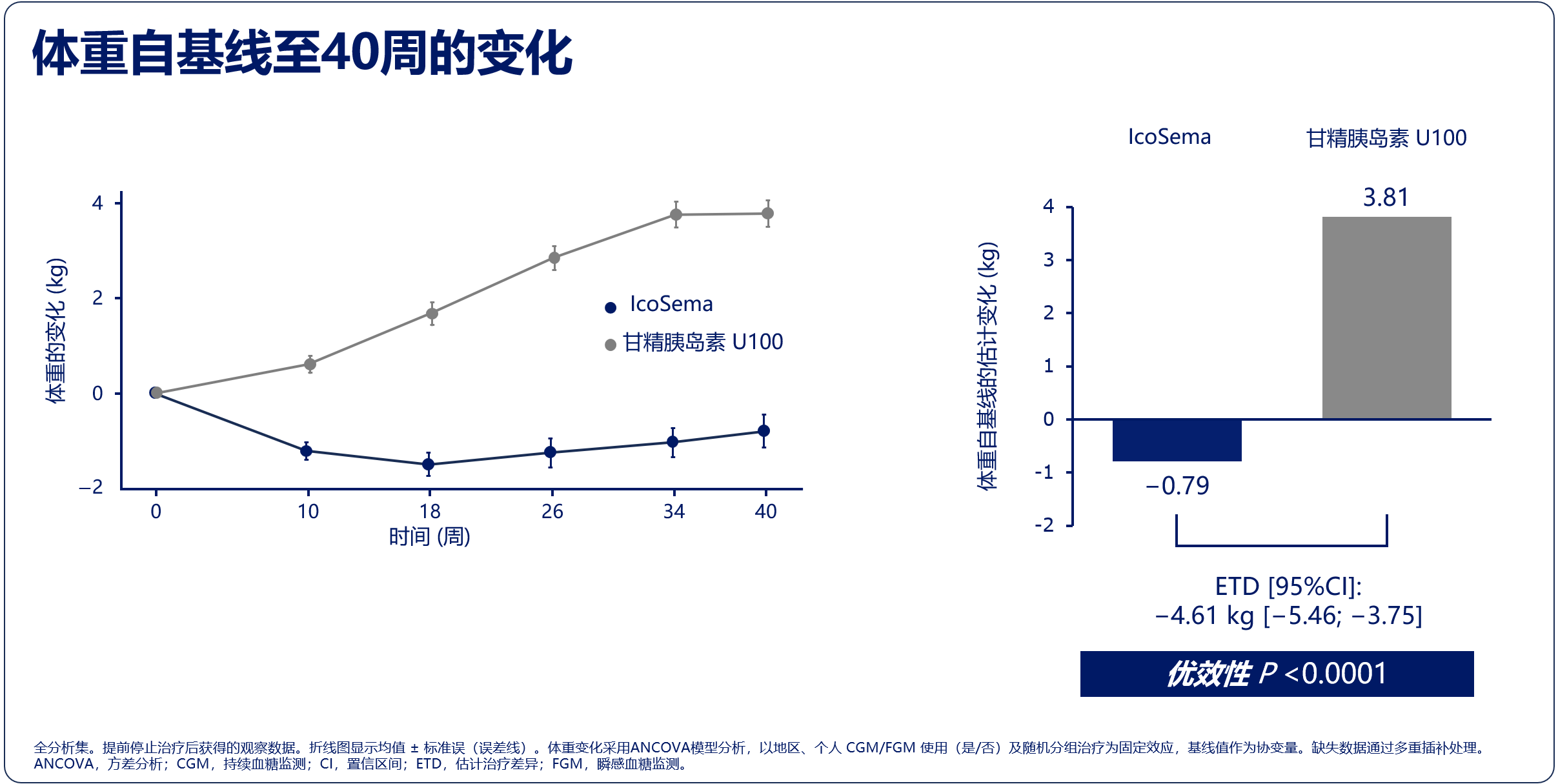
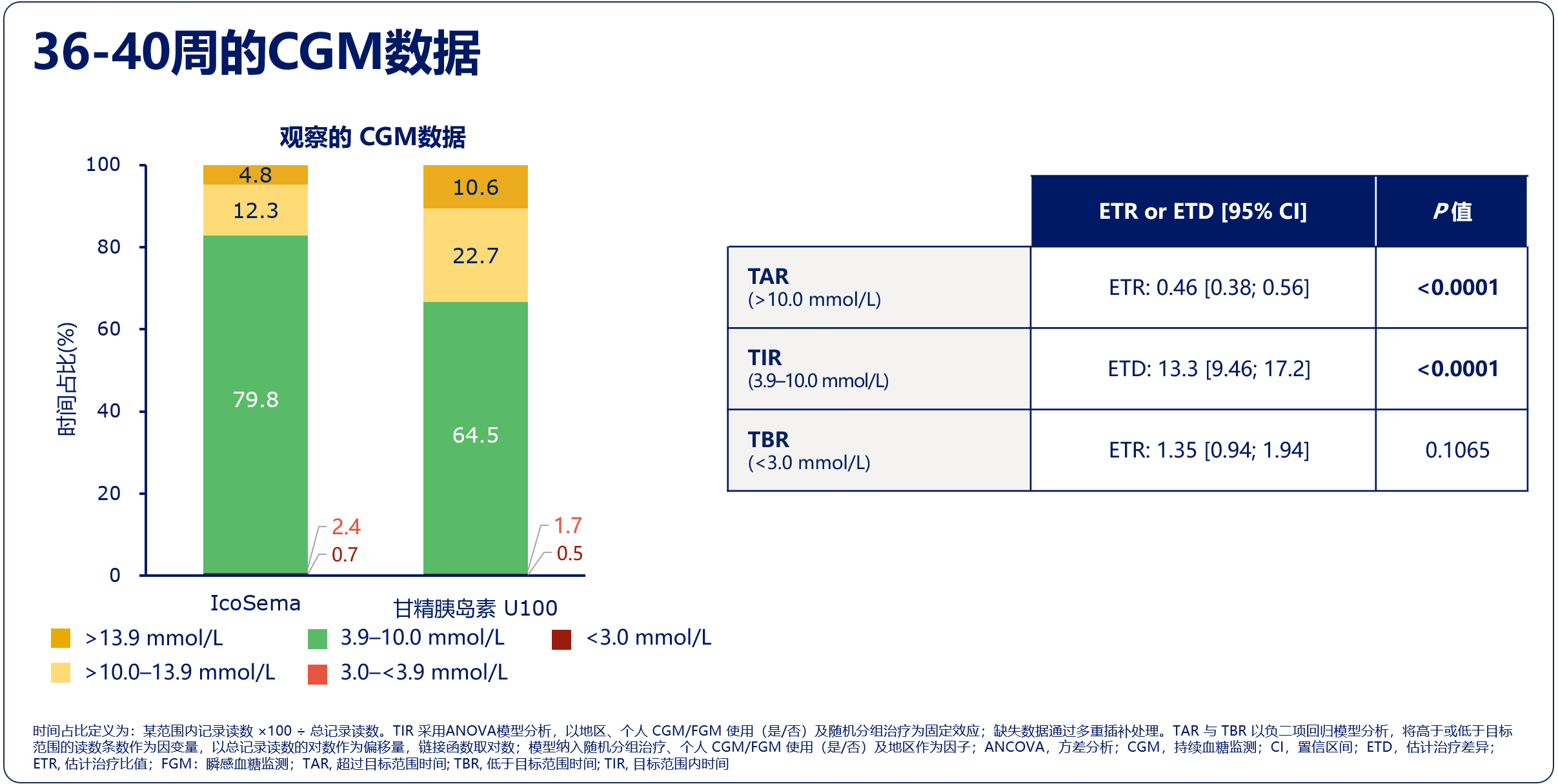
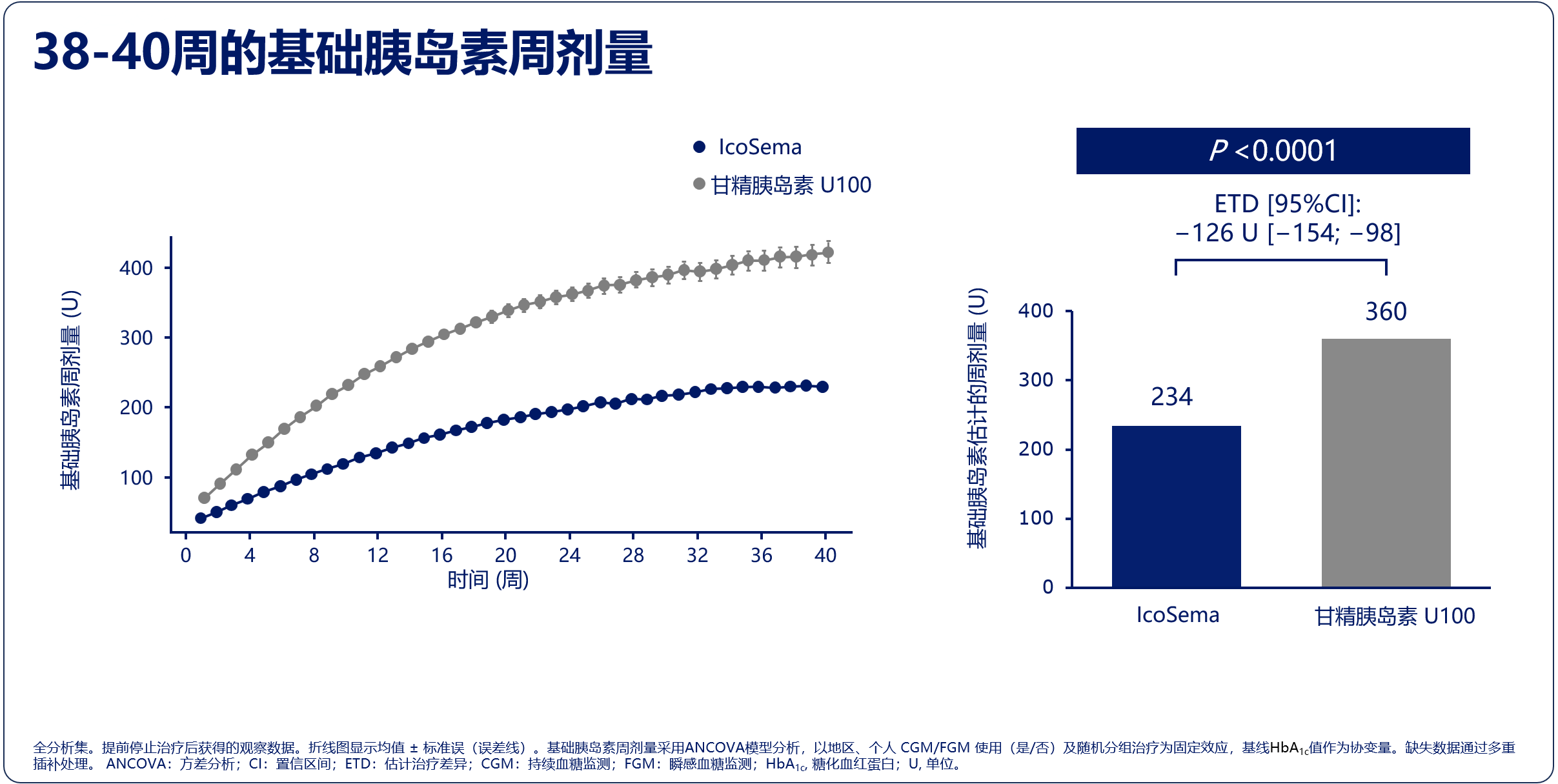
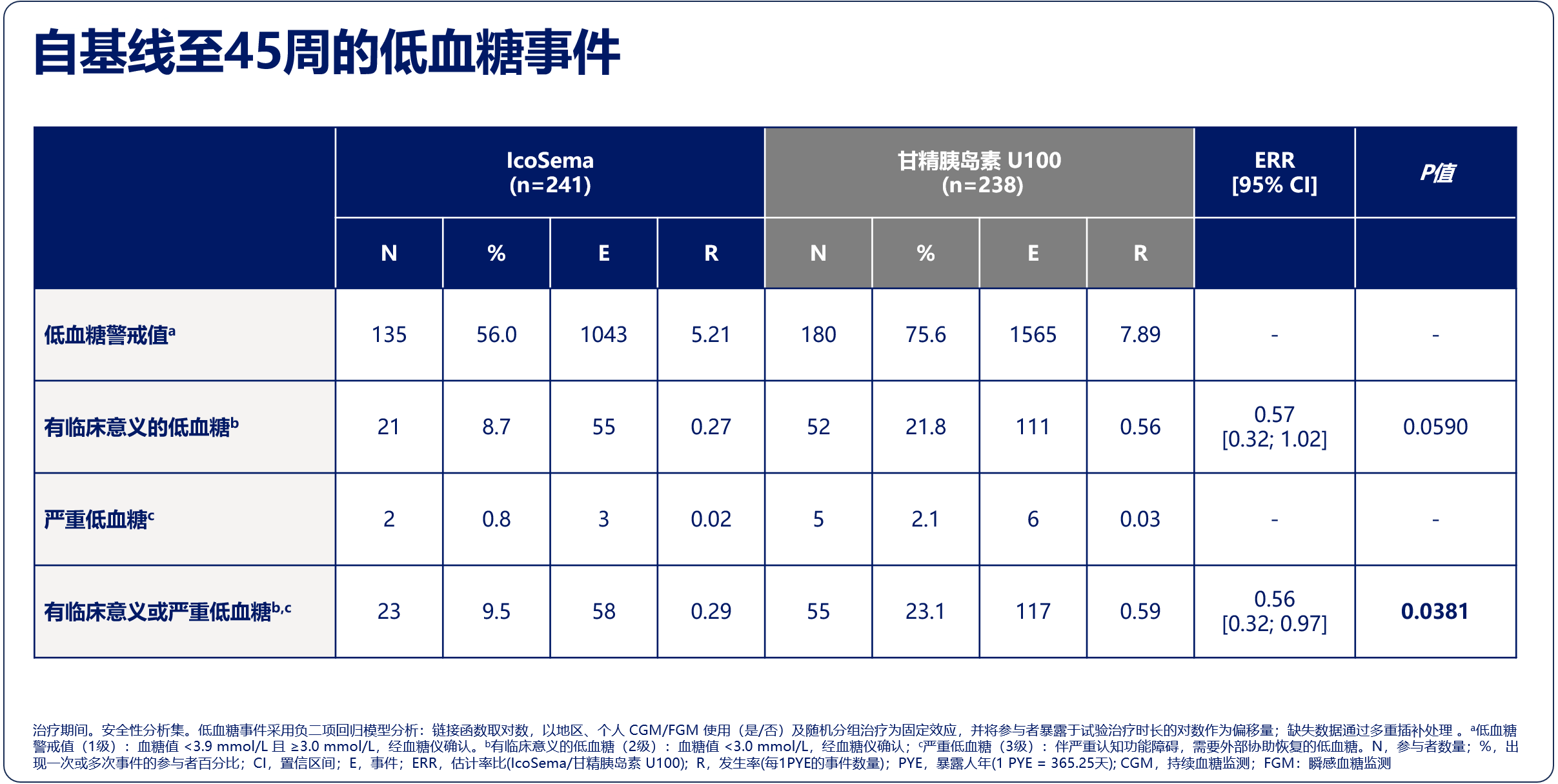
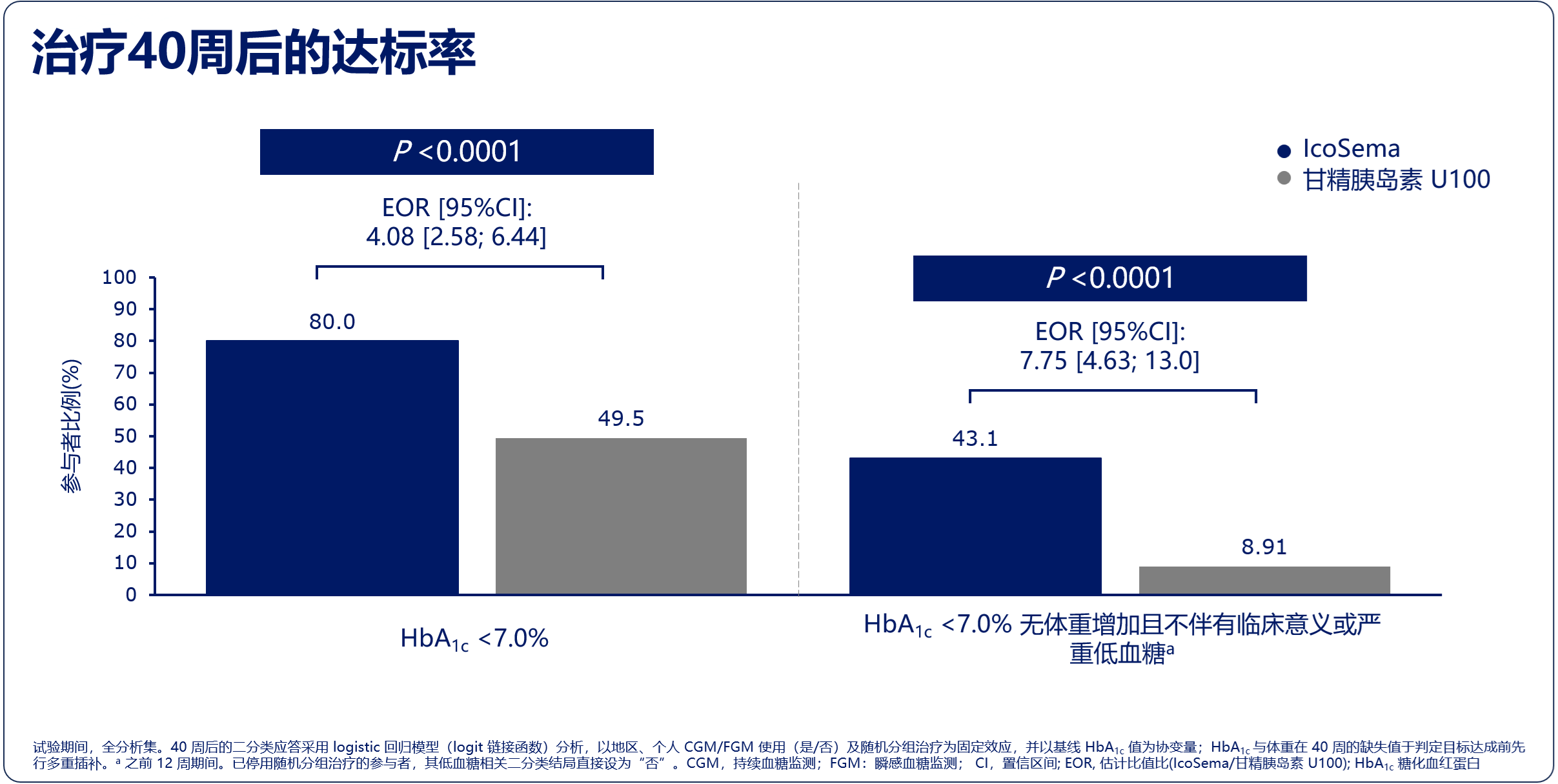
图4. COMBINE 4研究主要结果
综上,COMBINE 4研究结果表明,对于OAD治疗血糖控制不佳的T2DM患者,起始IcoSema治疗兼具有效性和安全性,相较于甘精胰岛素U100,HbA1c降幅和体重变化达成优效,TIR显著更优,有临床意义或严重低血糖风险显著更低,胰岛素剂量更少。
COMBINE 1研究中国亚组数据公布:兼具疗效和安全性,与全球结果保持一致
本次CDS会议上,COMBINE 1研究中国人群数据首次发布。COMBINE 1共纳入1291例基础胰岛素(±OAD)治疗血糖控制不佳的成人T2DM患者,其中中国亚组为130例,患者按1:1随机分配至IcoSema组或依柯胰岛素组(每组各65例)。主要终点为HbA1c从基线至第52周的变化。结果显示,IcoSema在中国T2DM患者中较基础胰岛素周制剂展现出更多优势(图5)[14]:
HbA1c降幅更优:中国亚组中,IcoSema组HbA1c从基线至第52周的改变显著优于依柯胰岛素组(-1.54% vs. -0.89%;ETD:-0.65%,95%CI:-0.91~-0.38;P<0.0001)。
体重变化更优:从基线至第52周的体重变化,IcoSema组为-2.70 kg,依柯胰岛素组为2.32 kg(ETD:-5.02,95%CI:-6.07~-3.97;P<0.0001)。
胰岛素周剂量更低:第50~52周,IcoSema组胰岛素周剂量显著更低(149 U vs. 312 U;ETD:-163,95%CI:-206~-119;2.14 vs. 4.10 U/kg;均P<0.0001)。
HbA1c达标率及复合达标率更高:52周时IcoSema组HbA1c<7.0%、HbA1c<7.0%且无体重增加和不伴有临床意义或严重低血糖的患者比例更高(分别为68.3% vs. 30.9%、52.4% vs. 6.0%;均P<0.0001)。
低血糖风险相似:从基线至第57周,两组有临床意义或严重低血糖的发生率相似(0.0735 vs. 0.0729事件/患者年)。
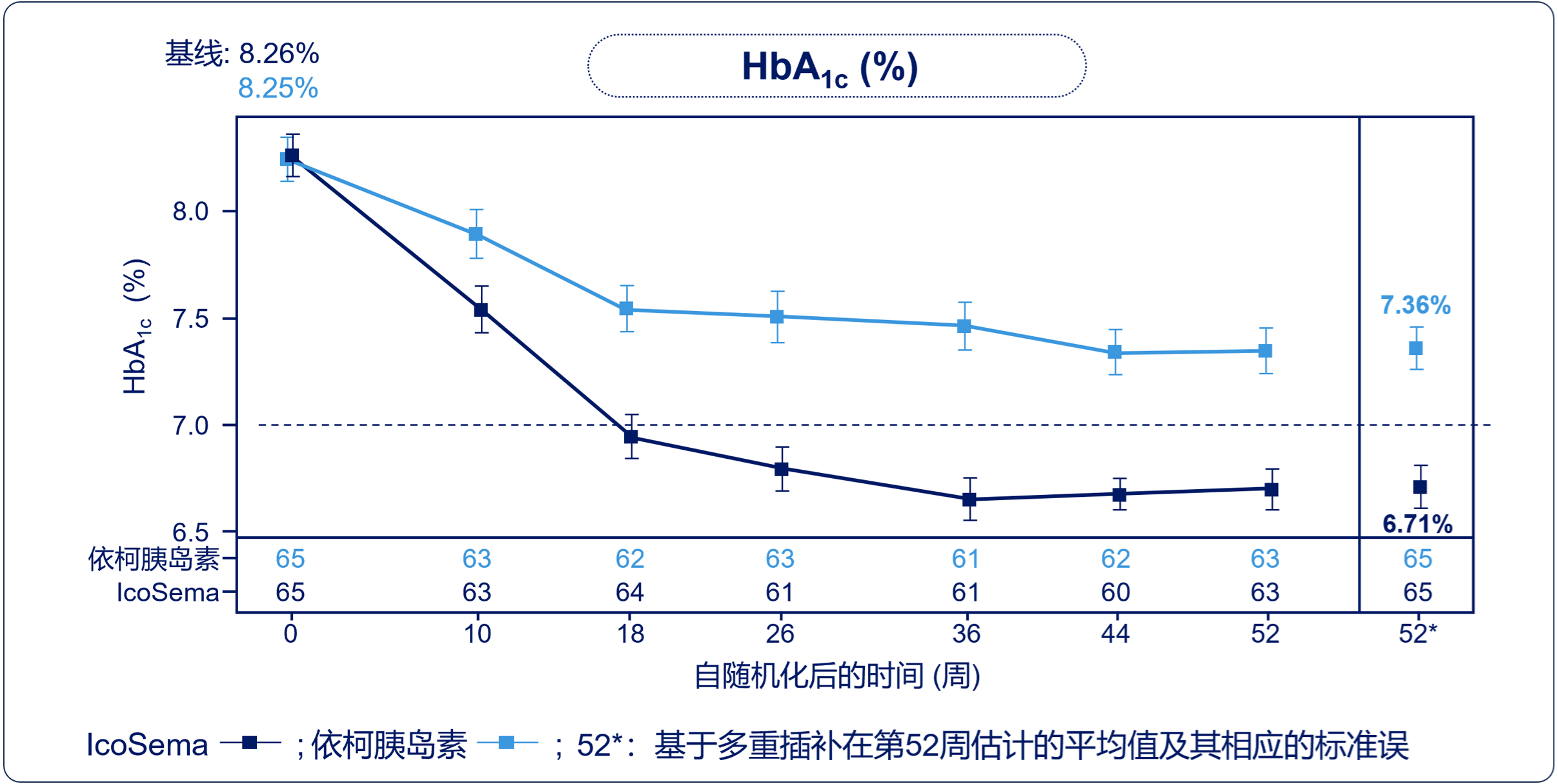
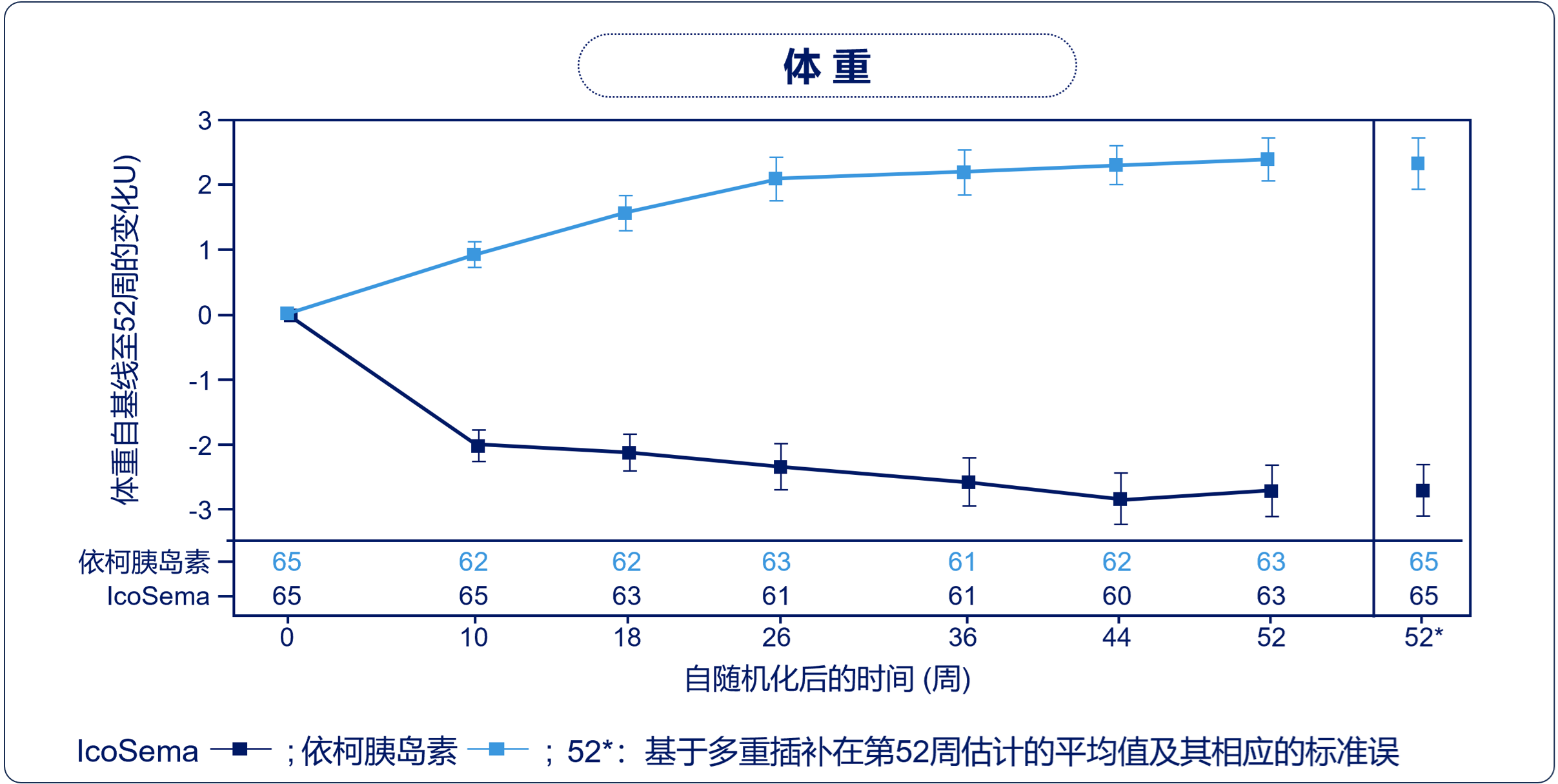
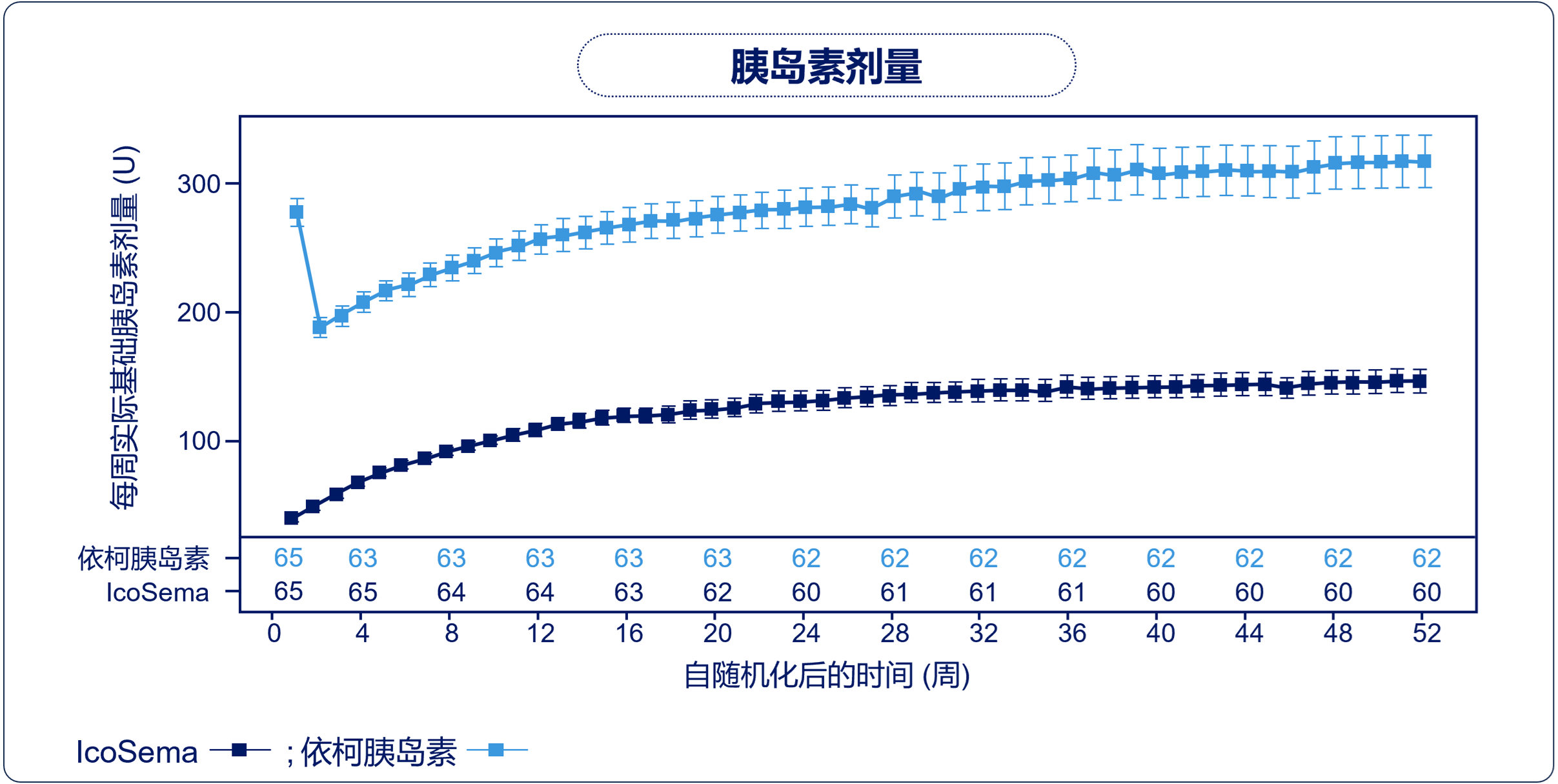
该事后分析证实,基础胰岛素日制剂治疗的中国T2DM患者转换为IcoSema治疗,在HbA1c改善、体重变化与胰岛素周剂量方面均显著优于依柯胰岛素,两组有临床意义或严重低血糖的发生率较低且相似。IcoSema在中国亚组中显示出良好的耐受性与安全性。中国亚组与全球COMBINE 1结果保持一致性。
三、结语及展望
联合降糖是T2DM的重要治疗策略,联合制剂也成为降糖药物创新研发的重要方向。IcoSema是全球首个基础胰岛素/GLP-1RA周制剂,其研发进展备受瞩目。COMBINE 1~4系列研究证实,既往不同治疗背景(包括接受基础胰岛素日制剂、GLP-1RA或OAD治疗)的T2DM患者,应用IcoSema可强效降糖且安全性良好,同时还能进一步减少注射次数、简化治疗方案,并带来体重获益、减少胰岛素剂量等多重获益,临床应用前景广阔。
姬秋和教授强调,IcoSema实现了“1+1>2”的创新联合,依柯胰岛素与司美格鲁肽强强联合并简化治疗,为改善糖尿病管理提供有力工具。纪立农教授表示,COMBINE系列研究及其事后分析的公布,为IcoSema将来在不同临床场景中的应用提供了更多支持。每周一次IcoSema引领联合降糖新高度,开启糖尿病药物治疗的新篇章。
参考文献
1. Ahmad E, et al. Lancet. 2022; 400(10365): 1803-1820.
2. ADA. Diabetes Care. 2025; 48(Suppl_1): S181-S206.
3. Davies MJ, et al . Diabetologia. 2022; 65(12): 1925-1966.
4. 中华医学会糖尿病学分会. 中华糖尿病杂志. 2025; 17(01): 16-139.
5. Dahlén AD, et al. Front Pharmacol. 2022; 12: 807548.
6. Philis-Tsimikas A, et al. Lancet Diabetes Endocrinol. 2023; 11(6): 414-425.
7. Bajaj HS, et al. Ann Intern Med. 2023; 176(11): 1476-1485.
8. Bajaj H. 2023 ADA Scientific Sessions. 803-P.
9. Polonsky WH, et al. Diabetes Ther. 2022; 13(1): 175-187.
10. Mathieu C, et al. Lancet Diabetes Endocrinol. 2025; 13(7): 568-579. COMBINE 1
11. Lingvay I, et al. Diabetologia. 2025; 68(4): 739-751. COMBINE 2
12. Billings L, et al. Lancet Diabetes Endocrinol. 2025; 13(7): 556-567. COMBINE 3
13. 纪立农, 等. COMBINE 4研究:每周一次IcoSema在口服降糖药控制不佳的2型糖尿病患者中,较每日一次甘精胰岛素U100实现更优的血糖控制. 中华医学会糖尿病学分会第二十七次学术会议, 陕西, 西安, 2025年11月19~22日.
14. 纪立农. 基于COMBINE 1研究的事后分析:每周一次IcoSema在中国2型糖尿病患者中的疗效与安全性. 中华医学会糖尿病学分会第二十七次学术会议, 陕西, 西安. 2025年11月19~22日.











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言