编者按:
2026年3月17日,美国临床内分泌医师协会(AACE)在Endocrine Practice杂志在线发布了《2026 AACE成人2型糖尿病管理流程共识声明(更新版)》[1],此次声明是在2023版基础上更新而成的,在延续既往循证框架的基础上,对糖尿病诊疗路径进行了系统性更新。此次更新流程图全文共分11部分,分别为:成人2型糖尿病管理原则、糖尿病前期、糖尿病分类(新增)、降低动脉粥样硬化性心血管疾病(ASCVD)风险:血脂异常、降低ASCVD风险:高血压、以合并症为中心的血糖控制、以血糖为中心的血糖控制、起始和调整胰岛素、2型糖尿病药物治疗概览、肥胖症药物治疗概览及成人2型糖尿病疫苗接种建议。此次更新重点包括以下几点:
强调生活方式干预与超重/肥胖治疗是糖尿病前期和2型糖尿病管理的核心支柱;
同时提供血脂异常、高血压等动脉粥样硬化危险因素的管理指导;
新增糖尿病分类流程,提醒临床医师关注2型糖尿病以外的其他糖尿病病因;
继续强调以合并症与并发症为中心的诊疗思路,而非仅关注血糖水平,以此指导成人2型糖尿病一线及后续药物选择。
医疗差异、新型药物可及性与费用问题,仍是部分2型糖尿病患者获得最优治疗的重要障碍。

流程 1:
AACE 成人2型糖尿病管理原则(图1)
生活方式干预被明确为所有治疗的基础,是贯穿疾病全程的核心策略。这不仅包括传统的饮食控制和运动干预,还涵盖戒烟限酒、改善睡眠质量以及心理健康管理等多个维度。该共识强调,只有在良好生活方式基础上实施药物治疗,才能实现长期稳定的代谢控制和并发症风险降低。
在体重管理方面,共识提出应采用综合减重方案以实现临床目标。超重与肥胖是胰岛素抵抗的关键驱动因素,与多种代谢并发症密切相关,因此减重不仅用于改善血糖,还可降低心血管疾病、脂肪肝及睡眠呼吸暂停(OSA)等风险。减重策略应结合生活方式干预、药物治疗及必要时的手术干预,实现个体化管理。
药物治疗选择需基于血糖目标及合并症情况综合决策,而非单纯依据血糖水平。对于合并超重或肥胖、ASCVD、慢性心力衰竭(CHF)、慢性肾脏疾病(CKD)、代谢相关脂肪性肝病(MASLD)及OSA等患者,应优先选择对相关并发症具有明确获益的药物。同时,治疗方案还需考虑药物的易用性、可及性及经济负担,以提高依从性和长期治疗效果。
在血糖控制目标方面,指南强调个体化制定,包括糖化血红蛋白(HbA1c)、葡萄糖管理指标(GMI)、目标范围内时间(TIR)、空腹血糖(FBG)、餐后血糖(PPG)等多个指标。总体目标为HbA1c≤6.5%,或在安全前提下尽可能接近正常水平。与此同时,应避免治疗惰性,建议在3个月内评估疗效并及时调整方案,以尽早达标。此外,治疗过程中需严格避免低血糖,并强烈推荐使用连续血糖监测(CGM)以优化血糖管理。最终目标是通过全面管理合并症与并发症,实现真正的综合照护。

图1.AACE 成人2型糖尿病管理原则
流程2:
糖尿病前期管理(图2)
糖尿病前期是因胰岛素抵抗(多由超重/肥胖导致)、胰腺分泌胰岛素不足引发的代谢异常状态。其诊断标准包括:空腹血糖受损(IFG)5.6~6.9mmol/L;糖耐量减低(IGT),即口服75g葡萄糖耐量试验(OGTT)2小时血糖7.8~11mmol/L;HbA1c为5.7%~6.4%(39~47mmol/mol)。代谢综合征(NCEP ATP Ⅲ标准)亦视为糖尿病前期等同状态。
核心管理目标包括:在合适情况下促进主动或预防体重增加,以减轻胰岛素抵抗;评估肥胖相关性慢性病(ABCD)并发症以指导诊疗;干预ASCVD危险因素(如高血压、血脂异常),并防治MASLD的发生与进展。
干预方案以生活方式干预为基础,适用于所有患者,包括医学营养治疗(控制热量、地中海饮食或DASH饮食)、规律运动(每周150分钟中等强度有氧运动及2~3次抗阻运动)、戒烟、限酒、改善睡眠以及关注心理健康。
在减重干预方面,减重7%~10%可有效延缓进展为2型糖尿病。一线减重药物包括司美格鲁肽(≥2.4mg)、替尔泊肽、利拉鲁肽(3mg)及芬特明/托吡酯缓释片;合并ASCVD、MASH或OSA者优先选择司美格鲁肽2.4mg或替尔泊肽。不耐受或不可及上述药物时,可选纳曲酮缓释/安非他酮缓释、芬特明(短期)或奥利司他。
此外,可考虑非药物器械干预,如口服水凝胶胶囊、胃内球囊等;BMI≥35kg/m2者可考虑代谢(减重)手术。降糖药物用于预防虽无明确适应证,但已有临床证据支持二甲双胍、吡格列酮及阿卡波糖的应用。
对于非肥胖患者,应排查1型糖尿病(T1D)及成人隐匿性自身免疫性糖尿病(LADA),必要时进行自身抗体筛查。

图2.糖尿病前期管理流程
流程3:
糖尿病分类(图3)
糖尿病诊断需基于标准化指标,包括HbA1c、空腹血糖、OGTT及随机血糖等,若无症状需重复确认。在确诊后,应进一步明确糖尿病类型,而不能简单归类为2型糖尿病,这是本次指南新增的重要内容。
分类过程中,应结合临床表现评估是否符合典型2型糖尿病特征,如超重、家族史及胰岛素抵抗表现等。对于表现不典型或治疗反应不佳的患者,应高度怀疑其他类型糖尿病。成人起病的1型糖尿病并不少见,需通过自身抗体及C肽检测进行鉴别。
此外,还应识别其他类型糖尿病,如继发性糖尿病、单基因糖尿病及药物诱导性糖尿病等。正确的分类对于制定合理治疗方案至关重要,可避免误诊带来的严重后果。

图3.糖尿病分类流程
流程4:
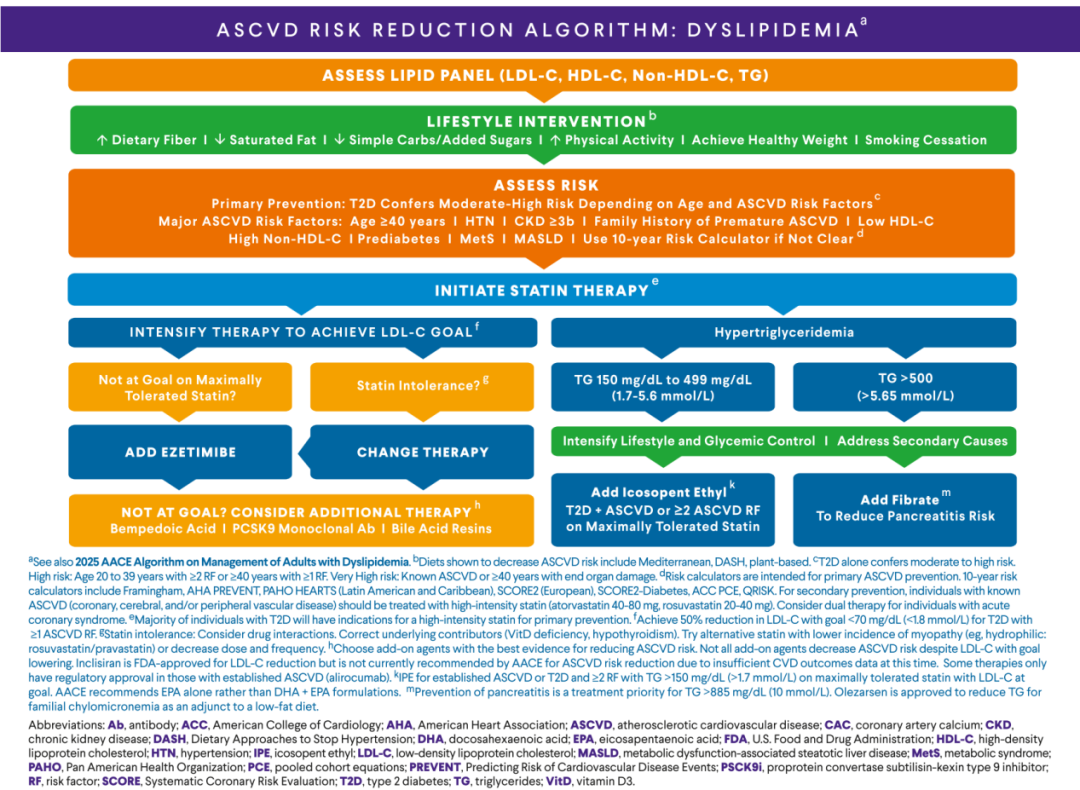
降低ASCVD风险——血脂异常(图4)
血脂管理是降低心血管风险的重要环节,应在确诊时进行系统评估,包括LDL-C、HDL-C及甘油三酯等指标,并排除继发性或遗传性因素。非空腹血脂可用于初步评估,但在特定情况下需空腹检测。
生活方式干预是基础措施,包括减重、健康饮食及规律运动。推荐采用富含膳食纤维和优质蛋白的饮食模式,同时限制糖和酒精摄入,以改善脂质代谢。
在药物治疗方面,应根据ASCVD风险分层选择治疗策略。他汀类为一线药物,不耐受者可调整剂量或更换药物。若未达标,可联合依折麦布或PCSK9抑制剂等进一步强化治疗。对于高甘油三酯患者,应根据水平采取相应措施,严重升高者需优先预防胰腺炎。
流程5:
降低ASCVD风险——高血压(图5)
多数糖尿病患者高血压管理目标通常为<130/80 mmHg,但需根据患者具体情况个体化调整。对于高风险人群可适当降低目标,而对于老年或特殊患者则可适当放宽。
生活方式干预是基础,包括减重、限钠、健康饮食及规律运动等。药物治疗方面,ACEI或ARB为一线选择,尤其适用于合并肾病或蛋白尿患者。对于血压较高者,可直接采用联合用药策略。
当常规治疗无法达标时,可逐步增加其他药物,如利尿剂、钙通道阻滞剂或MRA等。同时,应注意排查继发性高血压,特别是在难治性病例中。

图5.降低ASCVD风险流程:高血压
流程6:
以合并症为中心的血糖控制(图6)
该流程强调优先根据合并症/并发症选药,而非仅看血糖,兼顾心、肾、肝、体重获益。
心力衰竭(HF)方面,首选SGLT2i,无论HbA1c、是否用二甲双胍,射血分数降低型心力衰竭(HFrEF)/射血分数保留型心力衰竭(HFpEF)均获益,降低心衰住院+CV死亡。肥胖相关HFpEF可选用GLP-1RA、GIP/GLP-1RA。应避免DPP-4i中的部分药物(NYHAⅢ~Ⅳ级慎用)及TZD类(加重水钠潴留,NYHAⅢ~Ⅳ级禁用)。
CKD方面,首选SGLT2i,可护肾、延缓eGFR下降、降低终末期肾病风险;可联用非甾体MRA(eGFR≥25、UACR≥30mg/g);备选GLP-1RA,可显著降低肾脏不良事件。
ASCVD或高危ASCVD方面,首选GLP-1RA,可降低三点主要不良心血管事件(MACE)(心梗、卒中、CV死亡);备选SGLT2i,可降低MACE、心衰住院;GIP/GLP-1RA疗效不劣于GLP-1RA,可降低全因死亡。
卒中/短暂性脑缺血发作(T1A)方面,首选GLP-1RA,可降低非致死性卒中;备选TZD类,可降低卒中复发,适用于胰岛素抵抗/糖尿病前期/2型糖尿病合并卒中患者。
MASLD/MASH方面,首选GLP-1RA;备选包括GIP/GLP-1RA、TZD类、SGLT2i;生活方式干预包括减重>7%~10%,戒酒(中重度纤维化)。
用药原则方面,严重高血糖(HbA1c>10%、血糖>300mg/dl+症状)优先基础胰岛素、GLP-1RA或GIP/GLP-1RA;合并多个并发症时可联用(如SGLT2i+GLP-1RA);无上述并发症则转至流程7(以血糖为中心)。
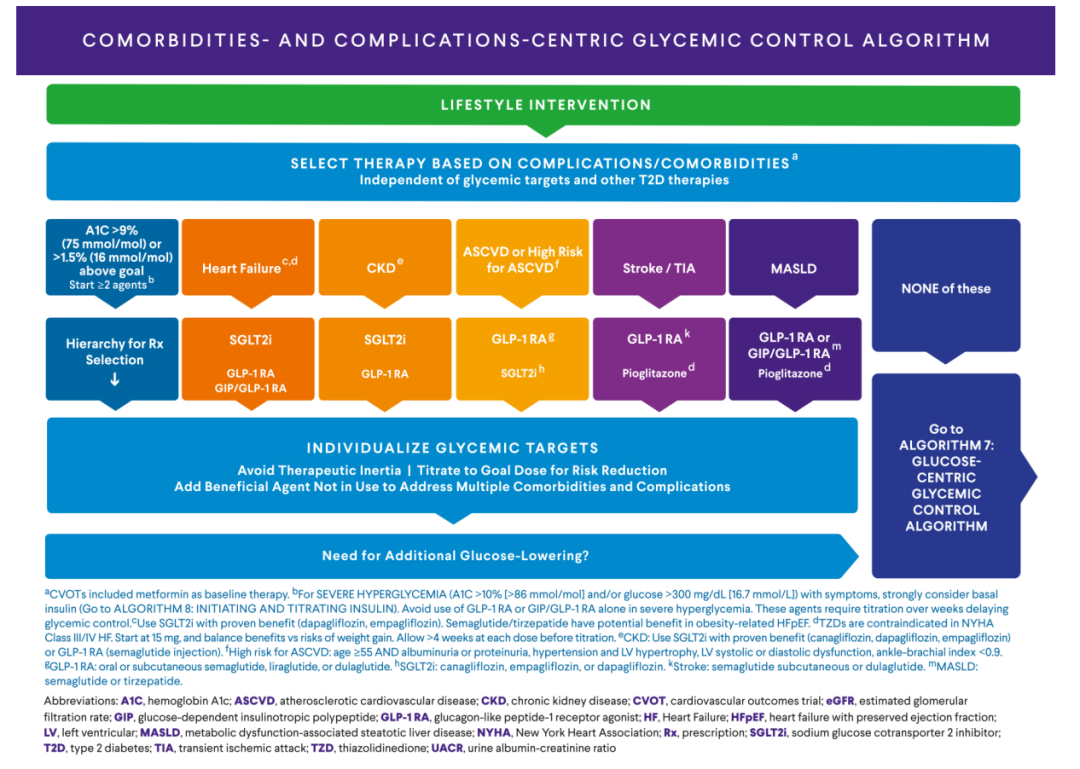
图6.以合并症为中心的血糖控制
流程7:
以血糖为中心的血糖控制(图7)
该流程适用于无高危HF、CKD、ASCVD、卒中及MASLD的2型糖尿病患者。
对于严重高血糖患者(HbA1c>10%、血糖>300mg/dl伴症状),应起始基础胰岛素,以快速、安全降低血糖,待血糖稳定后可转换为非胰岛素药物治疗。
对于非严重高血糖患者,一线首选二甲双胍(eGFR≥45ml/min/1.73m2)。如合并超重或肥胖、需减重者,优先选择替尔泊肽或GLP-1RA,其次为SGLT2i;如低血糖风险高或需避免低血糖,可选择GLP-1RA、SGLT2i、DPP-4i或TZD类药物;在费用受限情况下,可采用二甲双胍联合TZD、磺脲类或格列奈类。
对于新诊断且HbA1c>9%或高于目标1.5%的患者,建议直接起始双联或三联治疗,以尽快达标。同时不推荐DPP-4i与GLP-1RA或GIP/GLP-1 RA联合使用。
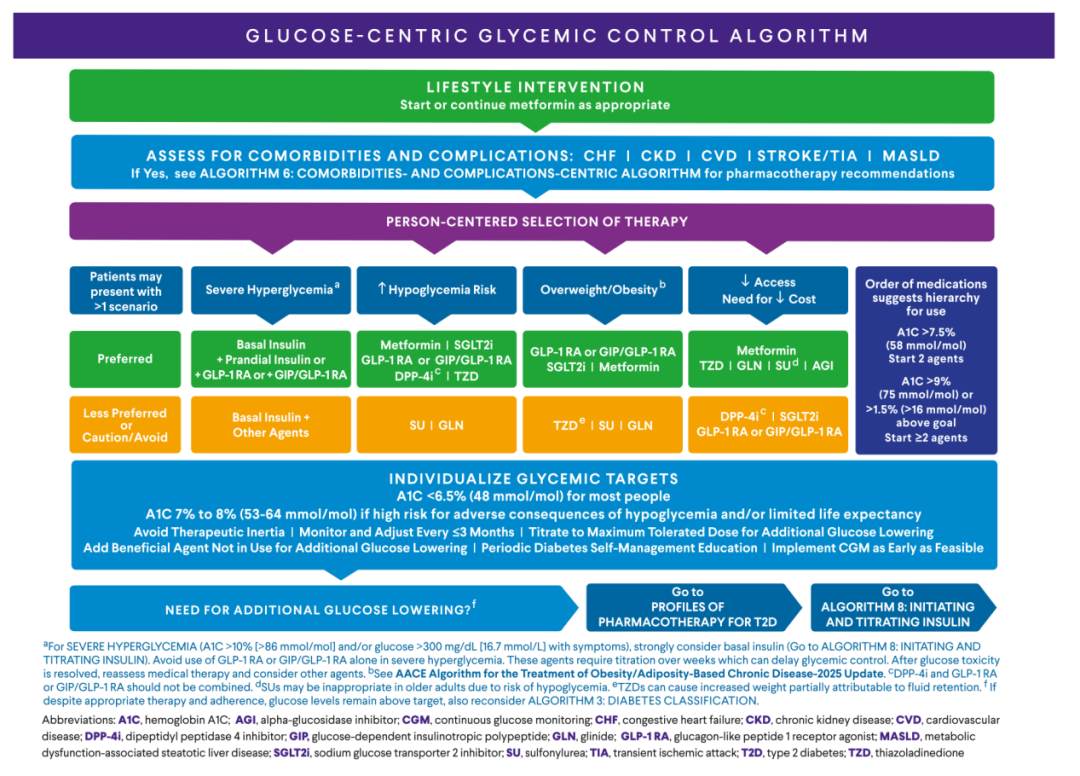
图7.以血糖为中心的血糖控制流程
流程8:
胰岛素起始与调整(图8)
胰岛素治疗应在个体化目标下进行,重点是在避免低血糖的前提下实现达标。CGM的应用可帮助优化治疗过程并提高安全性。基础胰岛素应根据HbA1c水平起始,并逐步调整剂量。若控制不佳,应考虑增加餐时胰岛素,并避免过度增加基础剂量。治疗过程中需持续监测血糖变化,并及时调整方案,同时做好低血糖预防及应急准备。
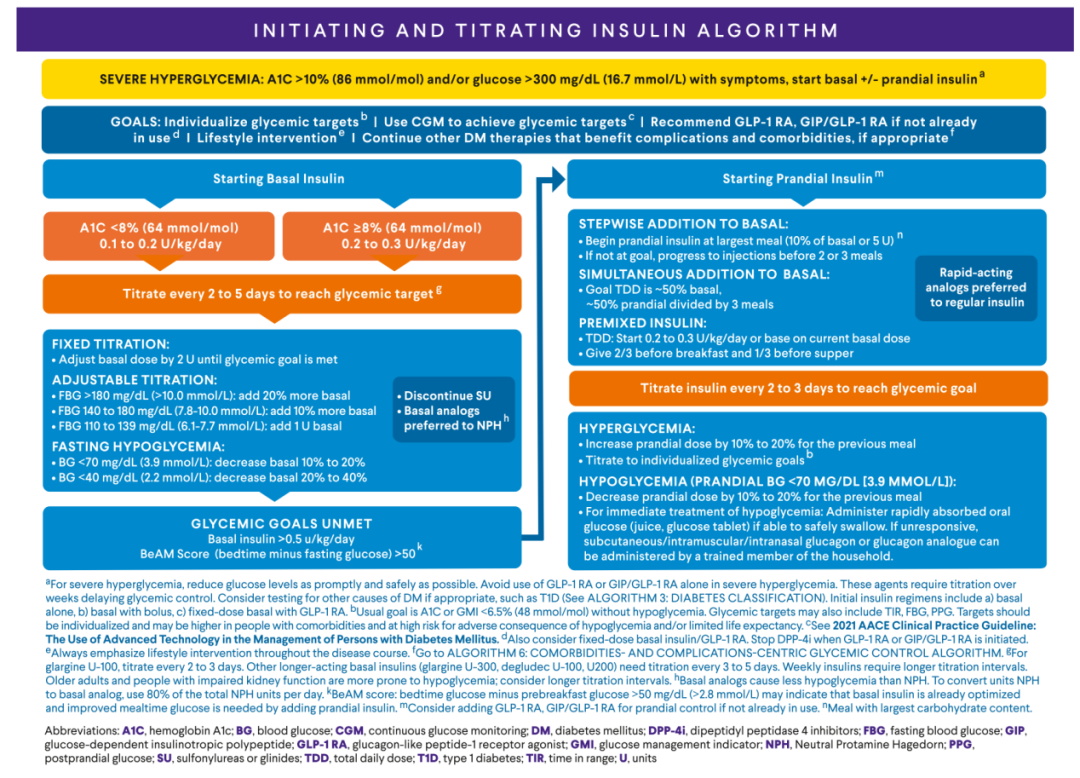
图8.胰岛素起始与调整流程
流程9:
药物治疗概要(图9)
降糖药物种类多样,不同药物在降糖效果、体重变化及心肾获益等方面存在差异,药物选择应基于疗效、安全性及患者个体特征进行综合评估与个体化决策。同时,应关注各类药物的特异性疗效(HbA1c降低幅度)、临床获益(ASCVD、HF、CKD、体重下降、MASLD)以及不良反应(低血糖、胃肠道反应及其他禁忌或注意事项)。
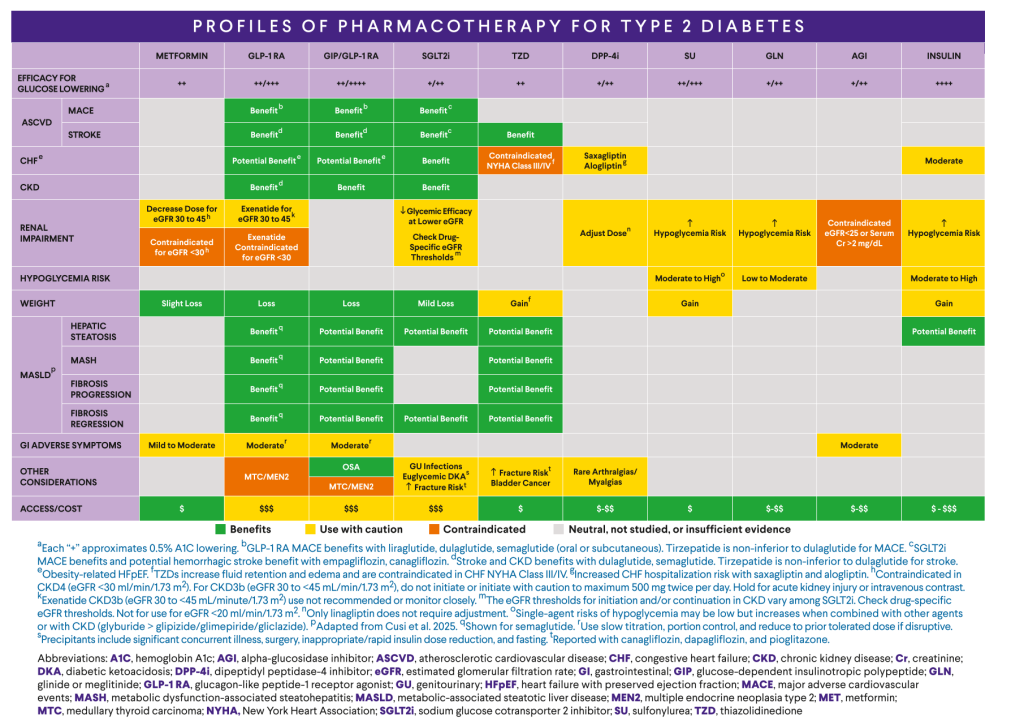
图9.2型糖尿病药物治疗特征
流程10:
肥胖药物治疗概要(图10)
肥胖治疗在糖尿病管理中占据重要地位。在选择药物时,应充分考虑不良反应及禁忌证,并结合患者具体情况制定个体化方案。
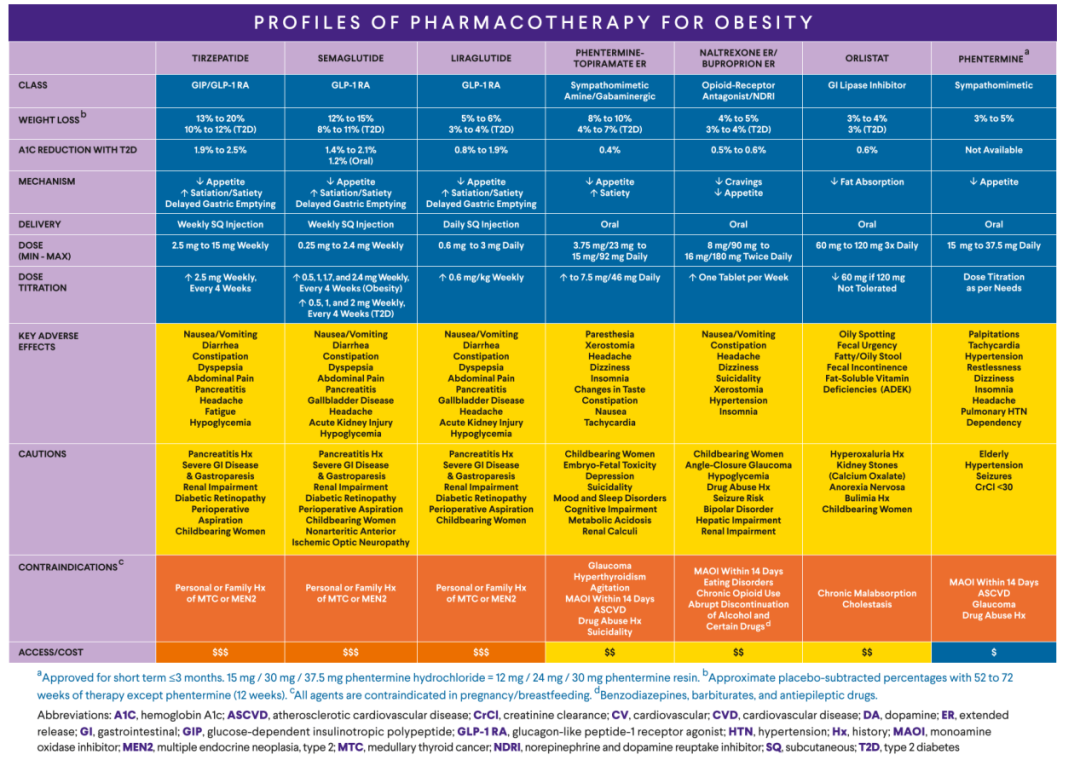
图10.常用减重药物的特征
流程11:
疫苗接种建议(图11)
糖尿病患者感染风险较高,因此疫苗接种是综合管理的重要组成部分。应按照推荐完成流感、肺炎球菌及新冠疫苗接种。对于特定年龄人群,还应补充带状疱疹、RSV及Tdap疫苗,以进一步降低感染相关风险。
临床实践中,应在每次就诊中评估疫苗接种情况,并进行推荐、接种及记录,以实现规范化管理。
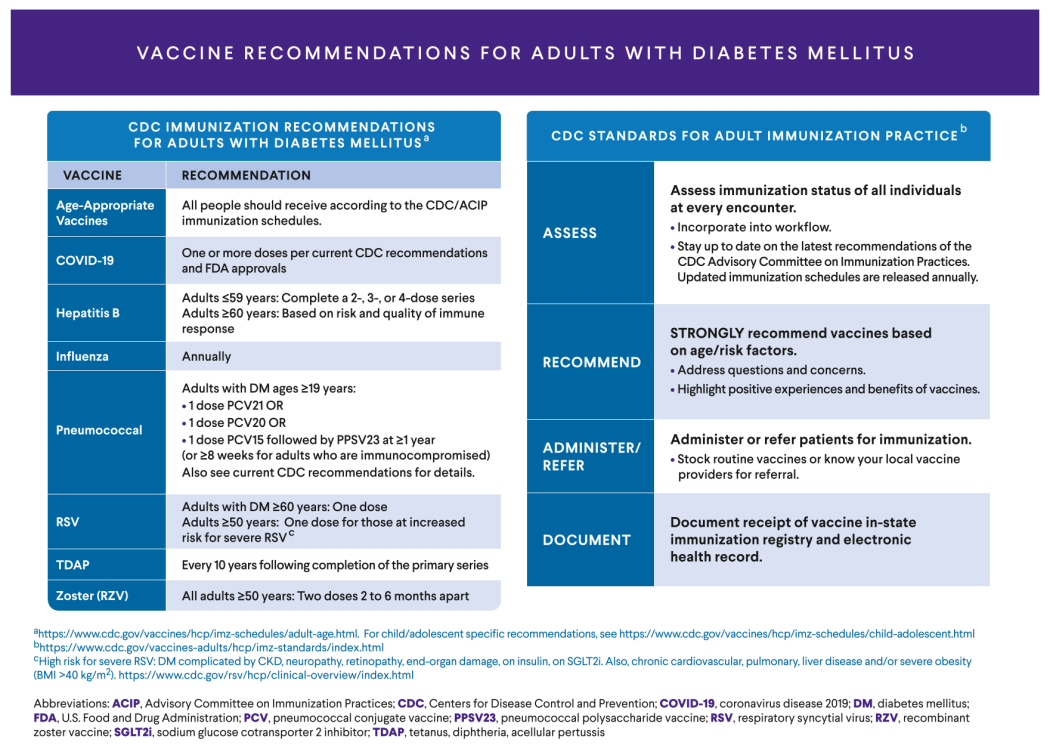
图11.成人糖尿病疫苗接种建议流程
结语
总体而言,2026版更新在延续既往框架的基础上,进一步明确了生活方式干预与超重/肥胖管理的核心地位,强化动脉粥样硬化危险因素的综合控制,并通过新增糖尿病分类流程完善诊断路径;同时基于最新循证证据,持续推动诊疗思路从单纯控糖转向以合并症与并发症为中心,以指导药物选择与长期管理策略。尽管如此,医疗差异、新型药物可及性及费用问题仍是实现最优治疗的重要挑战。
参考文献
1.Samson SL, et al. American Association of Clinical Endocrinology Consensus Statement: Algorithm for Management of Adults With Type 2 Diabetes-2026 Update. Endocr Pract. 2026 Mar 17:S1530-891X(26)00022-4. doi: 10.1016/j.eprac.2026.01.006. Epub ahead of print. PMID: 41842862. 2 comments
2026年3月17日,美国临床内分泌医师协会(AACE)在Endocrine Practice杂志在线发布了《2026 AACE成人2型糖尿病管理流程共识声明(更新版)》[1],此次声明是在2023版基础上更新而成的,在延续既往循证框架的基础上,对糖尿病诊疗路径进行了系统性更新。此次更新流程图全文共分11部分,分别为:成人2型糖尿病管理原则、糖尿病前期、糖尿病分类(新增)、降低动脉粥样硬化性心血管疾病(ASCVD)风险:血脂异常、降低ASCVD风险:高血压、以合并症为中心的血糖控制、以血糖为中心的血糖控制、起始和调整胰岛素、2型糖尿病药物治疗概览、肥胖症药物治疗概览及成人2型糖尿病疫苗接种建议。此次更新重点包括以下几点:
强调生活方式干预与超重/肥胖治疗是糖尿病前期和2型糖尿病管理的核心支柱;
同时提供血脂异常、高血压等动脉粥样硬化危险因素的管理指导;
新增糖尿病分类流程,提醒临床医师关注2型糖尿病以外的其他糖尿病病因;
继续强调以合并症与并发症为中心的诊疗思路,而非仅关注血糖水平,以此指导成人2型糖尿病一线及后续药物选择。
医疗差异、新型药物可及性与费用问题,仍是部分2型糖尿病患者获得最优治疗的重要障碍。

流程 1:
AACE 成人2型糖尿病管理原则(图1)
生活方式干预被明确为所有治疗的基础,是贯穿疾病全程的核心策略。这不仅包括传统的饮食控制和运动干预,还涵盖戒烟限酒、改善睡眠质量以及心理健康管理等多个维度。该共识强调,只有在良好生活方式基础上实施药物治疗,才能实现长期稳定的代谢控制和并发症风险降低。
在体重管理方面,共识提出应采用综合减重方案以实现临床目标。超重与肥胖是胰岛素抵抗的关键驱动因素,与多种代谢并发症密切相关,因此减重不仅用于改善血糖,还可降低心血管疾病、脂肪肝及睡眠呼吸暂停(OSA)等风险。减重策略应结合生活方式干预、药物治疗及必要时的手术干预,实现个体化管理。
药物治疗选择需基于血糖目标及合并症情况综合决策,而非单纯依据血糖水平。对于合并超重或肥胖、ASCVD、慢性心力衰竭(CHF)、慢性肾脏疾病(CKD)、代谢相关脂肪性肝病(MASLD)及OSA等患者,应优先选择对相关并发症具有明确获益的药物。同时,治疗方案还需考虑药物的易用性、可及性及经济负担,以提高依从性和长期治疗效果。
在血糖控制目标方面,指南强调个体化制定,包括糖化血红蛋白(HbA1c)、葡萄糖管理指标(GMI)、目标范围内时间(TIR)、空腹血糖(FBG)、餐后血糖(PPG)等多个指标。总体目标为HbA1c≤6.5%,或在安全前提下尽可能接近正常水平。与此同时,应避免治疗惰性,建议在3个月内评估疗效并及时调整方案,以尽早达标。此外,治疗过程中需严格避免低血糖,并强烈推荐使用连续血糖监测(CGM)以优化血糖管理。最终目标是通过全面管理合并症与并发症,实现真正的综合照护。

图1.AACE 成人2型糖尿病管理原则
流程2:
糖尿病前期管理(图2)
糖尿病前期是因胰岛素抵抗(多由超重/肥胖导致)、胰腺分泌胰岛素不足引发的代谢异常状态。其诊断标准包括:空腹血糖受损(IFG)5.6~6.9mmol/L;糖耐量减低(IGT),即口服75g葡萄糖耐量试验(OGTT)2小时血糖7.8~11mmol/L;HbA1c为5.7%~6.4%(39~47mmol/mol)。代谢综合征(NCEP ATP Ⅲ标准)亦视为糖尿病前期等同状态。
核心管理目标包括:在合适情况下促进主动或预防体重增加,以减轻胰岛素抵抗;评估肥胖相关性慢性病(ABCD)并发症以指导诊疗;干预ASCVD危险因素(如高血压、血脂异常),并防治MASLD的发生与进展。
干预方案以生活方式干预为基础,适用于所有患者,包括医学营养治疗(控制热量、地中海饮食或DASH饮食)、规律运动(每周150分钟中等强度有氧运动及2~3次抗阻运动)、戒烟、限酒、改善睡眠以及关注心理健康。
在减重干预方面,减重7%~10%可有效延缓进展为2型糖尿病。一线减重药物包括司美格鲁肽(≥2.4mg)、替尔泊肽、利拉鲁肽(3mg)及芬特明/托吡酯缓释片;合并ASCVD、MASH或OSA者优先选择司美格鲁肽2.4mg或替尔泊肽。不耐受或不可及上述药物时,可选纳曲酮缓释/安非他酮缓释、芬特明(短期)或奥利司他。
此外,可考虑非药物器械干预,如口服水凝胶胶囊、胃内球囊等;BMI≥35kg/m2者可考虑代谢(减重)手术。降糖药物用于预防虽无明确适应证,但已有临床证据支持二甲双胍、吡格列酮及阿卡波糖的应用。
对于非肥胖患者,应排查1型糖尿病(T1D)及成人隐匿性自身免疫性糖尿病(LADA),必要时进行自身抗体筛查。

图2.糖尿病前期管理流程
流程3:
糖尿病分类(图3)
糖尿病诊断需基于标准化指标,包括HbA1c、空腹血糖、OGTT及随机血糖等,若无症状需重复确认。在确诊后,应进一步明确糖尿病类型,而不能简单归类为2型糖尿病,这是本次指南新增的重要内容。
分类过程中,应结合临床表现评估是否符合典型2型糖尿病特征,如超重、家族史及胰岛素抵抗表现等。对于表现不典型或治疗反应不佳的患者,应高度怀疑其他类型糖尿病。成人起病的1型糖尿病并不少见,需通过自身抗体及C肽检测进行鉴别。
此外,还应识别其他类型糖尿病,如继发性糖尿病、单基因糖尿病及药物诱导性糖尿病等。正确的分类对于制定合理治疗方案至关重要,可避免误诊带来的严重后果。

图3.糖尿病分类流程
流程4:
降低ASCVD风险——血脂异常(图4)
血脂管理是降低心血管风险的重要环节,应在确诊时进行系统评估,包括LDL-C、HDL-C及甘油三酯等指标,并排除继发性或遗传性因素。非空腹血脂可用于初步评估,但在特定情况下需空腹检测。
生活方式干预是基础措施,包括减重、健康饮食及规律运动。推荐采用富含膳食纤维和优质蛋白的饮食模式,同时限制糖和酒精摄入,以改善脂质代谢。
在药物治疗方面,应根据ASCVD风险分层选择治疗策略。他汀类为一线药物,不耐受者可调整剂量或更换药物。若未达标,可联合依折麦布或PCSK9抑制剂等进一步强化治疗。对于高甘油三酯患者,应根据水平采取相应措施,严重升高者需优先预防胰腺炎。
流程5:
降低ASCVD风险——高血压(图5)
多数糖尿病患者高血压管理目标通常为<130/80 mmHg,但需根据患者具体情况个体化调整。对于高风险人群可适当降低目标,而对于老年或特殊患者则可适当放宽。
生活方式干预是基础,包括减重、限钠、健康饮食及规律运动等。药物治疗方面,ACEI或ARB为一线选择,尤其适用于合并肾病或蛋白尿患者。对于血压较高者,可直接采用联合用药策略。
当常规治疗无法达标时,可逐步增加其他药物,如利尿剂、钙通道阻滞剂或MRA等。同时,应注意排查继发性高血压,特别是在难治性病例中。

图5.降低ASCVD风险流程:高血压
流程6:
以合并症为中心的血糖控制(图6)
该流程强调优先根据合并症/并发症选药,而非仅看血糖,兼顾心、肾、肝、体重获益。
心力衰竭(HF)方面,首选SGLT2i,无论HbA1c、是否用二甲双胍,射血分数降低型心力衰竭(HFrEF)/射血分数保留型心力衰竭(HFpEF)均获益,降低心衰住院+CV死亡。肥胖相关HFpEF可选用GLP-1RA、GIP/GLP-1RA。应避免DPP-4i中的部分药物(NYHAⅢ~Ⅳ级慎用)及TZD类(加重水钠潴留,NYHAⅢ~Ⅳ级禁用)。
CKD方面,首选SGLT2i,可护肾、延缓eGFR下降、降低终末期肾病风险;可联用非甾体MRA(eGFR≥25、UACR≥30mg/g);备选GLP-1RA,可显著降低肾脏不良事件。
ASCVD或高危ASCVD方面,首选GLP-1RA,可降低三点主要不良心血管事件(MACE)(心梗、卒中、CV死亡);备选SGLT2i,可降低MACE、心衰住院;GIP/GLP-1RA疗效不劣于GLP-1RA,可降低全因死亡。
卒中/短暂性脑缺血发作(T1A)方面,首选GLP-1RA,可降低非致死性卒中;备选TZD类,可降低卒中复发,适用于胰岛素抵抗/糖尿病前期/2型糖尿病合并卒中患者。
MASLD/MASH方面,首选GLP-1RA;备选包括GIP/GLP-1RA、TZD类、SGLT2i;生活方式干预包括减重>7%~10%,戒酒(中重度纤维化)。
用药原则方面,严重高血糖(HbA1c>10%、血糖>300mg/dl+症状)优先基础胰岛素、GLP-1RA或GIP/GLP-1RA;合并多个并发症时可联用(如SGLT2i+GLP-1RA);无上述并发症则转至流程7(以血糖为中心)。

图6.以合并症为中心的血糖控制
流程7:
以血糖为中心的血糖控制(图7)
该流程适用于无高危HF、CKD、ASCVD、卒中及MASLD的2型糖尿病患者。
对于严重高血糖患者(HbA1c>10%、血糖>300mg/dl伴症状),应起始基础胰岛素,以快速、安全降低血糖,待血糖稳定后可转换为非胰岛素药物治疗。
对于非严重高血糖患者,一线首选二甲双胍(eGFR≥45ml/min/1.73m2)。如合并超重或肥胖、需减重者,优先选择替尔泊肽或GLP-1RA,其次为SGLT2i;如低血糖风险高或需避免低血糖,可选择GLP-1RA、SGLT2i、DPP-4i或TZD类药物;在费用受限情况下,可采用二甲双胍联合TZD、磺脲类或格列奈类。
对于新诊断且HbA1c>9%或高于目标1.5%的患者,建议直接起始双联或三联治疗,以尽快达标。同时不推荐DPP-4i与GLP-1RA或GIP/GLP-1 RA联合使用。

图7.以血糖为中心的血糖控制流程
流程8:
胰岛素起始与调整(图8)
胰岛素治疗应在个体化目标下进行,重点是在避免低血糖的前提下实现达标。CGM的应用可帮助优化治疗过程并提高安全性。基础胰岛素应根据HbA1c水平起始,并逐步调整剂量。若控制不佳,应考虑增加餐时胰岛素,并避免过度增加基础剂量。治疗过程中需持续监测血糖变化,并及时调整方案,同时做好低血糖预防及应急准备。

图8.胰岛素起始与调整流程
流程9:
药物治疗概要(图9)
降糖药物种类多样,不同药物在降糖效果、体重变化及心肾获益等方面存在差异,药物选择应基于疗效、安全性及患者个体特征进行综合评估与个体化决策。同时,应关注各类药物的特异性疗效(HbA1c降低幅度)、临床获益(ASCVD、HF、CKD、体重下降、MASLD)以及不良反应(低血糖、胃肠道反应及其他禁忌或注意事项)。

图9.2型糖尿病药物治疗特征
流程10:
肥胖药物治疗概要(图10)
肥胖治疗在糖尿病管理中占据重要地位。在选择药物时,应充分考虑不良反应及禁忌证,并结合患者具体情况制定个体化方案。

图10.常用减重药物的特征
流程11:
疫苗接种建议(图11)
糖尿病患者感染风险较高,因此疫苗接种是综合管理的重要组成部分。应按照推荐完成流感、肺炎球菌及新冠疫苗接种。对于特定年龄人群,还应补充带状疱疹、RSV及Tdap疫苗,以进一步降低感染相关风险。
临床实践中,应在每次就诊中评估疫苗接种情况,并进行推荐、接种及记录,以实现规范化管理。

图11.成人糖尿病疫苗接种建议流程
结语
总体而言,2026版更新在延续既往框架的基础上,进一步明确了生活方式干预与超重/肥胖管理的核心地位,强化动脉粥样硬化危险因素的综合控制,并通过新增糖尿病分类流程完善诊断路径;同时基于最新循证证据,持续推动诊疗思路从单纯控糖转向以合并症与并发症为中心,以指导药物选择与长期管理策略。尽管如此,医疗差异、新型药物可及性及费用问题仍是实现最优治疗的重要挑战。
参考文献
1.Samson SL, et al. American Association of Clinical Endocrinology Consensus Statement: Algorithm for Management of Adults With Type 2 Diabetes-2026 Update. Endocr Pract. 2026 Mar 17:S1530-891X(26)00022-4. doi: 10.1016/j.eprac.2026.01.006. Epub ahead of print. PMID: 41842862. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言