编者按:最新数据显示,48.0%的中国2型糖尿病(T2DM)患者存在空腹血糖(FPG)与餐后血糖(PPG)双高,而超半数患者正受困于PPG的飙升[1]。餐后高血糖犹如横亘在T2DM患者血糖达标之路上的“隐形高峰”,不仅导致血糖波动加剧,还会加速糖尿病病程进展、增加并发症风险。研究证实,餐后高血糖是中国人群发生心血管疾病(CVD)、肿瘤及全因死亡的独立危险因素[2]。从血糖异常波动到多系统并发症,这一连锁反应严重影响患者的长期预后和生活质量。
直面“中国式血糖”
为何餐后血糖问题更为突出?
餐后高血糖已成为中国T2DM人群血糖异常的重要特征,显著区别于西方人群[3-4]。特别是在口服降糖药(OADs)控制不佳、需要启动注射治疗的T2DM患者中,东亚(中国)患者的PPG水平更高、血糖漂移(即血糖波动)幅度更大[4]。中国人群餐后高血糖高发,主要源于三大关键因素:
其一,先天“控糖短板”:中国人群胰岛β细胞功能较差、胰岛素抵抗更显著。随着T2DM病程进展,β细胞功能衰退较西方人群更显著,尤以早相胰岛素分泌缺失或延迟为典型表现,直接推高了PPG峰值[5-7]。同时,在相同体重指数(BMI)水平下,中国人群也更容易出现内脏脂肪蓄积,这进一步加重胰岛素抵抗,从而助推PPG升高[8-10]。
其二,隐形“加速器”:胃排空速度更快。研究显示,中国T2DM患者胃排空速度显著快于西方人群(3.4 vs. 2.7 kcal/min,P<0.05),胃半排空时间(T50)明显缩短,整体胃排空速度加快约20%。胃排空加速会让餐后葡萄糖更快进入小肠并被吸收,从而导致PPG峰值更高(8.1 vs. 5.9 mmol/L,P<0.05)[11]。

其三,生活方式“催化剂”:高糖高油饮食、久坐少动、作息紊乱等不良习惯,进一步加剧血糖波动。中国人群饮食以碳水化合物为主,约82.2%的人以精制米面为主食,膳食升糖指数偏高,易引发PPG明显升高[12-13]。加之,体力活动不足、作息不规律、外卖消费增加等现代生活方式,进一步加剧了餐后高血糖风险[14]。
多重因素交织叠加,致使餐后高血糖成为中国T2DM患者的突出特征,也成为制约整体血糖达标的关键瓶颈。要突破这一困局,必须深入揭示其背后的病理生理机制,识别关键干预靶点,为制定个体化精准治疗策略奠定基础。
核心机制解密
胰岛β细胞功能基础上的肠促胰素效应
正常生理状态下PPG通过“肠促胰素-胰岛素-外周组织”的协同作用得到精细调控:进食后,肠道分泌胰高糖素样肽-1(GLP-1)和葡萄糖浓度依赖性促胰岛素释放多肽(GIP),促进胰腺分泌胰岛素并抑制胰高血糖素;胰岛素则作用于肝脏、骨骼肌和脂肪组织,促进葡萄糖摄取、糖原合成和脂肪合成,抑制葡萄糖生成及脂肪分解;同时,GLP-1还可延缓胃排空,并通过中枢神经系统抑制食欲。这一多层次的协调机制,共同维持PPG在生理范围内[15]。

然而在T2DM患者中,这一“精密调控网络”逐渐失衡。其中,胰岛β细胞功能衰退和肠促胰素效应减弱是推动PPG升高的两大核心机制,即β细胞功能下降为PPG升高奠定基础,而肠促胰素效应减弱则进一步放大这一过程。二者之间相互影响:一方面,肠促胰素效应减弱会加速β细胞功能衰退;另一方面,持续高血糖及血脂紊乱又会损伤肠道L细胞分泌GLP-1的能力,从而形成恶性循环[16]。
值得注意的是,肠促胰素效应的减弱还会影响胃排空调节。研究表明,胃排空可贡献约30%~40%的PPG升高,是影响PPG的关键决定因素[17]。在肠促胰素中,GLP-1可通过迷走神经等神经通路延缓胃排空,减缓碳水化合物吸收以避免PPG骤升;而GIP受体因在相关神经和胃组织中的表达很低,故GIP无类似的胃排空调节作用。
基于上述机制,以GLP-1受体激动剂(GLP-1RA)为核心的治疗策略应运而生,并在此基础上进一步演进为更具协同效应的基础胰岛素/GLP-1RA固定比例复方制剂(FRC)方案。其中,甘精胰岛素利司那肽(简称甘精利司)因其短效GLP-1RA成分对胃排空的延缓作用更强,与中国患者“胃排空更快”的特点高度契合,具备兼顾FPG和PPG的独特优势,可实现更精准、全面的血糖管理。
破局之道
协同构筑中国糖尿病综合管理新防线
随着对T2DM病理生理机制认识的不断深入,餐后高血糖的治疗策略也在持续演进。从单一机制干预到多机制协同控制,正逐渐成为改善PPG、推动整体血糖达标的重要突破方向。
01、短效GLP-1RA的独特优势:给胃排空装上“缓释阀”
GLP-1RA根据作用时程可分为短效与长效两类。两者均可通过作用于中枢神经系统抑制食欲,但在胃排空调节方面存在显著差异。
短效GLP-1RA能够通过抑制胃蠕动、延缓胃排空以及减少幽门部食物流动,从而减缓碳水化合物进入小肠的速度,降低PPG峰值。
长效GLP-1RA在延缓胃排空方面更容易出现耐受现象,这可能与其长期维持较高血药浓度所导致的快速适应有关[18-19]。
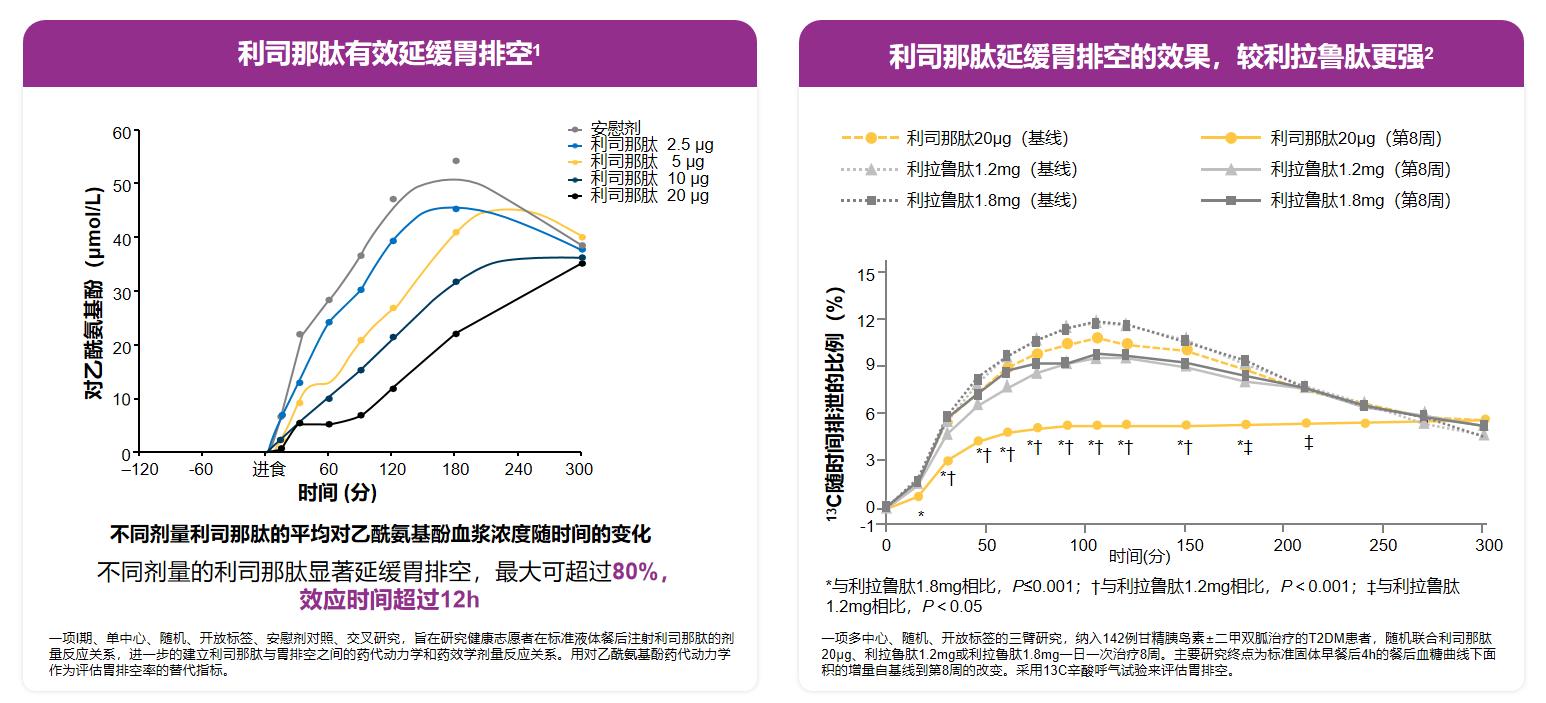
作为独特的短效GLP-1RA,利司那肽在延缓胃排空方面表现尤为突出。其不仅可使胃排空最大延缓超过80%,而且作用持续时间超过12小时[20]。多中心随机研究显示,与其他GLP-1RA相比,利司那肽对胃排空的延缓作用更为显著[21]。此外,即使在胰腺切除术后患者中,利司那肽仍可通过延缓胃排空降低PPG,提示其作用并不完全依赖β细胞功能[22]。
02、FRC“1+1>2”协同升级:空腹+餐后全面掌控
在此基础上,FRC依托双效成分机制互补,覆盖T2DM的多重病理生理缺陷,实现血糖控制的全面提升:
GLP-1RA:纠正肠促胰素效应减弱,促进胰岛素分泌并延缓胃排空等,起到“削峰去谷”的作用,即降低PPG峰值、减少胰岛素治疗的低血糖风险。
基础胰岛素:补充胰岛素,弥补β细胞功能不足,主要改善FPG,维持基础血糖稳定。
二者协同,不仅进一步增强了对PPG的控制,更实现了对FPG与PPG的全面/综合管理。
在目前临床应用的FRC中,甘精利司是由长效基础胰岛素甘精胰岛素与短效GLP-1RA利司那肽组成,得益于利司那肽更强的延缓胃排空作用,甘精利司在稳控24 h血糖的同时,可显著强化三餐后血糖控制。同时,甘精利司有两种规格(1 U:1 μg与2 U:1 μg),以优势配比为中国糖尿病患者量身定制,确保不同患者均能够获得足量的GLP-1RA[23-24],从而帮助获得更好的FPG和PPG控制。
03、循证铸章:甘精利司精准适配中国患者需求
多项中国人群RCT研究证实,FRC可进一步优化既往OADs或胰岛素治疗不佳患者的血糖管理,甘精利司在PPG改善上优势尤为突出[25-29],具体而言:
OADs控制不佳患者:甘精利司可显著降低PPG漂移达4.7 mmol/L,相较基础胰岛素不增加低血糖风险、兼具体重获益;HbA1c及各餐次PPG均值改善优于预混胰岛素[25,27]。
基础胰岛素±OADs控制不佳患者:转换为甘精利司,较增加基础胰岛素剂量进一步降低HbA1c、提升达标率、带来体重获益,PPG漂移降幅达5.1 mmol/L[28]。
与此同时,甘精利司亦显示出良好的安全性,其胃肠道不良反应多为轻度、一过性,患者整体耐受性良好。作为含GLP-1RA组分的复方制剂,其通过1剂量单位阶梯式调整,可显著降低胃肠道不良反应的发生风险[23-24,30]。这一优势可显著提高患者治疗接受度和依从性,进而更利于临床持续、规范使用,助力实现血糖的长期平稳管理。
总 结
餐后高血糖是中国T2DM患者的“特色难题”,受β细胞功能衰退、肠促胰素效应减弱、胃排空加快以及生活方式等多重因素共同驱动。基于中国人群独特的病理生理特征,临床亟需更精准、更契合此类人群需求的治疗方案。
创新FRC方案甘精利司,不仅全面覆盖导致“中国式血糖”的多重病理机制,更以丰富的中国人群循证数据,验证了其在有效性、安全性及全面血糖管理方面的独特价值,尤其在改善PPG方面表现出显著优势[25]。
从“追本溯源”的机制解析,到“立足国人”的精准适配,再到“循证赋能”的临床验证,精准治疗策略的不断完善正推动餐后高血糖管理迈向新高度,为中国T2DM患者提供更全面、更可持续的血糖管理解决方案。
参考文献:
[1]Zhang Q, et al. Diabetes Ther 2024, 16(1):1-14.
[2]Lu J, et al. Diabetes Care. 2019 Aug;42(8):1539-1548.
[3]母义明, 等. 中国2型糖尿病患者餐后高血糖管理专家共识[J].中国糖尿病杂志,2016,24(5):385-392.
[4]Zhang XM, et al. Diabetes Metab Res Rev 2018,34(8):e3062.
[5]Chen Y, et al. Rev Endocr Metab Disord 2025,26(1):31-53.
[6]张俊清, 等. 不同糖耐量人群胰岛素抵抗和胰岛β细胞功能减退的差异. 中国糖尿病杂志 2008,16(2):68-71.
[7]高妍. 关注胰岛素早相分泌的重要性. 中国糖尿病杂志 2011,19(5):384-386.
[8]He W, et al. PLoS One 2013,8(3):e58688.
[9]吴鸿,刘连勇,吴光雨,等. 内脏脂肪、异位脂肪与2型糖尿病:证据和假说. 中华糖尿病杂志,2025,17(07):919-925. DOI:10.3760/cma.j.cn115791-20241014-00615.
[10]Janssen JAMJL. International Journal of Molecular Sciences. 2025,26(18):9191.
[11]Wang X, et al. Diabetes Res Clin Pract. 2020 Jan;159:107951.
[12]陶利,等.营养与糖尿病并发症——达能营养中心第十六届学术会议论文集.2013.
[13]Miller V, et al. Lancet Diabetes Endocrinol 2024,12(5):330-338.
[14]Peng W, et al. Lancet Reg Health West Pac. 2024, 43:100809.
[15]Dimitriadis GD, et al. Nutrients. 2021 Jan 6;13(1):159.
[16]潘琦,郭立新.胰高糖素样肽-1 受体激动剂的 发展历程和临床应用进展[J].Chinese Journal of Diabetes Mellitus, 2022,14(12).DOI:10.3760/cma.j.cn115791-20220802-00375.
[17]De Fano M, et al. Diabetes Res Clin Pract. 2023 Sep;203:110828.
[18]Meier JJ. et al. Nat Rev Endocrinol, 2012, 8(12): 728-742.
[19]Jelsing J, et al. Diabetes Obes Metab, 2012, 14(6): 531-538.
[20]Becker RH, et al. Diabetes Metab Res Rev 2015,31(6):610-618.
[21]Meier JJ, et al. Diabetes Care. 2015 Jul;38(7):1263-73.
[22]Juel CTB, et al. Diabetologia. 2020 Jul;63(7):1285-1298.
[23]甘精胰岛素利司那肽注射液(Ⅰ)说明书.
[24]甘精胰岛素利司那肽注射液(Ⅱ)说明书.
[25]Yang W, et al. Diabetes Obes Metab. 2022,24(8):1522-1533.
[26]Wang W, et al. J Diabetes 2022 Jun;14(6):401-413.
[27]1988-LB - lmpact of Time of lnjecion Comparing iGlarLixi vs. iDegAsp in Chinese People with Type 2 Diabetes--Exploratory Analysis of the SoliD Study. ADA 2025.
[28]Yuan X, et al. Diabetes Obes Metab. 2022,24(11):2182-2191.
[29]Pei Y, et al. Diabetes Obes Metab .2021 Dec;23(12):2687-2696.
[30]Rosenstock J, et al. Diabetes Care 2016,39(11):2026-2035. 2 comments
那么,为何中国T2DM患者PPG问题尤为突出?本期中山大学附属第一医院李延兵教授和华中科技大学同济医学院附属协和医院陈璐璐教授将带领我们一同揭开“中国式”餐后高血糖背后的深层机制,并深入探讨创新治疗方案的精准干预策略,为临床实践提供破局新思路。

直面“中国式血糖”
为何餐后血糖问题更为突出?
餐后高血糖已成为中国T2DM人群血糖异常的重要特征,显著区别于西方人群[3-4]。特别是在口服降糖药(OADs)控制不佳、需要启动注射治疗的T2DM患者中,东亚(中国)患者的PPG水平更高、血糖漂移(即血糖波动)幅度更大[4]。中国人群餐后高血糖高发,主要源于三大关键因素:
其一,先天“控糖短板”:中国人群胰岛β细胞功能较差、胰岛素抵抗更显著。随着T2DM病程进展,β细胞功能衰退较西方人群更显著,尤以早相胰岛素分泌缺失或延迟为典型表现,直接推高了PPG峰值[5-7]。同时,在相同体重指数(BMI)水平下,中国人群也更容易出现内脏脂肪蓄积,这进一步加重胰岛素抵抗,从而助推PPG升高[8-10]。
其二,隐形“加速器”:胃排空速度更快。研究显示,中国T2DM患者胃排空速度显著快于西方人群(3.4 vs. 2.7 kcal/min,P<0.05),胃半排空时间(T50)明显缩短,整体胃排空速度加快约20%。胃排空加速会让餐后葡萄糖更快进入小肠并被吸收,从而导致PPG峰值更高(8.1 vs. 5.9 mmol/L,P<0.05)[11]。

其三,生活方式“催化剂”:高糖高油饮食、久坐少动、作息紊乱等不良习惯,进一步加剧血糖波动。中国人群饮食以碳水化合物为主,约82.2%的人以精制米面为主食,膳食升糖指数偏高,易引发PPG明显升高[12-13]。加之,体力活动不足、作息不规律、外卖消费增加等现代生活方式,进一步加剧了餐后高血糖风险[14]。
多重因素交织叠加,致使餐后高血糖成为中国T2DM患者的突出特征,也成为制约整体血糖达标的关键瓶颈。要突破这一困局,必须深入揭示其背后的病理生理机制,识别关键干预靶点,为制定个体化精准治疗策略奠定基础。
核心机制解密
胰岛β细胞功能基础上的肠促胰素效应
正常生理状态下PPG通过“肠促胰素-胰岛素-外周组织”的协同作用得到精细调控:进食后,肠道分泌胰高糖素样肽-1(GLP-1)和葡萄糖浓度依赖性促胰岛素释放多肽(GIP),促进胰腺分泌胰岛素并抑制胰高血糖素;胰岛素则作用于肝脏、骨骼肌和脂肪组织,促进葡萄糖摄取、糖原合成和脂肪合成,抑制葡萄糖生成及脂肪分解;同时,GLP-1还可延缓胃排空,并通过中枢神经系统抑制食欲。这一多层次的协调机制,共同维持PPG在生理范围内[15]。

然而在T2DM患者中,这一“精密调控网络”逐渐失衡。其中,胰岛β细胞功能衰退和肠促胰素效应减弱是推动PPG升高的两大核心机制,即β细胞功能下降为PPG升高奠定基础,而肠促胰素效应减弱则进一步放大这一过程。二者之间相互影响:一方面,肠促胰素效应减弱会加速β细胞功能衰退;另一方面,持续高血糖及血脂紊乱又会损伤肠道L细胞分泌GLP-1的能力,从而形成恶性循环[16]。
值得注意的是,肠促胰素效应的减弱还会影响胃排空调节。研究表明,胃排空可贡献约30%~40%的PPG升高,是影响PPG的关键决定因素[17]。在肠促胰素中,GLP-1可通过迷走神经等神经通路延缓胃排空,减缓碳水化合物吸收以避免PPG骤升;而GIP受体因在相关神经和胃组织中的表达很低,故GIP无类似的胃排空调节作用。
基于上述机制,以GLP-1受体激动剂(GLP-1RA)为核心的治疗策略应运而生,并在此基础上进一步演进为更具协同效应的基础胰岛素/GLP-1RA固定比例复方制剂(FRC)方案。其中,甘精胰岛素利司那肽(简称甘精利司)因其短效GLP-1RA成分对胃排空的延缓作用更强,与中国患者“胃排空更快”的特点高度契合,具备兼顾FPG和PPG的独特优势,可实现更精准、全面的血糖管理。
破局之道
协同构筑中国糖尿病综合管理新防线
随着对T2DM病理生理机制认识的不断深入,餐后高血糖的治疗策略也在持续演进。从单一机制干预到多机制协同控制,正逐渐成为改善PPG、推动整体血糖达标的重要突破方向。
01、短效GLP-1RA的独特优势:给胃排空装上“缓释阀”
GLP-1RA根据作用时程可分为短效与长效两类。两者均可通过作用于中枢神经系统抑制食欲,但在胃排空调节方面存在显著差异。
短效GLP-1RA能够通过抑制胃蠕动、延缓胃排空以及减少幽门部食物流动,从而减缓碳水化合物进入小肠的速度,降低PPG峰值。
长效GLP-1RA在延缓胃排空方面更容易出现耐受现象,这可能与其长期维持较高血药浓度所导致的快速适应有关[18-19]。
作为独特的短效GLP-1RA,利司那肽在延缓胃排空方面表现尤为突出。其不仅可使胃排空最大延缓超过80%,而且作用持续时间超过12小时[20]。多中心随机研究显示,与其他GLP-1RA相比,利司那肽对胃排空的延缓作用更为显著[21]。此外,即使在胰腺切除术后患者中,利司那肽仍可通过延缓胃排空降低PPG,提示其作用并不完全依赖β细胞功能[22]。

02、FRC“1+1>2”协同升级:空腹+餐后全面掌控
在此基础上,FRC依托双效成分机制互补,覆盖T2DM的多重病理生理缺陷,实现血糖控制的全面提升:
GLP-1RA:纠正肠促胰素效应减弱,促进胰岛素分泌并延缓胃排空等,起到“削峰去谷”的作用,即降低PPG峰值、减少胰岛素治疗的低血糖风险。
基础胰岛素:补充胰岛素,弥补β细胞功能不足,主要改善FPG,维持基础血糖稳定。
二者协同,不仅进一步增强了对PPG的控制,更实现了对FPG与PPG的全面/综合管理。
在目前临床应用的FRC中,甘精利司是由长效基础胰岛素甘精胰岛素与短效GLP-1RA利司那肽组成,得益于利司那肽更强的延缓胃排空作用,甘精利司在稳控24 h血糖的同时,可显著强化三餐后血糖控制。同时,甘精利司有两种规格(1 U:1 μg与2 U:1 μg),以优势配比为中国糖尿病患者量身定制,确保不同患者均能够获得足量的GLP-1RA[23-24],从而帮助获得更好的FPG和PPG控制。
03、循证铸章:甘精利司精准适配中国患者需求
多项中国人群RCT研究证实,FRC可进一步优化既往OADs或胰岛素治疗不佳患者的血糖管理,甘精利司在PPG改善上优势尤为突出[25-29],具体而言:
OADs控制不佳患者:甘精利司可显著降低PPG漂移达4.7 mmol/L,相较基础胰岛素不增加低血糖风险、兼具体重获益;HbA1c及各餐次PPG均值改善优于预混胰岛素[25,27]。
基础胰岛素±OADs控制不佳患者:转换为甘精利司,较增加基础胰岛素剂量进一步降低HbA1c、提升达标率、带来体重获益,PPG漂移降幅达5.1 mmol/L[28]。
与此同时,甘精利司亦显示出良好的安全性,其胃肠道不良反应多为轻度、一过性,患者整体耐受性良好。作为含GLP-1RA组分的复方制剂,其通过1剂量单位阶梯式调整,可显著降低胃肠道不良反应的发生风险[23-24,30]。这一优势可显著提高患者治疗接受度和依从性,进而更利于临床持续、规范使用,助力实现血糖的长期平稳管理。
总 结
餐后高血糖是中国T2DM患者的“特色难题”,受β细胞功能衰退、肠促胰素效应减弱、胃排空加快以及生活方式等多重因素共同驱动。基于中国人群独特的病理生理特征,临床亟需更精准、更契合此类人群需求的治疗方案。
创新FRC方案甘精利司,不仅全面覆盖导致“中国式血糖”的多重病理机制,更以丰富的中国人群循证数据,验证了其在有效性、安全性及全面血糖管理方面的独特价值,尤其在改善PPG方面表现出显著优势[25]。
从“追本溯源”的机制解析,到“立足国人”的精准适配,再到“循证赋能”的临床验证,精准治疗策略的不断完善正推动餐后高血糖管理迈向新高度,为中国T2DM患者提供更全面、更可持续的血糖管理解决方案。
参考文献:
[1]Zhang Q, et al. Diabetes Ther 2024, 16(1):1-14.
[2]Lu J, et al. Diabetes Care. 2019 Aug;42(8):1539-1548.
[3]母义明, 等. 中国2型糖尿病患者餐后高血糖管理专家共识[J].中国糖尿病杂志,2016,24(5):385-392.
[4]Zhang XM, et al. Diabetes Metab Res Rev 2018,34(8):e3062.
[5]Chen Y, et al. Rev Endocr Metab Disord 2025,26(1):31-53.
[6]张俊清, 等. 不同糖耐量人群胰岛素抵抗和胰岛β细胞功能减退的差异. 中国糖尿病杂志 2008,16(2):68-71.
[7]高妍. 关注胰岛素早相分泌的重要性. 中国糖尿病杂志 2011,19(5):384-386.
[8]He W, et al. PLoS One 2013,8(3):e58688.
[9]吴鸿,刘连勇,吴光雨,等. 内脏脂肪、异位脂肪与2型糖尿病:证据和假说. 中华糖尿病杂志,2025,17(07):919-925. DOI:10.3760/cma.j.cn115791-20241014-00615.
[10]Janssen JAMJL. International Journal of Molecular Sciences. 2025,26(18):9191.
[11]Wang X, et al. Diabetes Res Clin Pract. 2020 Jan;159:107951.
[12]陶利,等.营养与糖尿病并发症——达能营养中心第十六届学术会议论文集.2013.
[13]Miller V, et al. Lancet Diabetes Endocrinol 2024,12(5):330-338.
[14]Peng W, et al. Lancet Reg Health West Pac. 2024, 43:100809.
[15]Dimitriadis GD, et al. Nutrients. 2021 Jan 6;13(1):159.
[16]潘琦,郭立新.胰高糖素样肽-1 受体激动剂的 发展历程和临床应用进展[J].Chinese Journal of Diabetes Mellitus, 2022,14(12).DOI:10.3760/cma.j.cn115791-20220802-00375.
[17]De Fano M, et al. Diabetes Res Clin Pract. 2023 Sep;203:110828.
[18]Meier JJ. et al. Nat Rev Endocrinol, 2012, 8(12): 728-742.
[19]Jelsing J, et al. Diabetes Obes Metab, 2012, 14(6): 531-538.
[20]Becker RH, et al. Diabetes Metab Res Rev 2015,31(6):610-618.
[21]Meier JJ, et al. Diabetes Care. 2015 Jul;38(7):1263-73.
[22]Juel CTB, et al. Diabetologia. 2020 Jul;63(7):1285-1298.
[23]甘精胰岛素利司那肽注射液(Ⅰ)说明书.
[24]甘精胰岛素利司那肽注射液(Ⅱ)说明书.
[25]Yang W, et al. Diabetes Obes Metab. 2022,24(8):1522-1533.
[26]Wang W, et al. J Diabetes 2022 Jun;14(6):401-413.
[27]1988-LB - lmpact of Time of lnjecion Comparing iGlarLixi vs. iDegAsp in Chinese People with Type 2 Diabetes--Exploratory Analysis of the SoliD Study. ADA 2025.
[28]Yuan X, et al. Diabetes Obes Metab. 2022,24(11):2182-2191.
[29]Pei Y, et al. Diabetes Obes Metab .2021 Dec;23(12):2687-2696.
[30]Rosenstock J, et al. Diabetes Care 2016,39(11):2026-2035. 2 comments











 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言