编者按
作为新型非甾体类盐皮质激素受体拮抗剂(nsMRA),非奈利酮在糖尿病合并慢性肾脏病(CKD)领域的应用价值持续引发学界关注。今年美国糖尿病协会科学年会(ADA 2025)公布的CONFIDENCE研究亚组分析、肾脏标志物研究及FINE-ONE研究的基线特征3项研究,从不同维度进一步丰富了非奈利酮的研究数据,拓展了对该药物心肾保护作用及机制的认知,为糖尿病肾脏疾病(DKD)患者的临床决策提供了更精细化的证据支持。本刊特邀北京医院潘琦教授对这3项研究进行深入解读。
CONFIDENCE研究亚组:对于基线不同血糖水平的T2D合并CKD患者,联合治疗均可显著降低UACR
本月初正式发布的CONFIDENCE研究首次回答了心肾保护药物非奈利酮和钠-葡萄糖协调转运蛋白2抑制剂(SGLT2i)联合应用的疗效和安全性问题,为心肾获益药物的应用策略提供了里程碑式证据。该研究证实,对于T2D合并CKD患者,相较任一单药治疗,非奈利酮与恩格列净同步起始联合使用更能显著降低白蛋白尿水平,相关结果已发表于《新英格兰医学杂志》[1]。CONFIDENCE研究的血糖亚组分析[2]刚刚在ADA年会公布,旨在评估基线糖化血红蛋白(HbA1c)水平是否影响联合治疗效果。
研究设计与背景
CONFIDENCE研究中,CKD定义为估算肾小球滤过率(eGFR)30~90 ml/min/1.73 m2、尿白蛋白肌酐比值(UACR)≥100~<5000 mg/g、HbA1c<11%。受试者按1:1:1随机分配至非奈利酮(10 mg/d或20 mg/d)+安慰剂、恩格列净(10 mg/d)+安慰剂、非奈利酮(10 mg/d或20 mg/d)+恩格列净(10 mg/d)治疗组。本次亚组分析按基线HbA1c水平对患者进行四分位数分组,分析HbA1c较基线的变化,同时评估第180天UACR较基线的相对变化,旨在评估基线血糖水平对联合治疗疗效的影响。
关键结果数据
基线特征
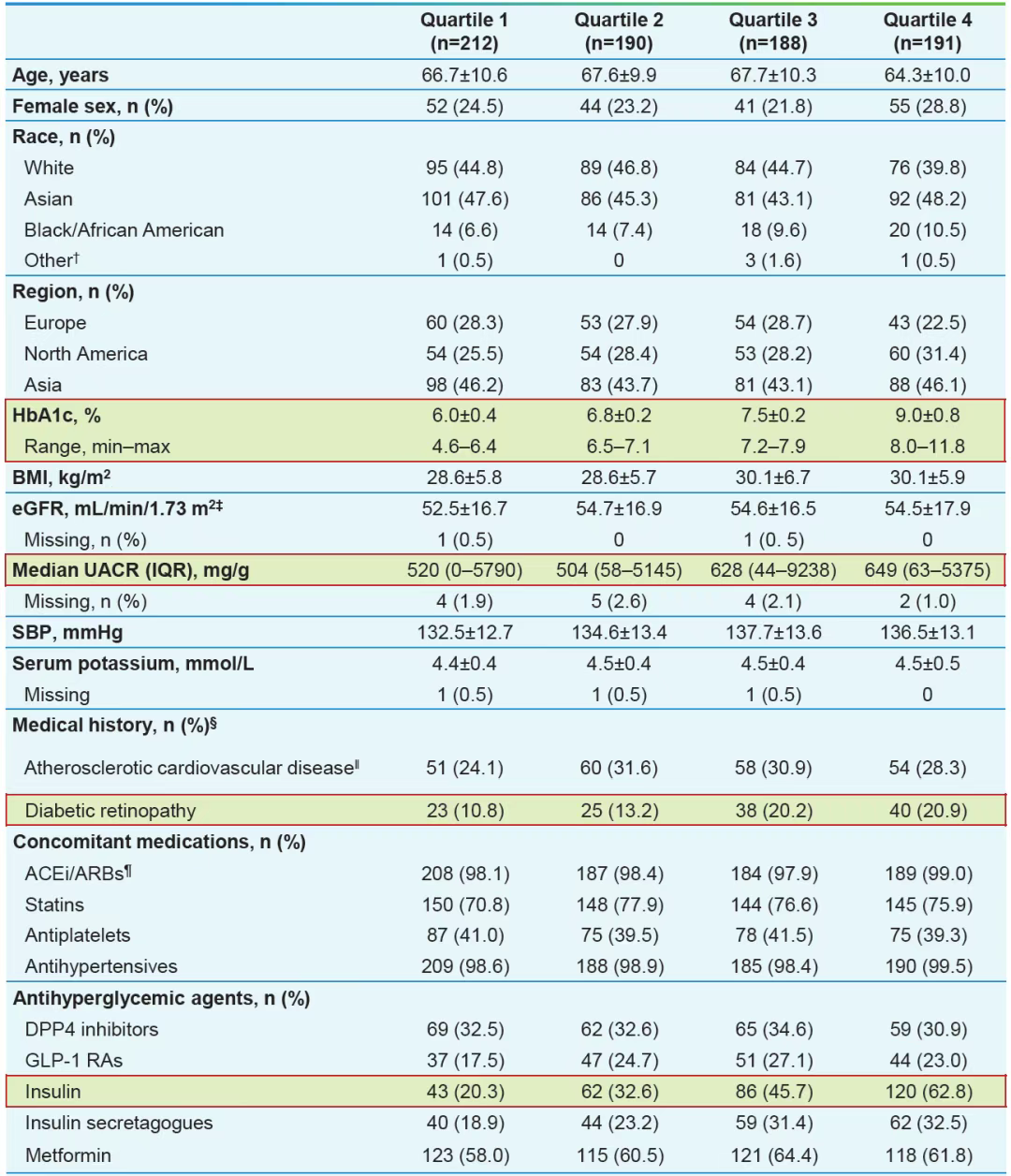
2022年6月~2024年8月,共有来自14个国家/地区818例患者被随机分组,其中800例纳入全分析集。基线平均eGFR 54.2 ml/min/1.73m2,中位UACR 579 mg/g,781例受试者的平均HbA1c为7.3%。按基线HbA1c水平对患者进行四分位数分组(Q1,≤6.4%;Q2,>6.4% ~ ≤7.1%;Q3,>7.1% ~ ≤7.9%;Q4,>7.9%),各组人数分别为212例、190例、188例和191例。HbA1c四分位数组间的基线特征基本均衡,部分指标存在差异,其中包括平均HbA1c、中位UACR、糖尿病视网膜病变患病率及胰岛素使用率(表1)。
表1. 按HbA1c四分位数划分的基线人口统计学和临床特征
第180天时,各治疗组之间HbA1c较基线的变化无显著差异,恩格列净组HbA1c较非奈利酮组有下降趋势(图1)。同样地,在每个四分位数组内,各治疗组第180天时HbA1c较基线的变化虽然无统计学差异,但恩格列净组HbA1c较非奈利酮组有更低的趋势,且随基线血糖升高趋势更明显(图2)。
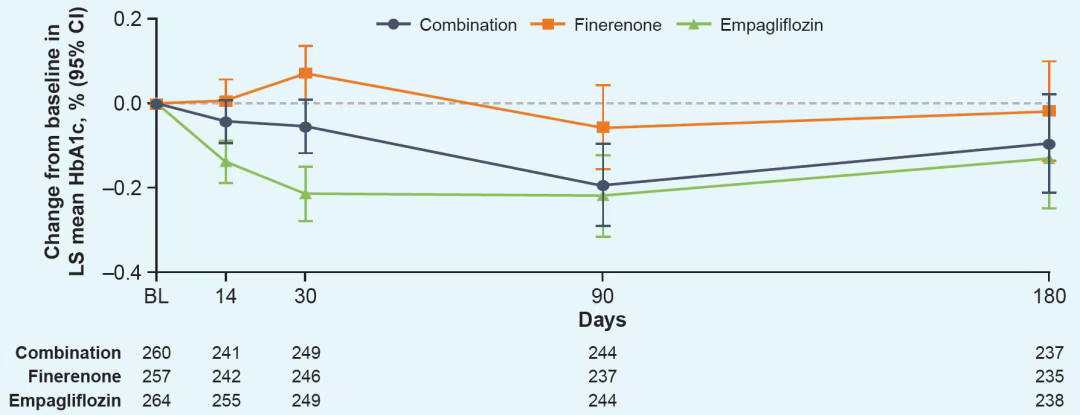
图1. 第180天时,各治疗组之间HbA1c较基线的变化无显著差异
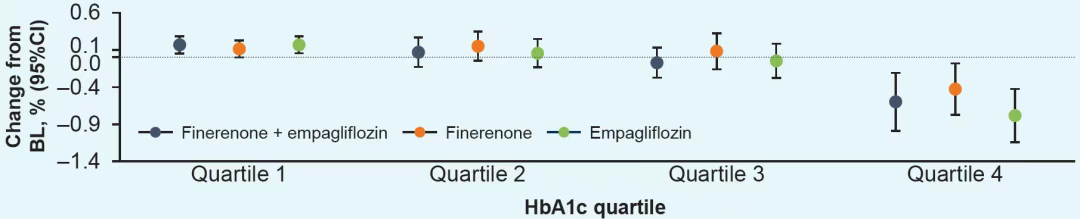
图2. 每个四分位数组内,各治疗组第180天时HbA1c较基线的变化也无差异
UACR变化
联合治疗在所有HbA1c四分位数组中降低UACR的幅度均显著大于单药治疗(图3)。Q1组联合治疗较非奈利酮单药和恩格列净单药分别多降低29%(95%CI:-48% ~ -4%)和38%(95%CI:-54% ~ -15%)(图4);Q3组联合治疗较单药分别多降低36%(95%CI:-54% ~ -10%)和34%(95%CI:-52% ~ -10%)。这种差异在各血糖分层中具有一致性,提示联合治疗的肾脏保护作用不依赖于血糖控制效果(图4)。
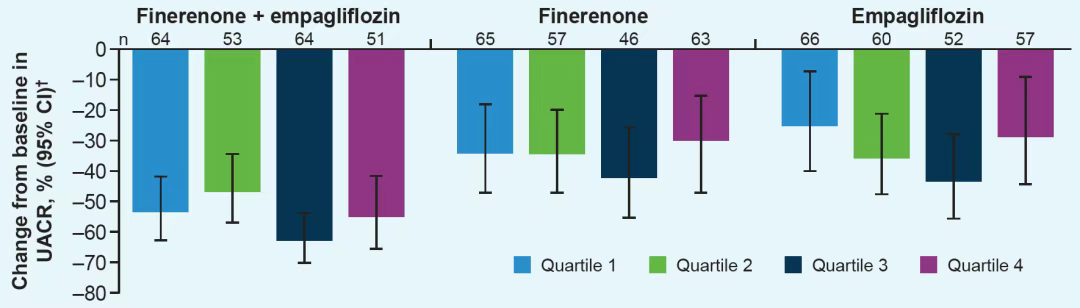
图3. 第180天时HbA1c较基线的最小二乘均数变化
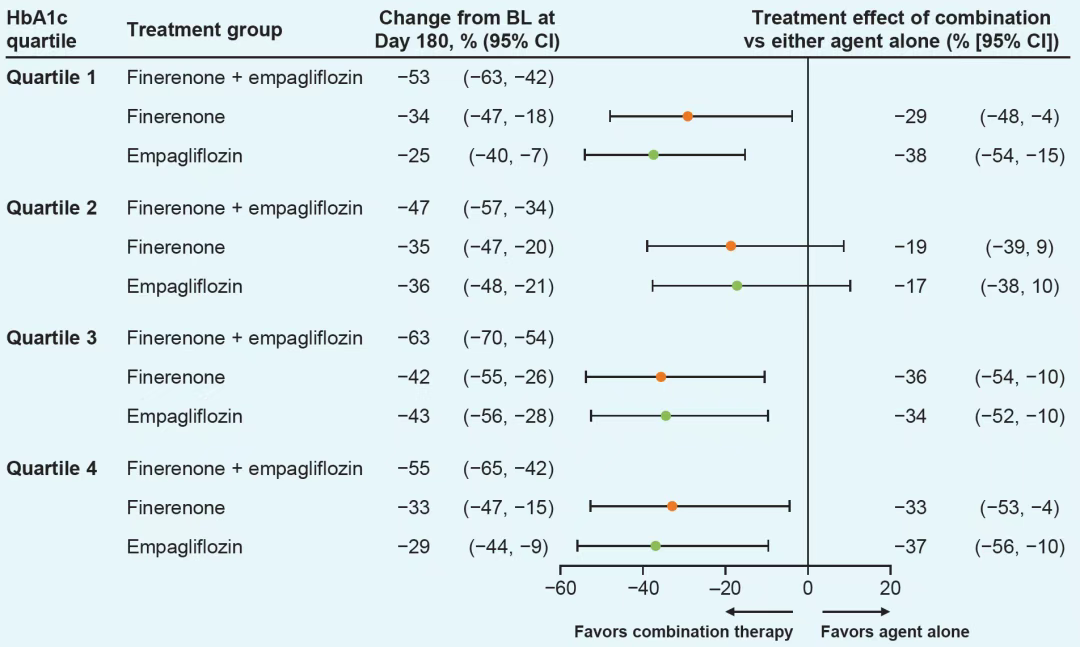
图4. 根据HbA1c四分位数分组,联合治疗相较于任一单药治疗从基线至第180天的UACR百分比变化
该亚组分析证实,非奈利酮与恩格列净联合治疗在不同基线HbA1c水平的T2D合并CKD患者中,均可显著降低UACR,且效果优于单药治疗,为T2D合并CKD患者的心肾保护提供了联合用药的进一步证据。无论基线血糖如何,联合治疗均可比单药治疗提供更多的心肾脏保护获益。
肾脏标志物研究:非奈利酮在优化治疗基础上的额外肾脏保护效应
研究设计与方法
该研究[3]回顾性分析了60例T2D合并CKD(1~3期)患者,所有患者均接受SGLT2i(达格列净)、血管紧张素受体拮抗剂(ARB,缬沙坦或替米沙坦)治疗,血压控制在<130/80 mmHg至少1年,在此基础上加用非奈利酮并随访6个月。定期监测体重、体重指数(BMI)、血压、血脂、高敏C反应蛋白(hs-CRP)、N末端脑钠肽前体(NT-ProBNP)、eGFR(分别基于肌酐和胱抑素C)、血钾及UACR等指标,旨在评估非奈利酮在接受ARB和SGLT2i治疗的DKD(1~3 期)患者中对肾脏标志物的影响。
主要研究结果
基线数据
患者平均年龄60.05±10.21岁,80%患者eGFR>60 ml/min/1.73m2,86.66%患者UACR在30~300 mg/g,平均HbA1c 7.16%±0.169%,基于肌酐的eGFR(eGFRCr) 88.96 ± 33.15 ml/min/1.73m2,基于胱抑素C的eGFR(eGFRCy) 65.2 ± 22.115 ml/min/1.73m2,血钾4.576 ± 0.45 mEq/L,UACR 170.76 ± 241.84 μg/mg,hs-CRP 1.35 ± 1.13 mg/L,NT-ProBNP 106.87 ± 100.68 pg/ml。
基线平均用药剂量
缬沙坦112±39.2 mg,替米沙坦87.43±43.37 mg,非奈利酮12.67±4.43 mg。ARB使用者占66.66%,血管紧张素受体脑啡肽酶抑制剂(ARNI)使用者占33.33%,钙通道阻滞剂(CCB)使用者占33.33%,β受体阻滞剂使用者占30%。
治疗后变化
6个月时,UACR较基线显著降低59.35%(自基线降至101.348±33.93 μg/mg,P<0.001),体重平均下降0.8 kg(P=0.025)。而血压(收缩压降低1.33±1.671 mmHg,P=1;舒张压降低1.9±1.34 mmHg,P=0.486)、HbA1c(变化0.038%±0.105%,P=1)、eGFRCr(降低0.713±2.22 ml/min/1.73m2,P=1)、eGFRCy(降低6.0±3.26 ml/min/1.73m2,P=0.063)、血钾(降低0.007±0.048 mEq/L,P=0.1)及NT-ProBNP(升高11.018±5.69 pg/ml,P=0.174)等指标的变化均无统计学意义。非奈利酮剂量在随访期间增至16.70±4.92 mg,ARB剂量略有调整,但整体用药方案保持稳定。
研究结果显示,在已接受SGLT2i和ARB优化治疗且血压控制达标的T2D合并早期CKD患者中,加用非奈利酮可进一步显著降低UACR,对血糖、血压、eGFR、血钾指标无明显影响。这一结果提示,非奈利酮的肾脏保护作用可能独立于传统降压、降糖及SGLT2i的机制,为临床中已接受标准治疗但仍存在蛋白尿的患者提供了肾脏保护的新选择。值得注意的是,UACR是T2D合并CKD心肾获益的强预测因子,该研究中,在ARB和SGLT2i治疗基础上,UACR降幅仍达59.35%,凸显了非奈利酮在蛋白尿管理和心肾保护中的独特价值。
FINE-ONE研究基线特征:非奈利酮在1型糖尿病合并CKD患者中的探索
1型糖尿病(T1D)患者中约1/3合并CKD,超过半数会出现肾功能显著丧失,近1/4进展至肾衰竭,而目前针对T1D合并CKD的特异性治疗手段有限。FINE-ONE研究旨在评估非奈利酮在T1D合并CKD患者中的疗效与安全性[4]。
研究设计与基线数据
FINE-ONE是一项正在进行的全球Ⅲ期非奈利酮临床研究。研究纳入242例T1D合并CKD患者,要求UACR≥200~<5000 mg/g,eGFR≥25~<90 ml/min/1.73m2,HbA1c<10%,血清钾≤4.8 mmol/L,且正在稳定服用ACEI/ARB。患者按1:1随机分至非奈利酮组(10 mg或20 mg,每日一次)或安慰剂治疗组。主要疗效指标是6个月时UACR相对于基线的变化(治疗结束后停药随访1个月)。值得注意的是,药监部门批准研究采用UACR作为主要终点,认可UACR作为桥接标志物可将FIDELITY研究T2D合并CKD人群的证据转换(“translate”)到FINE-ONE人群。
在研究纳入的242例患者中,大多数为男性(65%),平均年龄51.6岁;最常见地域来自欧洲(50%),其次为北美(34%)和亚洲(16%);86%患者有高血压病史,基线平均血压135.2/77.5 mmHg,超过99%患者使用ACEI/ARB,36%患者使用利尿剂,27%使用β受体阻滞剂;大约1/4患者有心血管疾病史,74%使用他汀;基线平均糖尿病病程32年(表2)。研究排除了在T1D中推荐证据有限的SGLT2i和GLP-1RA使用者。平均eGFR 58.8±19.1 ml/min/1.73m2,48%患者eGFR≥60 ml/min/1.73m2伴蛋白尿;中位UACR 549(299~1191)mg/g,74%患者UACR≥300 mg/g;平均HbA1c 7.6%±1.1%;平均血钾4.6±0.4 mmol/L(图5)。
表2. FINE-ONE基线人口统计学和临床特征
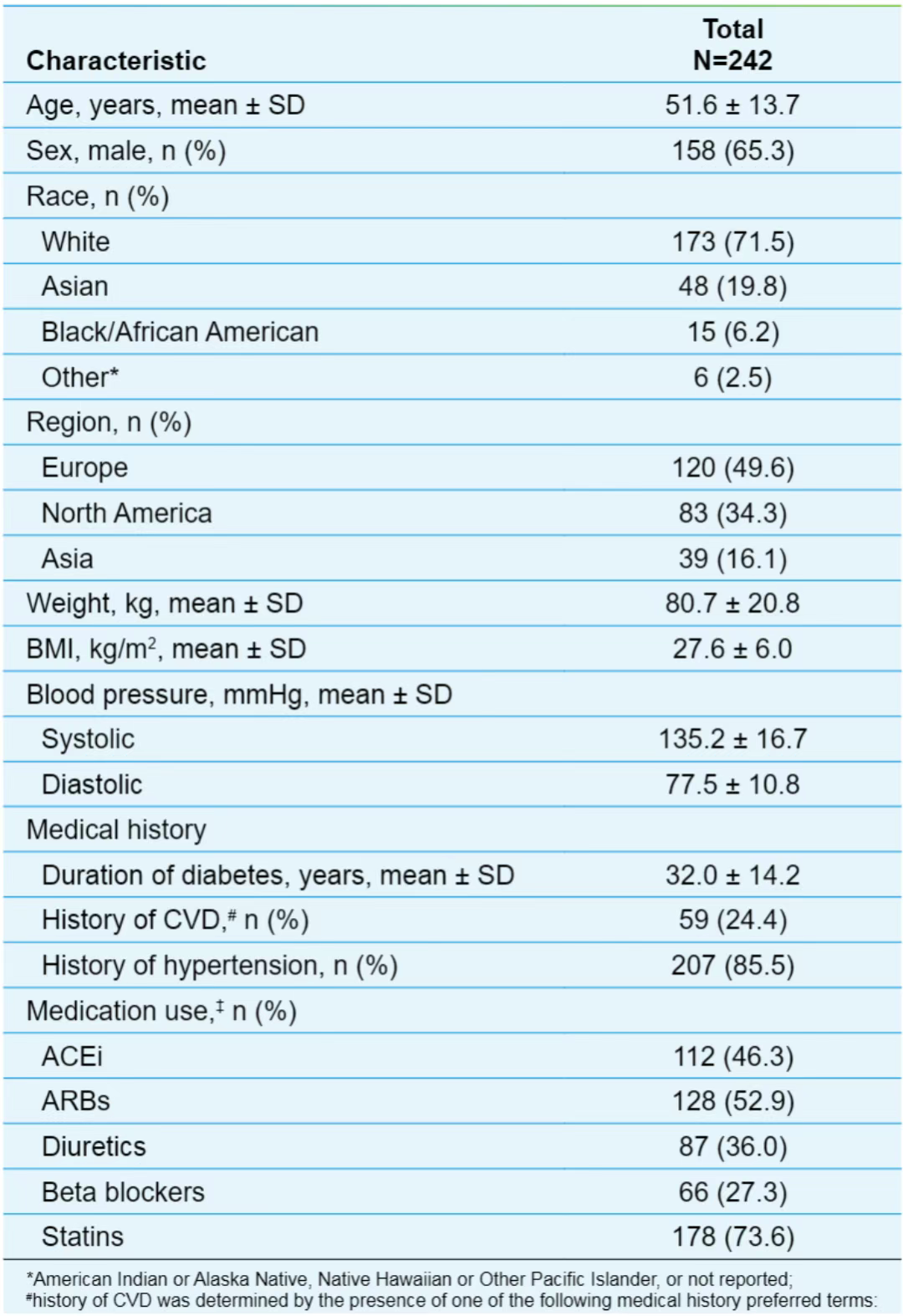
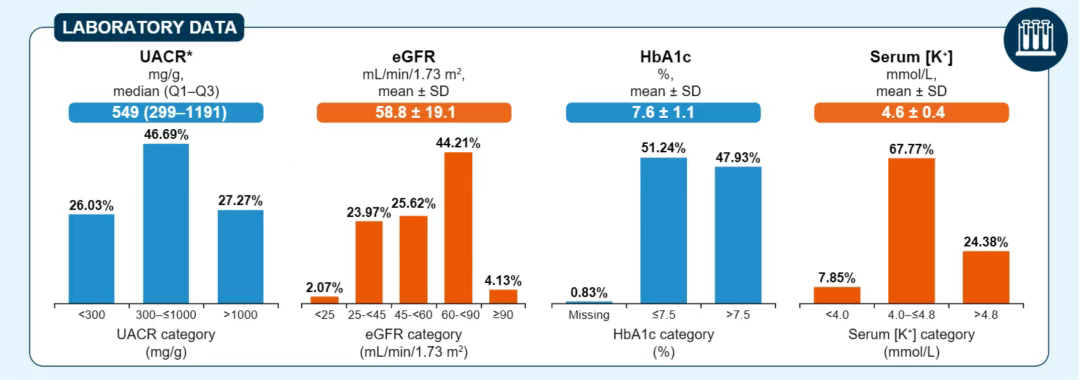
图5. FINE-ONE基线实验室数据
FINE-ONE研究是首个评估非奈利酮用于T1D合并CKD患者的Ⅲ期研究,其基线数据显示入组患者具有较高的肾脏事件风险和心血管共病率。该研究结果将填补非奈利酮在T1D领域的证据空白,若能证实其肾脏保护作用,将为这一缺乏有效治疗手段的患者群体提供新的治疗选择。目前研究仍在进行中,其最终结果值得期待。
专家点评
非奈利酮重塑糖尿病肾脏疾病管理格局
潘琦教授 北京医院
非奈利酮作为新一代nsMRA,ADA今年新公布的3项研究从多维度探索,进一步证实了其在DKD领域的循证价值。
不同血糖水平患者联合治疗的全新证据
CONFIDENCE亚组分析证实,非奈利酮与恩格列净联合治疗在平均HbA1c 6.4%~>7.9%的T2D合并CKD患者中,降低UACR效果均优于单药治疗(如HbA1c>7.9%组联合治疗较单药治疗多降34%~36%)。这一发现证明了在不同血糖水平的T2D合并CKD患者中联合治疗的普适性,不同血糖水平患者均可从非奈利酮与SGLT2i联合治疗方案中获得额外心肾保护收益。
优化治疗基础上的增量保护
真实世界研究显示,T2D合并早期(1~3期)CKD患者,在ARB+SGLT2i治疗基础上,加用非奈利酮仍可使UACR进一步降低59.35%,且安全性良好,对血糖、血压、eGFR和血钾均无显著影响。该结果揭示了其与现有疗法的机制互补性,为早期DKD患者提供蛋白尿和心肾风险管理新手段,其UACR降幅远超传统方案预期,提示非奈利酮在疾病早期的干预价值。
T1D领域的开拓性探索
FINE-ONE研究作为首个针对T1D合并CKD的Ⅲ期临床研究,入组患者呈现高肾病事件风险(中位UACR 549 mg/g)和高心血管共病特征。若证实疗效,将打破该人群治疗手段有限的困境,成为首个代表nsMRA的T1D心肾保护药物。
从独特机制到心肾保护
ADA发布的新研究数据进一步印证非奈利酮独立于血糖、血压、靶向肾脏纤维化的核心优势。作为国内外指南推荐的心肾保护重要支柱治疗药物之一,非奈利酮不断积累新证据,推动早期多机制心肾保护药物治疗,促进糖尿病合并CKD领域的管理迭代,使更多患者尽早获益。
专家简介

潘琦 教授
北京医院内分泌科主任
医学博士,主任医师,教授,博士研究生导师
中华医学会骨质疏松与骨矿盐分会委员
中华医学会糖尿病学分会糖尿病监测与治疗技术学组副组长
中国老年保健研究会老年骨质疏松分会秘书长
中华医学会老年医学分会内分泌学组副组长
北京医学会糖尿病分会副主任委员
“四大慢病”国家科技重大专项首席项目负责人
主持国家省部级课题9项,参与多项国家重大攻关课题、国家自然科学基金等项目
国内外核心期刊发表论文160余篇
《Diabetes Care中文版》《中华医学杂志》《中华内科杂志》《中华老年医学杂志》《中华全科医学杂志》《中国医学前沿》《中国糖尿病杂志》《中国心血管病杂志》编委
参考文献
1. Agarwal R, et al. Finerenone with Empagliflozin in Chronic Kidney Disease and Type 2 Diabetes. N Engl J Med. 2025 Jun 5. doi: 10.1056/NEJMoa2410659.
2. Rajiv Agarwal, et al. Simultaneous Initiation of Finerenone and Empagliflozin Across the Glycemic Spectrum in the CONFIDENCE Trial.2025 ADA.
3. Vishal Gupta, et al. Evaluating the Effect of Finerenone on Renal Markers in Patients with Diabetic Nephropathy (Stage 1–3) Receiving Angiotensin Receptor Blockers and SGLT2i Therapy. 2025 ADA.
4. Hiddo L. Heerspink, et al. Baseline Characteristics for FINE-ONE — A Randomized Phase III Trial Assessing Finerenone in People with T1D and CKD. 2025 ADA.
2 comments
作为新型非甾体类盐皮质激素受体拮抗剂(nsMRA),非奈利酮在糖尿病合并慢性肾脏病(CKD)领域的应用价值持续引发学界关注。今年美国糖尿病协会科学年会(ADA 2025)公布的CONFIDENCE研究亚组分析、肾脏标志物研究及FINE-ONE研究的基线特征3项研究,从不同维度进一步丰富了非奈利酮的研究数据,拓展了对该药物心肾保护作用及机制的认知,为糖尿病肾脏疾病(DKD)患者的临床决策提供了更精细化的证据支持。本刊特邀北京医院潘琦教授对这3项研究进行深入解读。
CONFIDENCE研究亚组:对于基线不同血糖水平的T2D合并CKD患者,联合治疗均可显著降低UACR
本月初正式发布的CONFIDENCE研究首次回答了心肾保护药物非奈利酮和钠-葡萄糖协调转运蛋白2抑制剂(SGLT2i)联合应用的疗效和安全性问题,为心肾获益药物的应用策略提供了里程碑式证据。该研究证实,对于T2D合并CKD患者,相较任一单药治疗,非奈利酮与恩格列净同步起始联合使用更能显著降低白蛋白尿水平,相关结果已发表于《新英格兰医学杂志》[1]。CONFIDENCE研究的血糖亚组分析[2]刚刚在ADA年会公布,旨在评估基线糖化血红蛋白(HbA1c)水平是否影响联合治疗效果。
研究设计与背景
CONFIDENCE研究中,CKD定义为估算肾小球滤过率(eGFR)30~90 ml/min/1.73 m2、尿白蛋白肌酐比值(UACR)≥100~<5000 mg/g、HbA1c<11%。受试者按1:1:1随机分配至非奈利酮(10 mg/d或20 mg/d)+安慰剂、恩格列净(10 mg/d)+安慰剂、非奈利酮(10 mg/d或20 mg/d)+恩格列净(10 mg/d)治疗组。本次亚组分析按基线HbA1c水平对患者进行四分位数分组,分析HbA1c较基线的变化,同时评估第180天UACR较基线的相对变化,旨在评估基线血糖水平对联合治疗疗效的影响。
关键结果数据
基线特征
2022年6月~2024年8月,共有来自14个国家/地区818例患者被随机分组,其中800例纳入全分析集。基线平均eGFR 54.2 ml/min/1.73m2,中位UACR 579 mg/g,781例受试者的平均HbA1c为7.3%。按基线HbA1c水平对患者进行四分位数分组(Q1,≤6.4%;Q2,>6.4% ~ ≤7.1%;Q3,>7.1% ~ ≤7.9%;Q4,>7.9%),各组人数分别为212例、190例、188例和191例。HbA1c四分位数组间的基线特征基本均衡,部分指标存在差异,其中包括平均HbA1c、中位UACR、糖尿病视网膜病变患病率及胰岛素使用率(表1)。
表1. 按HbA1c四分位数划分的基线人口统计学和临床特征

HbA1c变化
第180天时,各治疗组之间HbA1c较基线的变化无显著差异,恩格列净组HbA1c较非奈利酮组有下降趋势(图1)。同样地,在每个四分位数组内,各治疗组第180天时HbA1c较基线的变化虽然无统计学差异,但恩格列净组HbA1c较非奈利酮组有更低的趋势,且随基线血糖升高趋势更明显(图2)。

图1. 第180天时,各治疗组之间HbA1c较基线的变化无显著差异

图2. 每个四分位数组内,各治疗组第180天时HbA1c较基线的变化也无差异
UACR变化
联合治疗在所有HbA1c四分位数组中降低UACR的幅度均显著大于单药治疗(图3)。Q1组联合治疗较非奈利酮单药和恩格列净单药分别多降低29%(95%CI:-48% ~ -4%)和38%(95%CI:-54% ~ -15%)(图4);Q3组联合治疗较单药分别多降低36%(95%CI:-54% ~ -10%)和34%(95%CI:-52% ~ -10%)。这种差异在各血糖分层中具有一致性,提示联合治疗的肾脏保护作用不依赖于血糖控制效果(图4)。

图3. 第180天时HbA1c较基线的最小二乘均数变化

图4. 根据HbA1c四分位数分组,联合治疗相较于任一单药治疗从基线至第180天的UACR百分比变化
该亚组分析证实,非奈利酮与恩格列净联合治疗在不同基线HbA1c水平的T2D合并CKD患者中,均可显著降低UACR,且效果优于单药治疗,为T2D合并CKD患者的心肾保护提供了联合用药的进一步证据。无论基线血糖如何,联合治疗均可比单药治疗提供更多的心肾脏保护获益。
肾脏标志物研究:非奈利酮在优化治疗基础上的额外肾脏保护效应
研究设计与方法
该研究[3]回顾性分析了60例T2D合并CKD(1~3期)患者,所有患者均接受SGLT2i(达格列净)、血管紧张素受体拮抗剂(ARB,缬沙坦或替米沙坦)治疗,血压控制在<130/80 mmHg至少1年,在此基础上加用非奈利酮并随访6个月。定期监测体重、体重指数(BMI)、血压、血脂、高敏C反应蛋白(hs-CRP)、N末端脑钠肽前体(NT-ProBNP)、eGFR(分别基于肌酐和胱抑素C)、血钾及UACR等指标,旨在评估非奈利酮在接受ARB和SGLT2i治疗的DKD(1~3 期)患者中对肾脏标志物的影响。
主要研究结果
基线数据
患者平均年龄60.05±10.21岁,80%患者eGFR>60 ml/min/1.73m2,86.66%患者UACR在30~300 mg/g,平均HbA1c 7.16%±0.169%,基于肌酐的eGFR(eGFRCr) 88.96 ± 33.15 ml/min/1.73m2,基于胱抑素C的eGFR(eGFRCy) 65.2 ± 22.115 ml/min/1.73m2,血钾4.576 ± 0.45 mEq/L,UACR 170.76 ± 241.84 μg/mg,hs-CRP 1.35 ± 1.13 mg/L,NT-ProBNP 106.87 ± 100.68 pg/ml。
基线平均用药剂量
缬沙坦112±39.2 mg,替米沙坦87.43±43.37 mg,非奈利酮12.67±4.43 mg。ARB使用者占66.66%,血管紧张素受体脑啡肽酶抑制剂(ARNI)使用者占33.33%,钙通道阻滞剂(CCB)使用者占33.33%,β受体阻滞剂使用者占30%。
治疗后变化
6个月时,UACR较基线显著降低59.35%(自基线降至101.348±33.93 μg/mg,P<0.001),体重平均下降0.8 kg(P=0.025)。而血压(收缩压降低1.33±1.671 mmHg,P=1;舒张压降低1.9±1.34 mmHg,P=0.486)、HbA1c(变化0.038%±0.105%,P=1)、eGFRCr(降低0.713±2.22 ml/min/1.73m2,P=1)、eGFRCy(降低6.0±3.26 ml/min/1.73m2,P=0.063)、血钾(降低0.007±0.048 mEq/L,P=0.1)及NT-ProBNP(升高11.018±5.69 pg/ml,P=0.174)等指标的变化均无统计学意义。非奈利酮剂量在随访期间增至16.70±4.92 mg,ARB剂量略有调整,但整体用药方案保持稳定。
研究结果显示,在已接受SGLT2i和ARB优化治疗且血压控制达标的T2D合并早期CKD患者中,加用非奈利酮可进一步显著降低UACR,对血糖、血压、eGFR、血钾指标无明显影响。这一结果提示,非奈利酮的肾脏保护作用可能独立于传统降压、降糖及SGLT2i的机制,为临床中已接受标准治疗但仍存在蛋白尿的患者提供了肾脏保护的新选择。值得注意的是,UACR是T2D合并CKD心肾获益的强预测因子,该研究中,在ARB和SGLT2i治疗基础上,UACR降幅仍达59.35%,凸显了非奈利酮在蛋白尿管理和心肾保护中的独特价值。
FINE-ONE研究基线特征:非奈利酮在1型糖尿病合并CKD患者中的探索
1型糖尿病(T1D)患者中约1/3合并CKD,超过半数会出现肾功能显著丧失,近1/4进展至肾衰竭,而目前针对T1D合并CKD的特异性治疗手段有限。FINE-ONE研究旨在评估非奈利酮在T1D合并CKD患者中的疗效与安全性[4]。
研究设计与基线数据
FINE-ONE是一项正在进行的全球Ⅲ期非奈利酮临床研究。研究纳入242例T1D合并CKD患者,要求UACR≥200~<5000 mg/g,eGFR≥25~<90 ml/min/1.73m2,HbA1c<10%,血清钾≤4.8 mmol/L,且正在稳定服用ACEI/ARB。患者按1:1随机分至非奈利酮组(10 mg或20 mg,每日一次)或安慰剂治疗组。主要疗效指标是6个月时UACR相对于基线的变化(治疗结束后停药随访1个月)。值得注意的是,药监部门批准研究采用UACR作为主要终点,认可UACR作为桥接标志物可将FIDELITY研究T2D合并CKD人群的证据转换(“translate”)到FINE-ONE人群。
在研究纳入的242例患者中,大多数为男性(65%),平均年龄51.6岁;最常见地域来自欧洲(50%),其次为北美(34%)和亚洲(16%);86%患者有高血压病史,基线平均血压135.2/77.5 mmHg,超过99%患者使用ACEI/ARB,36%患者使用利尿剂,27%使用β受体阻滞剂;大约1/4患者有心血管疾病史,74%使用他汀;基线平均糖尿病病程32年(表2)。研究排除了在T1D中推荐证据有限的SGLT2i和GLP-1RA使用者。平均eGFR 58.8±19.1 ml/min/1.73m2,48%患者eGFR≥60 ml/min/1.73m2伴蛋白尿;中位UACR 549(299~1191)mg/g,74%患者UACR≥300 mg/g;平均HbA1c 7.6%±1.1%;平均血钾4.6±0.4 mmol/L(图5)。
表2. FINE-ONE基线人口统计学和临床特征


图5. FINE-ONE基线实验室数据
FINE-ONE研究是首个评估非奈利酮用于T1D合并CKD患者的Ⅲ期研究,其基线数据显示入组患者具有较高的肾脏事件风险和心血管共病率。该研究结果将填补非奈利酮在T1D领域的证据空白,若能证实其肾脏保护作用,将为这一缺乏有效治疗手段的患者群体提供新的治疗选择。目前研究仍在进行中,其最终结果值得期待。
专家点评
非奈利酮重塑糖尿病肾脏疾病管理格局
潘琦教授 北京医院
非奈利酮作为新一代nsMRA,ADA今年新公布的3项研究从多维度探索,进一步证实了其在DKD领域的循证价值。
不同血糖水平患者联合治疗的全新证据
CONFIDENCE亚组分析证实,非奈利酮与恩格列净联合治疗在平均HbA1c 6.4%~>7.9%的T2D合并CKD患者中,降低UACR效果均优于单药治疗(如HbA1c>7.9%组联合治疗较单药治疗多降34%~36%)。这一发现证明了在不同血糖水平的T2D合并CKD患者中联合治疗的普适性,不同血糖水平患者均可从非奈利酮与SGLT2i联合治疗方案中获得额外心肾保护收益。
优化治疗基础上的增量保护
真实世界研究显示,T2D合并早期(1~3期)CKD患者,在ARB+SGLT2i治疗基础上,加用非奈利酮仍可使UACR进一步降低59.35%,且安全性良好,对血糖、血压、eGFR和血钾均无显著影响。该结果揭示了其与现有疗法的机制互补性,为早期DKD患者提供蛋白尿和心肾风险管理新手段,其UACR降幅远超传统方案预期,提示非奈利酮在疾病早期的干预价值。
T1D领域的开拓性探索
FINE-ONE研究作为首个针对T1D合并CKD的Ⅲ期临床研究,入组患者呈现高肾病事件风险(中位UACR 549 mg/g)和高心血管共病特征。若证实疗效,将打破该人群治疗手段有限的困境,成为首个代表nsMRA的T1D心肾保护药物。
从独特机制到心肾保护
ADA发布的新研究数据进一步印证非奈利酮独立于血糖、血压、靶向肾脏纤维化的核心优势。作为国内外指南推荐的心肾保护重要支柱治疗药物之一,非奈利酮不断积累新证据,推动早期多机制心肾保护药物治疗,促进糖尿病合并CKD领域的管理迭代,使更多患者尽早获益。
专家简介

潘琦 教授
北京医院内分泌科主任
医学博士,主任医师,教授,博士研究生导师
中华医学会骨质疏松与骨矿盐分会委员
中华医学会糖尿病学分会糖尿病监测与治疗技术学组副组长
中国老年保健研究会老年骨质疏松分会秘书长
中华医学会老年医学分会内分泌学组副组长
北京医学会糖尿病分会副主任委员
“四大慢病”国家科技重大专项首席项目负责人
主持国家省部级课题9项,参与多项国家重大攻关课题、国家自然科学基金等项目
国内外核心期刊发表论文160余篇
《Diabetes Care中文版》《中华医学杂志》《中华内科杂志》《中华老年医学杂志》《中华全科医学杂志》《中国医学前沿》《中国糖尿病杂志》《中国心血管病杂志》编委
参考文献
1. Agarwal R, et al. Finerenone with Empagliflozin in Chronic Kidney Disease and Type 2 Diabetes. N Engl J Med. 2025 Jun 5. doi: 10.1056/NEJMoa2410659.
2. Rajiv Agarwal, et al. Simultaneous Initiation of Finerenone and Empagliflozin Across the Glycemic Spectrum in the CONFIDENCE Trial.2025 ADA.
3. Vishal Gupta, et al. Evaluating the Effect of Finerenone on Renal Markers in Patients with Diabetic Nephropathy (Stage 1–3) Receiving Angiotensin Receptor Blockers and SGLT2i Therapy. 2025 ADA.
4. Hiddo L. Heerspink, et al. Baseline Characteristics for FINE-ONE — A Randomized Phase III Trial Assessing Finerenone in People with T1D and CKD. 2025 ADA.
2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言