编者按
GLP-1受体激动剂(GLP-1RA)已成为2型糖尿病(T2DM)和肥胖管理的重要药物,其持续控糖、减重及低血糖风险低的优势已被广泛证实。然而,现有GLP-1RA以注射剂型为主,患者依从性仍有提升空间。在此背景下,新型口服小分子GLP-1RA——HRS-7535的研发备受关注。作为全球范围内T2DM领域研发进度第二的口服小分子GLP-1RA,HRS-7535近期两项发表于2025年ADA年会的Ⅱ期临床研究(分别针对T2DM和肥胖人群)揭示了HRS-7535的疗效与安全性,为口服GLP-1RA的临床应用提供了重要证据。以下从研究设计、核心结果及临床启示三方面展开解读。
ADA 2025
研究设计:多中心、双盲、随机对照Ⅱ期试验
该研究(NCT05759897)由北京医院·国家老年医学中心内分泌科郭立新教授牵头,纳入194例18~75岁、二甲双胍单药治疗(≥1000 mg/d,持续8周以上)后血糖控制不佳(糖化血红蛋白[HbA1c] 7.5%~11.0%)的T2DM患者,按1:1:1:1:1随机分配至HRS-7535 15 mg、30 mg、60 mg、90 mg或安慰剂组,每日口服1次,治疗16周(部分剂量需滴定)(图1)。主要终点为16周时HbA1c较基线的变化。
核心结果
(1)基线特征
177例患者完成了16周的治疗周期。基线时,患者的平均年龄为52.3岁,HbA1c为 8.5%,体重指数(BMI)为 26.7 kg/m2,体重73.4 kg,59.3%为男性,约80%的患者每日服用≥1500 mg 二甲双胍(表1)。
表1. 人口统计学和基线特征
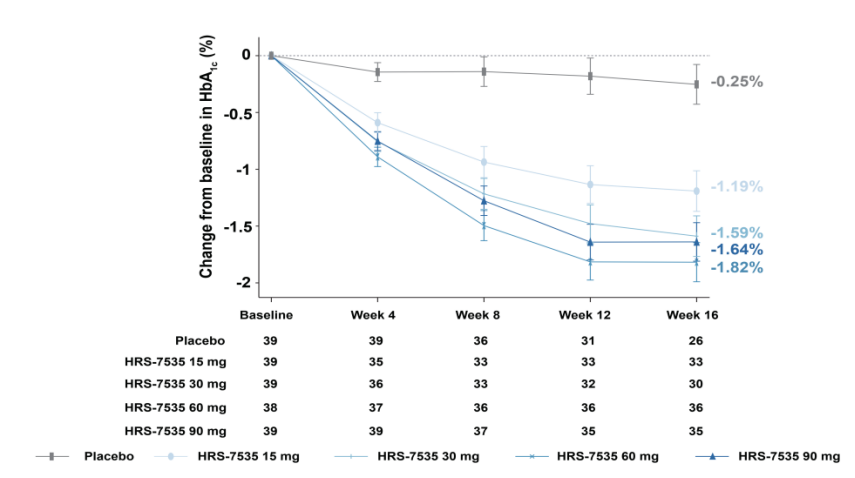
16周时,HRS-7535各剂量组HbA1c降幅分别为-1.19%(15 mg)、-1.59%(30 mg)、-1.82%(60 mg)、-1.64%(90 mg)和-0.25%(安慰剂组),各组降幅均显著优于安慰剂(P < 0.001,图2)。这一结果与现有注射用GLP-1RA的Ⅱ期数据相当。此外,近期公布的礼来Orforglipron Ⅲ期临床ACHIEVE-1研究,结果显示Orforglipron各剂量组HbA1c降幅分别-1.3%(3 mg),-1.6%(12 mg),-1.5%(36 mg),-0.1%(安慰剂组),与HRS-7535降糖效应接近。
(3)体重与代谢指标同步改善
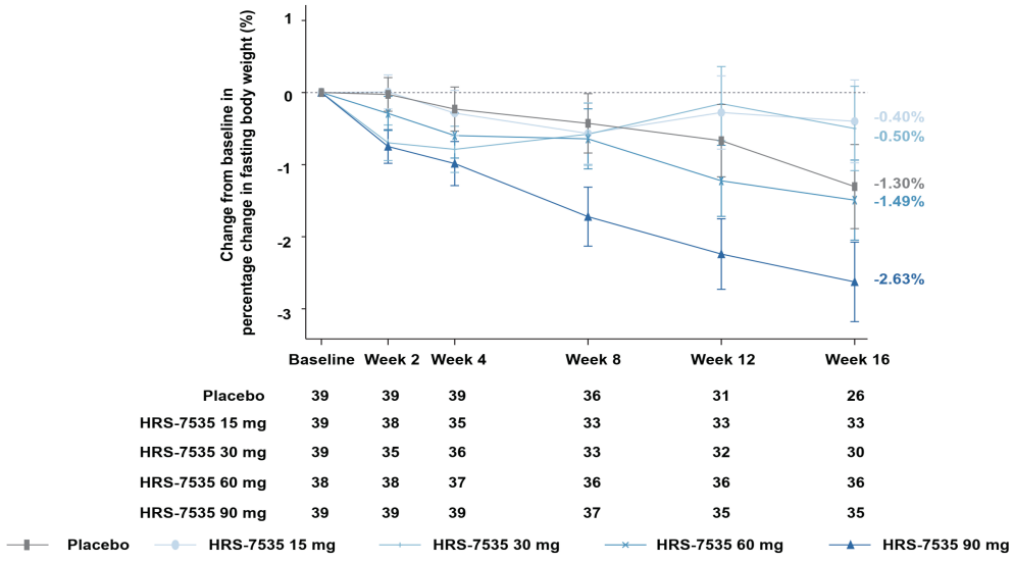
本研究旨在探索 HRS-7535 在二甲双胍控制不佳的T2DM患者中降糖的疗效,入组患者的基线体重及BMI水平较低,但仍可观察到90 mg剂量下明确的体重降低趋势。90 mg组体重较基线降低2.63%,显著优于安慰剂组的1.30%(图3)。此外,HRS-7535各剂量组均观察到空腹血糖(FPG)、餐后2小时血糖(2-h PPG)及腰围的剂量依赖性下降,提示其对代谢功能的综合改善作用。值得注意的是,仅3.2%的HRS-7535组患者进行补救治疗,远低于安慰剂组的30.8%,进一步证实其可强效控糖。
(4)安全性与耐受性良好
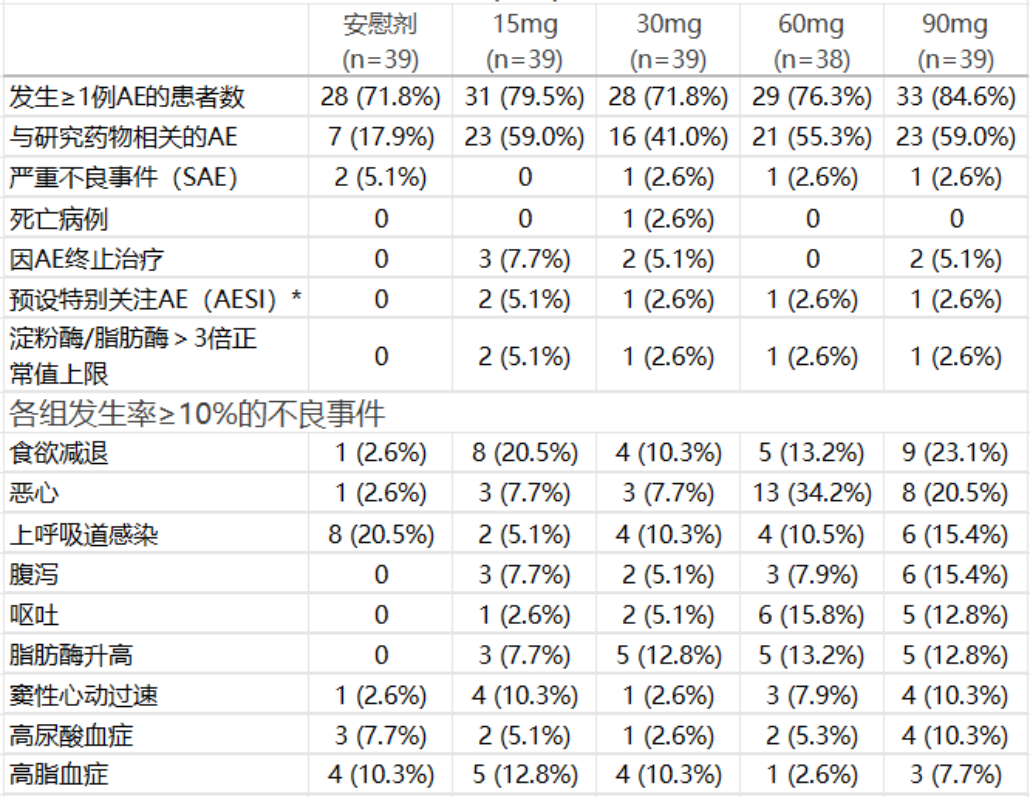
治疗期间,HRS-7535组不良事件(TEAE)发生率为71.8%~84.6%,与安慰剂组(71.8%)相近。主要不良反应为轻度至中度胃肠道症状(恶心7.7%~34.2%、腹泻5.1%~15.4%、呕吐2.6%~15.8%),多发生于剂量滴定阶段,随治疗延长逐渐缓解。仅5.8%患者出现低血糖,均为1级低血糖事件;血清淀粉酶和脂肪酶水平轻度升高,其升高程度在同类品报告范围内。本研究未观察到肝酶升高的趋势,也无其他预期外的安全性信号出现。
表2. 治疗16周期间的不良事件
对于二甲双胍控制不佳的T2DM患者,HRS-7535可显著改善血糖,且口服给药方式有望突破注射治疗的依从性瓶颈。目前正在开展HRS-7535治疗T2DMⅢ期临床研究。
研究二:HRS-7535在非糖尿病肥胖人群中的减重疗效:一项Ⅱ期随机对照研究
研究设计:长周期、多剂量探索肥胖治疗潜力
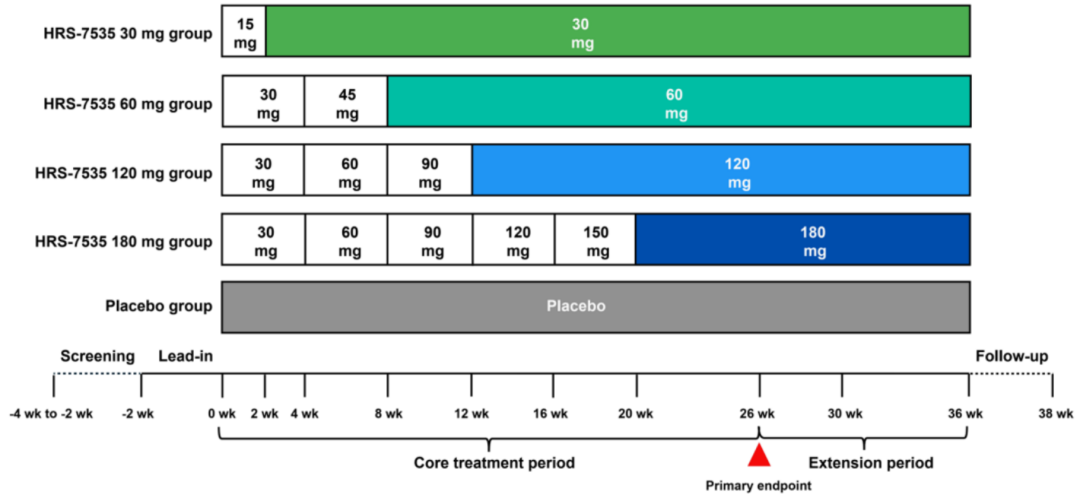
该研究(NCT06621316)由中国人民解放军总医院母义明教授牵头,研究纳入235例BMI 28.0~40.0 kg/m2的不合并糖尿病的肥胖受试者,随机分配至HRS-7535 30 mg、60 mg、120 mg、180 mg或安慰剂组,每日口服1次,双盲治疗36周(含26周核心期+10周延长期)(图4)。主要终点为26周时体重较基线的百分比变化。
核心结果
(1)基线特征
204例患者(86.8%)完成了36周的治疗周期。基线时,患者的平均BMI为32.5 kg/m2,平均体重为91.6 kg,48.5%为女性(表3)。
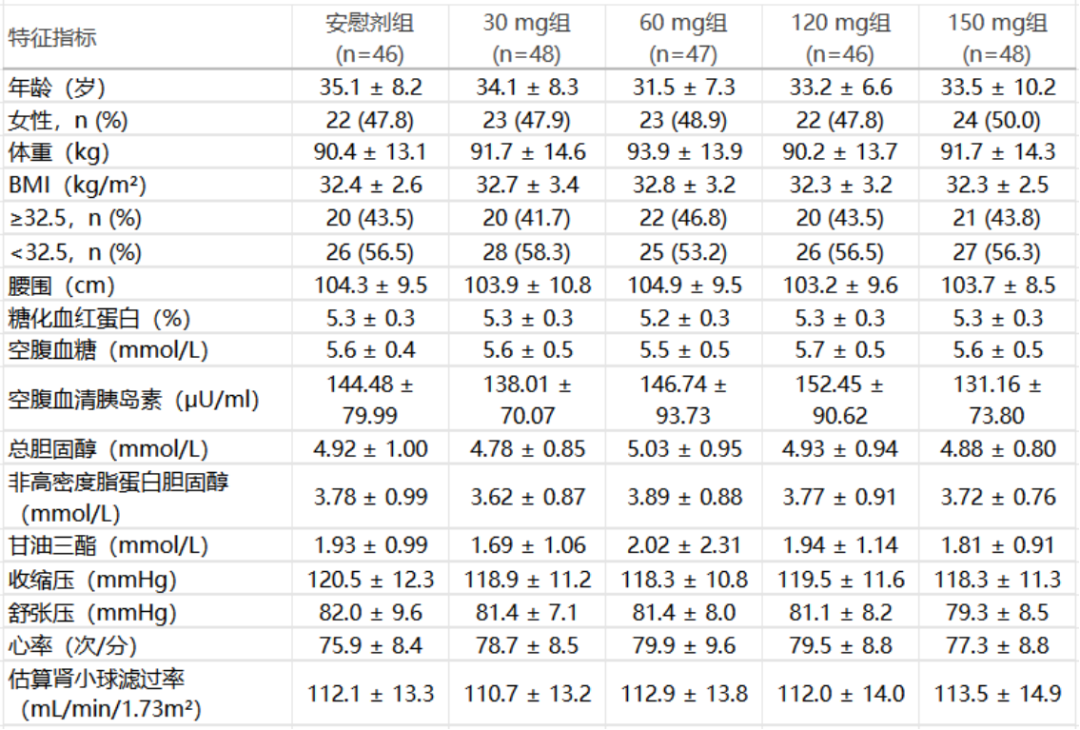
表3. 人口统计学和基线特征
在第26周, HRS-7535 30 mg组、60 mg组、120 mg组、180 mg组体重相对基线变化百分比的最小二乘均值分别为–2.99% ,–7.09%,–6.17%和–9.36%,安慰组为-2.50%,180 mg组相对于安慰剂组体重降低最为显著(P< 0.0001 )(图5)。同时,180 mg组41.7%的患者体重降幅≥10%,而安慰剂组仅6.5%(图6),提示180 mg组在肥胖患者中减重效应的稳健性。值得关注的是,180 mg组的体重降低效果在10周的延伸期内维持,36周时,平均体重降低达9.47%,显示出HRS-7535 180 mg长期体重管理的潜能。
(3)安全性特征与GLP-1类产品类似,具有良好的耐受性
治疗36周内,HRS-7535组TEAE发生率为93.5%~97.9%,略高于安慰剂组(91.3%),主要不良反应为胃肠道症状(恶心16.7%~58.3%、呕吐18.8%~43.8%、腹泻18.8%~26.1%),多为轻中度,且呈现随治疗时间延长而逐步耐受的特征。研究中未观察到肝酶升高趋势,各剂量组脂肪酶、淀粉酶升高>3倍的不良事件发生率低。这表明HRS-7535的安全性与同类药物类似。
表4. 治疗36周期间的不良事件
对于非糖尿病肥胖人群,HRS-7535 60-180 mg可带来显著且持续的体重下降,其中 180 mg 剂量组在肥胖患者中展现出稳健减重效应,且有长期持续减重的潜力。口服剂型兼具高便利性和可及性,既为饮食运动控制不佳的肥胖人群提供口服片的选择,也可作为注射治疗后的长期减重维持方案。目前该分子减重Ⅲ期研究已启动。未来需开展更长周期研究,评估其对肥胖相关并发症(如血脂异常、高血压)的影响。
HRS-7535为代谢性疾病治疗开辟口服新路径
作为新型口服小分子GLP-1RA,HRS-7535在T2DM和肥胖人群中均展现了显著的疗效与良好的安全性,其口服便利性有望改写现有GLP-1RA的治疗格局。对于临床医生而言,这一药物为血糖或体重控制不佳的患者提供了新的治疗选项,尤其适用于偏好口服治疗或对注射剂依从性差的人群。目前,HRS-7535的Ⅲ期研究正在推进中,期待其长期疗效、心血管安全性及与其他药物联合应用的数据进一步揭晓,为代谢性疾病的精准管理提供更充分的证据支持。
参考文献:
1. Lixin Guo, et al. Efficacy and Safety of a Novel Oral Small Molecule Glucagon-Like Peptide-1 Receptor Agonist (HRS-7535) in Type 2 Diabetes Mellitus Patients Inadequately Controlled by Metformin. 2025 ADA.
GLP-1受体激动剂(GLP-1RA)已成为2型糖尿病(T2DM)和肥胖管理的重要药物,其持续控糖、减重及低血糖风险低的优势已被广泛证实。然而,现有GLP-1RA以注射剂型为主,患者依从性仍有提升空间。在此背景下,新型口服小分子GLP-1RA——HRS-7535的研发备受关注。作为全球范围内T2DM领域研发进度第二的口服小分子GLP-1RA,HRS-7535近期两项发表于2025年ADA年会的Ⅱ期临床研究(分别针对T2DM和肥胖人群)揭示了HRS-7535的疗效与安全性,为口服GLP-1RA的临床应用提供了重要证据。以下从研究设计、核心结果及临床启示三方面展开解读。
ADA 2025
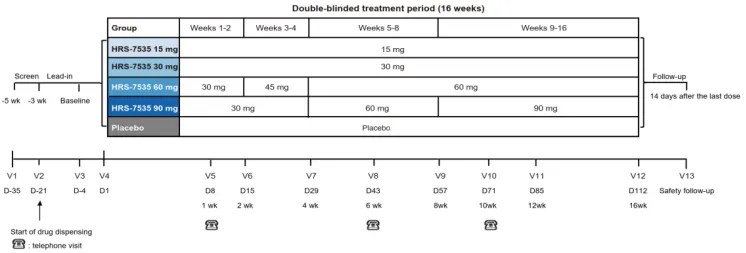
研究设计:多中心、双盲、随机对照Ⅱ期试验
该研究(NCT05759897)由北京医院·国家老年医学中心内分泌科郭立新教授牵头,纳入194例18~75岁、二甲双胍单药治疗(≥1000 mg/d,持续8周以上)后血糖控制不佳(糖化血红蛋白[HbA1c] 7.5%~11.0%)的T2DM患者,按1:1:1:1:1随机分配至HRS-7535 15 mg、30 mg、60 mg、90 mg或安慰剂组,每日口服1次,治疗16周(部分剂量需滴定)(图1)。主要终点为16周时HbA1c较基线的变化。
核心结果
(1)基线特征
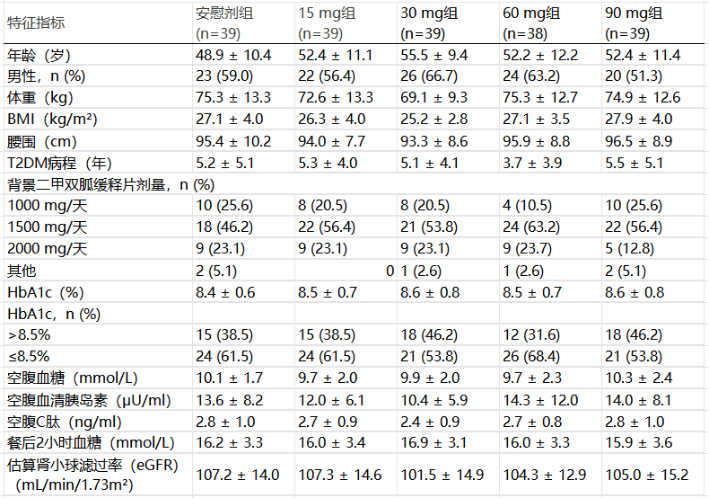
177例患者完成了16周的治疗周期。基线时,患者的平均年龄为52.3岁,HbA1c为 8.5%,体重指数(BMI)为 26.7 kg/m2,体重73.4 kg,59.3%为男性,约80%的患者每日服用≥1500 mg 二甲双胍(表1)。
表1. 人口统计学和基线特征
16周时,HRS-7535各剂量组HbA1c降幅分别为-1.19%(15 mg)、-1.59%(30 mg)、-1.82%(60 mg)、-1.64%(90 mg)和-0.25%(安慰剂组),各组降幅均显著优于安慰剂(P < 0.001,图2)。这一结果与现有注射用GLP-1RA的Ⅱ期数据相当。此外,近期公布的礼来Orforglipron Ⅲ期临床ACHIEVE-1研究,结果显示Orforglipron各剂量组HbA1c降幅分别-1.3%(3 mg),-1.6%(12 mg),-1.5%(36 mg),-0.1%(安慰剂组),与HRS-7535降糖效应接近。
(3)体重与代谢指标同步改善
本研究旨在探索 HRS-7535 在二甲双胍控制不佳的T2DM患者中降糖的疗效,入组患者的基线体重及BMI水平较低,但仍可观察到90 mg剂量下明确的体重降低趋势。90 mg组体重较基线降低2.63%,显著优于安慰剂组的1.30%(图3)。此外,HRS-7535各剂量组均观察到空腹血糖(FPG)、餐后2小时血糖(2-h PPG)及腰围的剂量依赖性下降,提示其对代谢功能的综合改善作用。值得注意的是,仅3.2%的HRS-7535组患者进行补救治疗,远低于安慰剂组的30.8%,进一步证实其可强效控糖。
(4)安全性与耐受性良好
治疗期间,HRS-7535组不良事件(TEAE)发生率为71.8%~84.6%,与安慰剂组(71.8%)相近。主要不良反应为轻度至中度胃肠道症状(恶心7.7%~34.2%、腹泻5.1%~15.4%、呕吐2.6%~15.8%),多发生于剂量滴定阶段,随治疗延长逐渐缓解。仅5.8%患者出现低血糖,均为1级低血糖事件;血清淀粉酶和脂肪酶水平轻度升高,其升高程度在同类品报告范围内。本研究未观察到肝酶升高的趋势,也无其他预期外的安全性信号出现。
表2. 治疗16周期间的不良事件
对于二甲双胍控制不佳的T2DM患者,HRS-7535可显著改善血糖,且口服给药方式有望突破注射治疗的依从性瓶颈。目前正在开展HRS-7535治疗T2DMⅢ期临床研究。
研究二:HRS-7535在非糖尿病肥胖人群中的减重疗效:一项Ⅱ期随机对照研究
研究设计:长周期、多剂量探索肥胖治疗潜力
该研究(NCT06621316)由中国人民解放军总医院母义明教授牵头,研究纳入235例BMI 28.0~40.0 kg/m2的不合并糖尿病的肥胖受试者,随机分配至HRS-7535 30 mg、60 mg、120 mg、180 mg或安慰剂组,每日口服1次,双盲治疗36周(含26周核心期+10周延长期)(图4)。主要终点为26周时体重较基线的百分比变化。
核心结果
(1)基线特征
204例患者(86.8%)完成了36周的治疗周期。基线时,患者的平均BMI为32.5 kg/m2,平均体重为91.6 kg,48.5%为女性(表3)。
表3. 人口统计学和基线特征
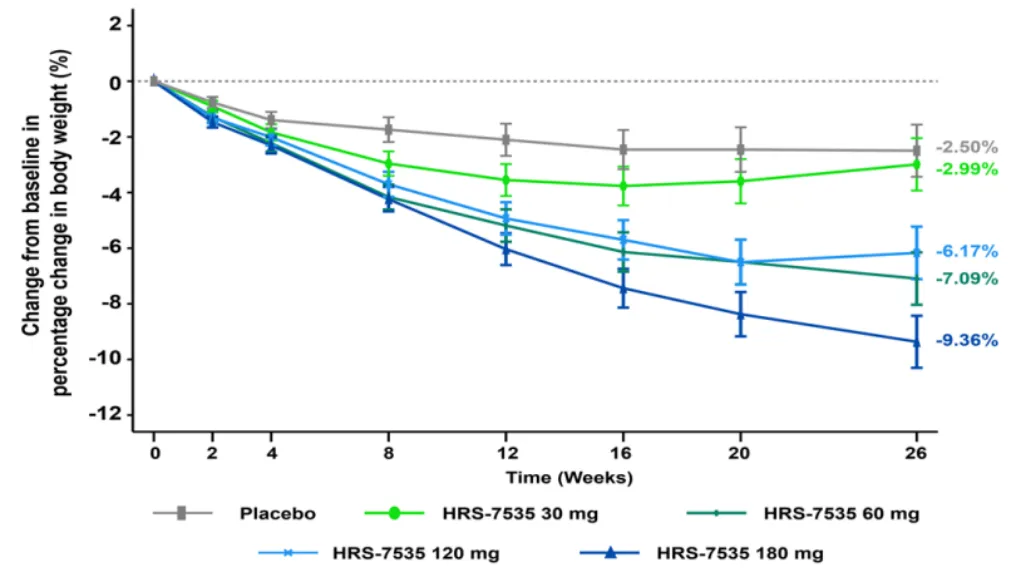
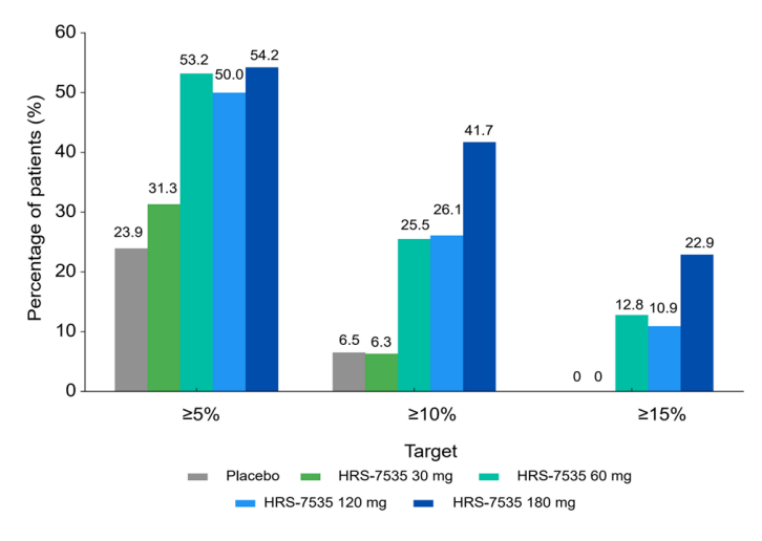
在第26周, HRS-7535 30 mg组、60 mg组、120 mg组、180 mg组体重相对基线变化百分比的最小二乘均值分别为–2.99% ,–7.09%,–6.17%和–9.36%,安慰组为-2.50%,180 mg组相对于安慰剂组体重降低最为显著(P< 0.0001 )(图5)。同时,180 mg组41.7%的患者体重降幅≥10%,而安慰剂组仅6.5%(图6),提示180 mg组在肥胖患者中减重效应的稳健性。值得关注的是,180 mg组的体重降低效果在10周的延伸期内维持,36周时,平均体重降低达9.47%,显示出HRS-7535 180 mg长期体重管理的潜能。
(3)安全性特征与GLP-1类产品类似,具有良好的耐受性
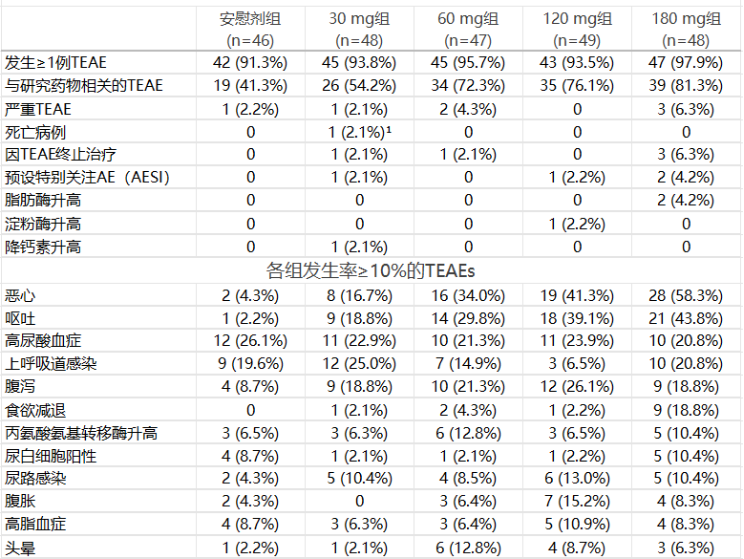
治疗36周内,HRS-7535组TEAE发生率为93.5%~97.9%,略高于安慰剂组(91.3%),主要不良反应为胃肠道症状(恶心16.7%~58.3%、呕吐18.8%~43.8%、腹泻18.8%~26.1%),多为轻中度,且呈现随治疗时间延长而逐步耐受的特征。研究中未观察到肝酶升高趋势,各剂量组脂肪酶、淀粉酶升高>3倍的不良事件发生率低。这表明HRS-7535的安全性与同类药物类似。
表4. 治疗36周期间的不良事件
对于非糖尿病肥胖人群,HRS-7535 60-180 mg可带来显著且持续的体重下降,其中 180 mg 剂量组在肥胖患者中展现出稳健减重效应,且有长期持续减重的潜力。口服剂型兼具高便利性和可及性,既为饮食运动控制不佳的肥胖人群提供口服片的选择,也可作为注射治疗后的长期减重维持方案。目前该分子减重Ⅲ期研究已启动。未来需开展更长周期研究,评估其对肥胖相关并发症(如血脂异常、高血压)的影响。
HRS-7535为代谢性疾病治疗开辟口服新路径
作为新型口服小分子GLP-1RA,HRS-7535在T2DM和肥胖人群中均展现了显著的疗效与良好的安全性,其口服便利性有望改写现有GLP-1RA的治疗格局。对于临床医生而言,这一药物为血糖或体重控制不佳的患者提供了新的治疗选项,尤其适用于偏好口服治疗或对注射剂依从性差的人群。目前,HRS-7535的Ⅲ期研究正在推进中,期待其长期疗效、心血管安全性及与其他药物联合应用的数据进一步揭晓,为代谢性疾病的精准管理提供更充分的证据支持。
参考文献:
1. Lixin Guo, et al. Efficacy and Safety of a Novel Oral Small Molecule Glucagon-Like Peptide-1 Receptor Agonist (HRS-7535) in Type 2 Diabetes Mellitus Patients Inadequately Controlled by Metformin. 2025 ADA.
2. Weijun Gu, et al. Efficacy and Safety of a Novel Oral Small Molecule Glucagon-Like Peptide-1 Receptor Agonist (HRS-7535) in Chinese adults with obesity without diabetes. 2025 ADA.












 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言