为何迄今为止双胰岛素制剂只有德谷门冬双胰岛素一种?缘何中国权威指南将双胰岛素类似物以单独类别作为胰岛素起始治疗方案推荐?当我们把胰岛素结构类比为火车车厢后,以上问题的答案很快跃然纸上……
1921这个年份在内分泌乃至整个医学领域都具有里程碑的意义。
正是在这一年,科学家从狗的胰腺中成功提取出胰岛素。次年,人类历史上首次将胰岛素应用于临床,从此糖尿病无药可治时代成为序章,糖尿病治疗新纪元正式开启[1]。
作为1型糖尿病(T1DM)患者赖以生存、2型糖尿病(T2DM)患者(尤其是病程长的患者)控制血糖、减少并发症风险的有效治疗手段[2],胰岛素不断发展创新,从动物胰岛素到人胰岛素,再到胰岛素类似物,以及近年来诞生的双胰岛素制剂——德谷门冬双胰岛素,其有效性、安全性和便利性在不断提升。既往研究大多是基于临床试验得到的结论,而本次特别邀请到中国医学科学院药物研究所吕晓希教授,深入分子机构,探寻双胰岛素制剂优势之所在。
多重构象,揭开胰岛素制剂神秘面纱
通过单一注射实现对于空腹以及餐后血糖完美调控的胰岛素制剂,是科学家一直以来的研发方向。纵观胰岛素界,基础胰岛素和速效胰岛素品类多种多样,但是并非所有的基础胰岛素类似物和速效胰岛素类似物都能合成双胰岛素。
成功来之不易。基于甘精胰岛素U100的药学性质,其在pH 4制剂可溶,在皮下组织的中性环境(pH 7.4)成微沉淀物,使其能够缓慢释放,达到延长半衰期的目的[3]。但将甘精胰岛素U100与速效胰岛素混合后,甘精胰岛素在进行沉淀的过程中可能会结合速效胰岛素,导致速效胰岛素无法快速发挥生物学功能(图1),我们就会观察到所谓“肩效应”,这并不是一个成功的尝试,吕教授表示。
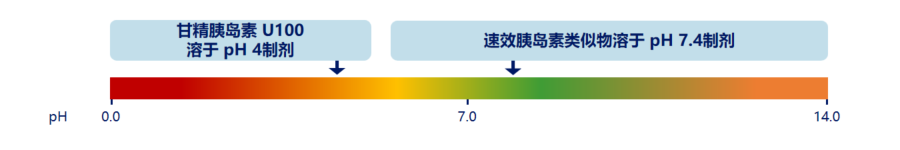
图1 甘精胰岛素和速效胰岛素类似物的等电点
地特胰岛素是第一个使用脂肪酸酰化技术的胰岛素类似物,但是它仍然不能和速效胰岛素形成双胰岛素。这是由于胰岛素多种多样构象带来的药物相互作用[4]。
胰岛素的结构非常复杂,其包括T6、T3R3、R6构象的胰岛素六聚体。为了将这些扑朔迷离的结构简单化,吕教授进行了生动的比喻。
吕教授指出,我们可以把每个六聚体的胰岛素比喻成火车的车厢,T6构象的车厢具有两个挂钩、T3R3构象的车厢仅有一端有挂钩、R6构象的车厢没有挂钩。如此地特胰岛素、德谷胰岛素、门冬胰岛素,在制剂中和皮下注射后所展现出的模式完全不同(图2)。门冬胰岛素在制剂中为R6构象,以单六聚体的形式存在,进入制剂中后,门冬胰岛素变为T6构象。
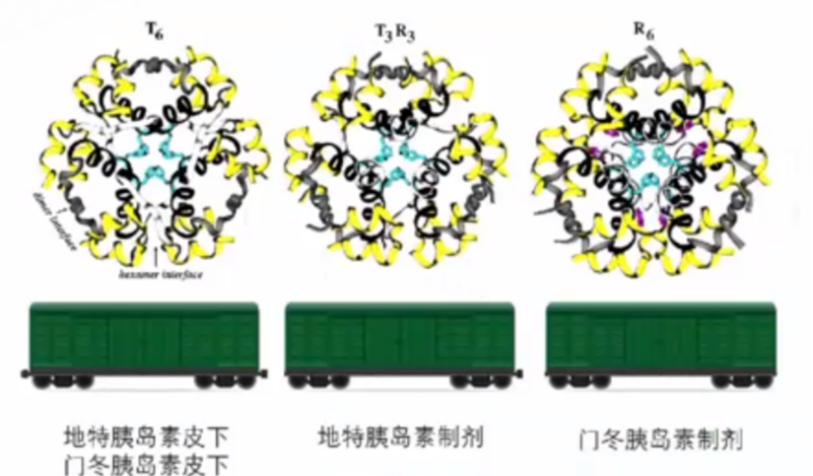
图2 胰岛素制剂的不同结构
在制剂中,地特胰岛素为T3R3构象,每节车厢上靠仅有的一个挂钩相互连接,形成双六聚体结构。但是皮下注射后,地特胰岛素会形成T6构象,加上两端通过脂肪酸酰化技术链接的白蛋白,从而缓慢起效发挥餐时胰岛素作用。由此看来,地特胰岛素和门冬胰岛素组合失败的原因便迎刃而解,其注射到皮下后,可能会形成地特胰岛素-门冬胰岛素的异源六聚体,所以,门冬胰岛素就失去了其快速进入血液循环的可能性,被地特胰岛素所“拖累”。
“那同样来自于脂肪酸酰化技术的德谷胰岛素,为什么不会和门冬胰岛素在皮下发生药物相互作用,它们就不会形成这样的异源六聚体吗?”
一切的源头还要从结构出发。吕教授表示,德谷胰岛素进一步改造了脂肪酸酰化技术,其脂肪酸酰化技术的侧链更长。德谷胰岛素在制剂中为T3R3构象,其以双六聚体形式存在。德谷胰岛素注射到皮下后,其结构就发生了相应的变化,将脂肪酸长链束缚在车厢两端的苯酚溶解了,侧面挂钩被快速解离,德谷胰岛素不再通过先前的胰岛素构象本来的挂钩相连接,而是通过脂肪酸酰化技术的长链结合在一起(图3)。而在皮下的门冬胰岛素因为没有脂肪酸酰化修饰,所以就挤不上这趟列车。这趟列车上只会有一个又一个的德谷胰岛素同源六聚体形成了长串样结构,稳定地对空腹血糖进行干预;而门冬胰岛素由于其六聚体的快速崩解,迅速入血发挥降糖作用,所以德谷门冬双胰岛素变成了目前为止,更为智能的双时相胰岛素制剂[4]。
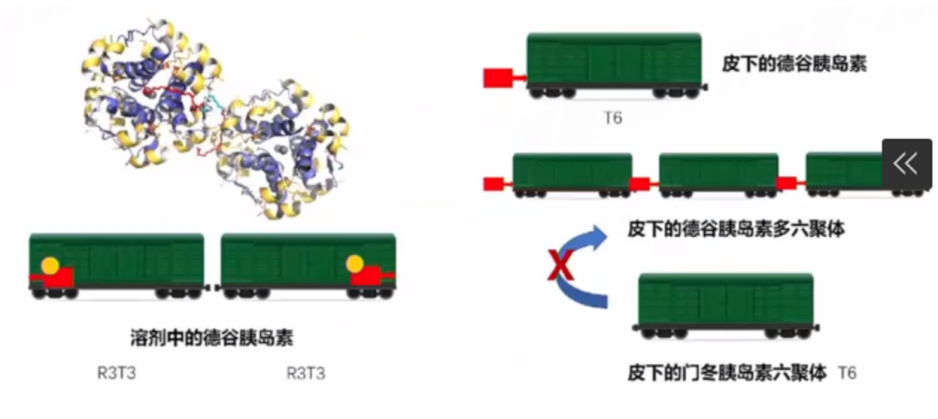
图3 德谷门冬双胰岛素制剂中两组分在不同状态下的结构
德谷门冬双胰岛素包含70%德谷胰岛素和30%门冬胰岛素,无论在制剂中还是皮下注射后,两组分均独立存在且药物代谢动力学完全分离,可各自发挥降低空腹和餐后高血糖作用[4]。德谷门冬双胰岛素被《中国2型糖尿病防治指南(2020年版)》(以下简称“CDS指南”)作为单独类别推荐,CDS指南指出:德谷门冬双胰岛素可作为胰岛素起始治疗方案之一[2]。
结构明晰,优势跃然于纸上
评价降糖药物的疗效,有效性、安全性、便捷性缺一不可,分子结构的独特性令德谷门冬双胰岛素获益匪浅。在有效性方面,德谷门冬双胰岛素可兼顾全天血糖控制,可有效降低糖化血红蛋白(HbA1c)。相较于甘精胰岛素U100,德谷门冬双胰岛素每日注射一次HbA1c控制更优、达标率更高(P<0.01)[5];相较于门冬胰岛素30,两者HbA1c控制相似,但德谷门冬双胰岛素组空腹血糖(FPG)控制显著更优(P<0.0001)[6]。
在安全性方面,预混胰岛素多年来被广泛应用于临床,但是其存在一定的局限性,预混胰岛素中的精蛋白会影响速效胰岛素的释放过程,注射到皮下后会有部分发挥速效作用的胰岛素不能快速崩解,被精蛋白所拖累,由此产生了 “肩效应”,容易诱发餐后低血糖[3,7]。得益于德谷门冬双胰岛素独特的理化性质,其可避免“肩效应”的发生,降低低血糖发生风险。相较于门冬胰岛素30,德谷门冬双胰岛素夜间确证性低血糖事件和总体确证性低血糖事件发生风险显著降低47%(P=0.0056)和43%(P=0.0001)[6]。相较于甘精胰岛素U100,德谷门冬双胰岛素可降低确证性低血糖事件发生率27%、夜间低血糖事件发生率25%[5]。
在依从性方面,德谷门冬双胰岛素在制剂中为澄清溶液,无需混匀,可避免预混胰岛素因混匀不充分而出现的注射剂量不准确的局限,相比预混胰岛素每年可少摇14600次;相较于基础-餐时治疗方案,德谷门冬双胰岛素在疗效相当的情况下,可减少注射次数,并能随主餐给药,注射时间灵活,治疗方案便捷性提高[3,8]。
小结
由此可见,德谷门冬双胰岛素制剂的出现并不是偶然,而是研发过程中,分子生物学的进步、蛋白质化学的进步以及研发人员经过数以千万次尝试后的必然。在众多基础胰岛素+餐时胰岛素组合中,将德谷胰岛素+门冬胰岛素两组分进行完美融合,最终诞生出兼顾有效性、安全性、依从性的德谷门冬双胰岛素制剂。其上市已近4年,被临床广泛应用,也得到了众多医生和患者的认可,助力我国糖尿病患者血糖管理优质达标。
专家简介

吕晓希
中国医学科学院,北京协和医学院药物研究所分子免疫药理课题组副研究员,天然药物活性物质与功能国家重点实验室成员。从事非感染型慢性炎性疾病发病机制研究及创新多肽药物研发。负责多个国家自然科学基金项目及省部级基金项目,承担多个国家级新药研发项目。在Immunity,Nat Commun,Cancer Cell, Autophagy,APSB,STTT等杂志发表SCI论文三十余篇,申请国家专利10项。研究工作获得中华医学会科技奖三等奖、教育部自然科学奖二等奖、北京市科学技术奖三等奖。
参考文献
[1].Hegele RA, et al. Lancet Diabetes Endocrinol . 2020 Dec;8(12):971-977.
[2].中华医学会糖尿病学分会. 中华糖尿病杂志, 2021, 13(4): 315-409.
[3].Haahr H,et al. Clin Pharmacokinet. 2017 Apr;56(4):339-354.
[4].Jonassen et al. Pharm Res 2012;29:2104–14.
[5].Onishi Y,et al.Diabetes Obes Metab. 2013 Sep;15(9)826-32.
[6].Yang et al, Diabetes Obes Metab, 2019; 21(7):1652-1660.
[7].Atkin S, et al. Ther Adv Chronic Dis. 2015;6:375–88.
[8].Kalra S, et al. Diabetes Ther. 2015;6:101-11.
“此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场”
2 comments










 京公网安备 11010502033361号
京公网安备 11010502033361号
发布留言